Indikationer
Budesonide Teva Pharma suspension för nebulisator är avsett för vuxna, ungdomar och barn över 6 månader.
Astma
Budesonide Teva Pharma suspension för nebulisator är avsett för bronkialastma hos patienter där användning av en inhalationsspray eller pulverinhalator bedöms som otillfredsställande eller olämplig.
Pseudokrupp
Mycket svår pseudokrupp (laryngitis subglottica) som kräver sjukhusbehandling.
Kronisk obstruktiv lungsjukdom (KOL)
Exacerbationer av kroniskt obstruktiv lungsjukdom (KOL) som alternativ till systemiska kortikosteroider.
Kontraindikationer
Överkänslighet mot den aktiva substansen (budesonid) eller mot något hjälpämne som anges i avsnitt Innehåll.
Dosering
Dosering
Generellt
Budesonidsuspension för nebulisator inhaleras med hjälp av en lämplig nebulisator (jetnebulisator försedd med munstycke eller ansiktsmask). Mängden budesonid som en patient får i sig via nebulisatorn varierar och är beroende av faktorer som:
-
nebuliseringstiden
-
använd volym
-
nebulisatorns egenskaper
-
förhållandet mellan patientens in- och utandningsvolym och dead space.
-
användning av ansiktsmask eller munstycke.
Astma
Dosen bör ges två gånger per dygn. Administrering en gång per dygn kan övervägas vid lindrig till måttlig stabil astma.
Initial dosering
Initialdosen ska anpassas efter sjukdomens svårighetsgrad och därefter justeras individuellt. Följande doseringar rekommenderas, men minsta effektiv dos bör alltid eftersträvas.
Barn från 6 månader och uppåt
0,25–1 mg per dygn. För patienter som får underhållsbehandling med orala steroider bör en högre initial dosering, upp till 2 mg per dygn, övervägas.
Vuxna (inklusive äldre) samt barn och ungdomar över 12 år
0,5–2 mg per dygn. I mycket svåra fall kan dosen ökas ytterligare.
Underhållsdos
Underhållsdosen ska anpassas till patientens individuella behov med hänsyn till sjukdomens svårighetsgrad samt behandlingssvaret. När den önskade kliniska effekten har uppnåtts bör underhållsdosen minskas till lägsta möjliga dos som krävs för att hålla symtomen under kontroll.
Barn från 6 månader och uppåt
0,25–1 mg per dygn.
Vuxna (inklusive äldre) samt barn och ungdomar över 12 år
0,5–2 mg per dygn. I mycket svåra fall kan dosen ökas ytterligare.
Pseudokrupp
Hos spädbarn och barn med pseudokrupp, är den vanligen använda dosen 2 mg nebuliserad budesonid. Det ges som en engångsdos, eller som två 1 mg-doser med 30 minuters mellanrum. Doseringen kan upprepas var 12:e timme i högst 36 timmar eller tills klinisk förbättring erhålls.
Pediatrisk population
Säkerhet och effekt för nebuliserad budesonid för barn yngre än sex månader har ännu inte fastställts.
Exacerbationer av KOL
Patienter bör behandlas med en dygnsdos på 4 till 8 mg av budesonidsuspension för nebulisator, uppdelat på två till fyra doseringstillfällen tills klinisk förbättring uppnås, men inte längre än 10 dagar.
Vid behandling i hemmet ska instruktioner om korrekt användning av nebulisator tillhandahållas.
Användning av budesonidsuspension för nebulisator har inte studerats hos KOL-patienter med lunginflammation eller som kräver intubering.
Administreringssätt
För inhalation.
Astma
Administrering en gång per dygn
Administrering en gång per dygn bör övervägas till barn och vuxna med lindrig till måttlig, stabil astma och med en underhållsdos på mellan 0,25 mg och 1 mg budesonid per dygn.
Administrering en gång per dygn kan sättas in både hos patienter som inte behandlas med kortikosteroider och till välkontrollerade patienter som redan behandlas med inhalationssteroider. Dosen kan ges morgon eller kväll. Vid försämring av astman bör dygnsdosen ökas till två doser per dygn.
Effekttillslag
En förbättring av astman efter administrering av budesonid kan ses inom 3 dagar efter att behandlingen påbörjats. Maximal effekt uppnås först efter 2–4 veckors behandling.
Patienter som underhållsbehandlas med orala glukokortikosteroider
Budesonidsuspension för nebulisator kan möjliggöra utbyte eller signifikant reduktion av dosen av orala glukokortikosteroider samtidigt som astmakontrollen upprätthålls. När övergång från orala steroider till inhalerad budesonid påbörjas ska patienten vara i en relativt stabil fas.
Initialt ska en hög dos av inhalerad budesonid ges. Den kan ges tillsammans med den tidigare använda orala glukokortikosteroiden under ungefär 10 dagar. Den orala dosen minskas sedan (med exempelvis 2,5 mg prednisolon eller motsvarande dos per månad) till lägsta möjliga nivå. Hos många patienter är det möjligt att helt ersätta den orala glukokortikosteroiden med inhalerad budesonid.
Vid nedtrappning av systemiska kortikosteroider kan vissa patienter uppleva symptom orsakade av steroidutsättningen, t.ex. led- och/eller muskelvärk, kraftlöshet och depression, och även en försämrad lungfunktion. Dessa patienter ska rådas att fortsätta behandlingen med inhalerad budesonid, men de bör även undersökas för eventuella tecken på binjurebarkinsufficiens. Om sådana tecken föreligger ska dosen av den systemiska kortikosteroiden tillfälligt ökas, för att sedan trappas ned i en ännu långsammare takt. Under perioder med stress eller svåra astmaattacker kan patienter som befinner sig i övergångsfasen behöva behandling med systemiska kortikosteroider. För ytterligare information om utsättning av kortikosteroider, se avsnitt Varningar och försiktighet.
Doseringsschema
Nedanstående schema bör följas:
|
Dosering i mg |
Volym budesonidsuspension för nebulisator |
||||
|
0,125 mg/ml |
0,25 mg/ml |
|
0,5 mg/ml |
||
|
0,25 |
2 ml | ||||
|
0,5 |
4 ml |
eller |
2 ml | ||
|
0,75*** |
2 ml |
plus |
2 ml | ||
|
1* |
4 ml |
eller |
2 ml |
||
|
1,5** |
2 ml |
plus |
2 ml |
||
|
2 |
4 ml |
||||
-
* antingen 2 endosbehållare med budesonidsuspension för nebulisator 0,25 mg/ml eller en endosbehållare med budesonidsuspension för nebulisator 0,5 mg/ml.
-
** en endosbehållare med budesonidsuspension för nebulisator 0,25 mg/ml plus en endosbehållare med budesonidsuspension för nebulisator 0,5 mg/ml.
-
*** en endosbehållare med budesonidsuspension för nebulisator 0,125 mg/ml plus en endosbehållare med budesonidsuspension för nebulisator 0,25 mg/ml.
Uppdelning av dos och blandbarhet
Budesonidsuspension för nebulisator kan blandas med 0,9 % natriumkloridlösning, liksom med lösningar för inhalation innehållande terbutalin, salbutamol, natriumkromoglikat eller ipratropium.
Nebulisator
Budesonidsuspension för nebulisator måste administreras med jetnebulisator försedd med munstycke eller ansiktsmask. Nebulisatorn ska anslutas till en luftkompressor med lämpligt luftflöde (6 8 l/min), och fyllnadsvolymen ska vara 2-4 ml.
Prestanda (levererad dos) hos olika nebulisatorer kan variera även för samma modell och tillverkare.
Obs! Ultraljudsnebulisatorer är inte lämpliga för nebulisering av budesonidsuspension för inhalation och kan därför inte rekommenderas
Bruksanvisning
För att minimera risken för candidainfektion i munhåla och svalg bör patienten skölja ur munnen med vatten efter inhalation.
-
Ställ iordning nebulisatorn enligt tillverkarens instruktion.
-
Öppna folieförpackningen och ta ut remsan med endosbehållare. Tag en endosbehållare från remsan genom att vrida och dra (Figur 1).
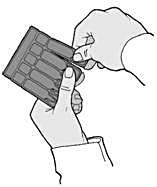
-
Skaka endosbehållaren varsamt under ca 10 sekunder eller tills ingen fällning syns.
-
Håll endosbehållaren upprätt och vrid av den övre delen (Figur 2).
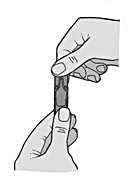
-
Vänd endosbehållaren upp och ned och tryck ur innehållet i nebulisatorbehållaren (kammaren) (Figur 3).
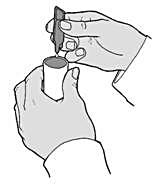
-
Endosbehållaren är avsedd för engångsbruk. Efter varje administrering ska därför eventuellt oanvänt läkemedel kastas och nebulisatorbehållaren ska rengöras. Tvätta nebulisatorkammaren och munstycket eller ansiktsmasken med varmt vatten eller milt rengöringsmedel. Skölj väl och torka genom att ansluta nebulisatorkammaren till kompressorn.
-
Patienterna bör instrueras att skölja munnen med vatten efter inhalation för att undvika svampinfektion i munhålan.
-
Patienterna bör också tvätta ansiktet med vatten efter att ha använt ansiktsmasken för att förhindra hudirritation i ansiktet.
Varningar och försiktighet
Budesonidsuspension för nebulisator är inte avsett för behandling av akut dyspné eller akut svår astma (status asthmaticus). Dessa tillstånd ska behandlas med kortverkande beta-2-stimulerare eller andra bronkodilaterare.
Särskild försiktighet måste iakttas beträffande patienter som överförs från orala kortikosteroider till inhalerade kortikosteroider. Patienternas tillstånd bör vara relativt stabilt innan man påbörjar behandling med en hög dos inhalerad kortikosteroid som adderas till underhållsdosen av systemisk kortikosteroid. Efter ungefär 10 dagar påbörjas utsättandet av den systemiska kortikosteroiden med en stegvis minskning av dygnsdosen (exempelvis 2,5 mg prednisolon eller motsvarande, varje månad) till lägsta möjliga dos. Eventuellt kan oral dos av kortikosteroid fullständigt ersättas med inhalerad dos. Överförda patienter som har nedsatt binjurebarksfunktion kan behöva tillförsel av systemisk kortikosteroid under perioder av stress, t.ex. kirurgi, infektioner eller vid försämring av astman.
Patienter som tidigare krävt höga doser av kortikosteroider eller som under lång tid fått behandling med den högsta rekommenderade dosen av inhalerade kortikosteroider kan också vara i riskzonen för binjurebarkinsufficiens. Dessa patienter kan eventuellt uppvisa tecken och symtom på binjureinsufficiens då de utsätts för svår stress. Tillägg av systemiska kortikosteroider bör övervägas i samband med perioder av stress eller elektiv kirurgi.
Under överföringen från oral terapi till inhalation av budesonid, kan symptom uppkomma som tidigare varit undertryckta av den systemiska glukokortikosteroidbehandlingen t.ex. symtom på allergisk rinit, eksem, muskel- och ledsmärtor. Specifik tilläggsbehandling bör ges vid sådana tillstånd.
Patienter som tidigare varit beroende av orala kortikosteroider kan få nedsatt binjurebarksfunktion efter långtidsbehandling med systemiska kortikosteroider. Återhämtningen kan ta lång tid efter utsättning av långvarig oral kortikosteroidbehandling. Risken för nedsatt binjurebarksfunktion kan därför bestå under en längre tid när patienter som är beroende av orala glukokortikosteroider överförs till budesonid. Under sådana omständigheter ska hypotalamus-hypofys-binjurebarkfunktionen (HPA) övervakas regelbundet.
En del patienter kan uppleva allmän ospecifik sjukdomskänsla under nedtrappningen av systemiska steroider trots upprätthållande eller till och med förbättring av andningsfunktionen. Dessa patienter ska uppmuntras att fortsätta inhalationsbehandlingen med budesonid och nedtrappningen av oral kortikosteroid, såvida inte de kliniska symtomen motsäger detta, t.ex. tecken som tyder på binjurebarksinsufficiens. I dessa fall kan ibland en tillfällig ökning av den orala steroiddosen vara nödvändig.
Eliminering av kortikosteroider kan påverkas av nedsatt leverfunktion. Man får en minskad elimineringshastighet och därmed en högre systempåverkan. Var uppmärksam på möjliga systembiverkningar. Farmakokinetiken för budesonid efter intravenös administrering var jämförbar för patienter med levercirros som för friska frivilliga. Oral administrering av budesonid påverkade farmakokinetiken hos patienter med nedsatt leverfunktion: den systemiska biotillgängligheten ökade. Detta kan vara kliniskt signifikant hos patienter med gravt nedsatt leverfunktion.
Liksom vid annan inhalationsterapi kan paradoxal bronkospasm uppträda med väsande andning omedelbart efter dosering. Om detta uppträder ska behandlingen omedelbart avbrytas, patienten undersökas och alternativ terapi initieras vid behov.
När akut dyspné uppkommer trots en noga övervakad behandling ska en snabbverkande bronkodilaterare användas och ny medicinsk bedömning övervägas. Om astmasymptomen inte kan kontrolleras adekvat trots maximala doser av inhalerad kortikosteroid, kan patienten behöva korttidsbehandling med systemisk kortikosteroid. I sådana fall ska inhalationsbehandlingen med kortikosteroid fortsättas tillsammans med den systemiska behandlingen.
Systempåverkan kan förekomma vid inhalationsbehandling med kortikosteroider, särskilt vid höga doser under längre behandlingsperioder. Det är mindre troligt att denna påverkan uppträder vid inhalationsbehandling jämfört med när kortikosteroider ges peroralt. Eventuella systembiverkningar inkluderar Cushings syndrom, Cushingliknande symtombild, binjuresuppression, hämmad längdtillväxt hos barn och ungdomar, minskad bentäthet, katarakt, glaukom, och mer sällsynt en rad psykologiska störningar eller beteendestörningar innefattande psykomotorisk hyperaktivitet, sömnstörningar, oro, depression eller aggression (särskilt hos barn). Det är därför angeläget att dosen av kortikosteroid i inhalation titreras till den lägsta dos vid vilken effektiv systemkontroll av astman uppnås.
Synrubbning kan rapporteras vid systemisk och topisk användning av kortikosteroider. Om en patient inkommer med symtom såsom dimsyn eller andra synrubbningar bör man överväga att remittera patienten till en oftalmolog för utredning av möjliga orsaker. Dessa kan innefatta katarakt, glaukom eller sällsynta sjukdomar, såsom central serös korioretinopati (CSCR), som har rapporterats efter användning av systemiska och topiska kortikosteroider.
Försämring av kliniska symtom på astma kan bero på akut bakteriell luftvägsinfektion och lämplig antibiotikabehandling kan behövas. Sådana patienter kan behöva öka dosen av inhalerad budesonid och korttidsbehandling med orala steroider kan behövas. Snabbverkande bronkodilaterare för inhalation ska användas som akutmedicinering för att lindra akuta astmasymtom.
Särskild försiktighet bör iakttas för patienter med aktiv och tyst lungtuberkulos, liksom för patienter med svamp- eller virusinfektioner i luftvägarna. Detta ska beaktas vid behandling av astma hos patienter som också har luftvägsinfektion; både astman och luftvägsinfektionen ska behandlas adekvat.
Hos patienter med hög slemsekretion i luftvägarna kan korttidsbehandling med orala kortikosteroider vara nödvändig.
Oral candidos kan uppkomma vid behandling med kortikosteroider för inhalation. I sådana fall kan behandling med lämpligt antimykotikum vara nödvändig och för vissa patienter kan det vara nödvändigt att avsluta behandlingen med kortikosteroider (se även avsnitt Dosering).
För att undvika hudirritationer rekommenderas användning av munstycke framför ansiktsmask vid inhalation av kortikosteroider. Tvätta ansiktet med vatten efter behandling om ansiktsmask används.
Tvätta nebulisatorbehållaren och munstycket eller ansiktsmasken i varmt vatten och använd ett milt diskmedel efter varje användning. Skölj ordentligt och torka behållaren genom att ansluta den till kompressorn.
Samtidig behandling med ketokonazol, HIV-proteashämmare eller andra potenta CYP3A4-hämmande läkemedel bör undvikas. Om detta inte är möjligt bör intervallet mellan behandlingarna vara så lång som möjligt (se avsnitt Interaktioner).
Pneumoni hos patienter med KOL
En ökning av incidensen av pneumoni, inklusive pneumoni som kräver inläggning på sjukhus, har observerats hos patienter med KOL som får inhalerade kortikosteroider. Det finns viss evidens för en ökad risk för pneumoni vid höjningar av steroiddosen, men detta har inte slutgiltigt påvisats i alla studier.
Det finns ingen slutgiltig klinisk evidens för skillnader inom klassen inhalerade kortikosteroider när det gäller pneumoniriskens storleksordning.
Läkare bör vara fortsatt vaksamma när det gäller möjlig utveckling av pneumoni hos patienter med KOL eftersom de kliniska tecknen på sådana infektioner överlappar symtomen på KOL- exacerbationer.
Riskfaktorer för pneumoni hos patienter med KOL inkluderar nuvarande rökning, hög ålder, lågt kroppsmasseindex (BMI) och allvarlig KOL.
Pediatrisk population
Det föreligger otillräcklig data gällande budesonids eventuella tillväxthämmande effekt för barn i åldrarna 6 månader till 4 år.
Påverkan på tillväxt
Hos barn och ungdomar som behandlas med inhalationssteroider under längre tid bör kroppslängden följas regelbundet. Om tillväxten är hämmad skall behandlingen utvärderas på nytt och målet ska vara att minska dosen inhalationssteroid till den lägsta nivån. Fördelarna med kortikosteroidbehandling bör noggrant vägas mot de potentiella riskerna för hämmad tillväxt. Man bör även överväga att remittera patienten till barnallergolog.
Interaktioner
Metabolism av budesonid sker primärt genom CYP3A4. Hämmare av detta enzym, t.ex. ketokonazol, itrakonazol och HIV-proteashämmare (ritonavir och sakvinavir) kan därför flerfaldigt öka den systemiska exponeringen för budesonid (se avsnitt Varningar och försiktighet). Eftersom data saknas för att ge doseringsrekommendationer bör kombinationen undvikas. Om det ej är möjligt bör intervallet mellan behandlingarna vara så långt som möjligt och en minskning av budesoniddosen kan också övervägas.
Samtidig behandling med CYP3A-hämmare, inklusive läkemedel som innehåller kobicistat, väntas öka risken för systemiska biverkningar. Kombinationen ska undvikas såvida inte nyttan uppväger den ökade risken för systemiska biverkningar av kortikosteroider, och om så är fallet ska patienter övervakas avseende systemiska biverkningar av kortikosteroider.
Eftersom binjurefunktionen kan vara hämmad, kan ett ACTH‑stimuleringstest för diagnostisering av hypofysinsufficiens visa felaktiga resultat (låga värden).
Begränsade data för den här interaktionen och inhalerat budesonid i hög dos indikerar att markanta ökningar i plasmanivåerna (i medeltal fyrfaldigt) kan uppstå om itrakonazol i doser om 200 mg dagligen administreras samtidigt med inhalerat budesonid (singeldos om 1000 µg).
Andra potenta hämmare av CYP 3A4 såsom erytromycin och klaritromycin ger sannolikt också en markant ökning av plasmakoncentrationerna för budesonid.
Förhöjda plasmakoncentrationer och ökade effekter av kortikosteroider har observerats hos kvinnor som samtidigt behandlats med östrogener och kontraceptiva steroider, men ingen sådan effekt har observerats med budesonid och samtidigt intag av kombinerade lågdos-p-piller.
Samtidig användning av cimetidin kan medföra en något förhöjd plasmakoncentration av budesonid men detta är inte kliniskt signifikant.
Den hämmande effekten på binjurefunktionen är additiv vid samtidigt intag av systemiska eller intranasala steroider.
Inga interaktioner har observerats mellan budesonid och andra läkemedel som används vid behandling av astma.
Graviditet
De flesta resultaten från prospektiva epidemiologiska studier och data, som inkommit efter godkännande för försäljning i hela världen, har inte kunnat påvisa en ökad risk för biverkningar hos fostret och det nyfödda barnet på grund av användning av inhalerad budesonid under graviditet. Det är viktigt för både fostret och modern och att upprätthålla en adekvat astmabehandling under graviditeten. Liksom för andra läkemedel som administreras under graviditeten ska nyttan av administrering av budesonid under graviditet för modern vägas mot risken för fostret.
Amning
Budesonid passerar över i bröstmjölk. Vid terapeutiska doser av budesonid förväntas dock inga effekter på det ammade barnet. Budesonid kan användas under amning.
Underhållsbehandling med inhalerat budesonid (200 eller 400 mikrogram två gånger dagligen) hos astmatiska ammande kvinnor resulterar i försumbar systemisk exponering av budesonid hos det ammade barnet.
I en farmakokinetisk studie, var barnets beräknade dagliga dos 0,3% av moderns dagliga dos vid båda dosnivåerna. Den genomsnittliga plasmakoncentrationen hos spädbarn uppskattades till en 600-del av koncentrationerna som observerats i moderns plasma, förutsatt fullständig oral biotillgänglighet hos spädbarnet. Koncentrationerna av budesonid i plasmaprover från spädbarnen låg alla under gränsen för kvantifiering.
Baserat på data från inhalerat budesonid, och det faktum att budesonid uppvisar linjära farmakokinetiska egenskaper inom det terapeutiska doseringsintervallet efter nasal, inhalerad, oral och rektal administrering förväntas exponeringen för det ammade barnet vara låg.
Trafik
Budesonide Teva Pharma suspension för nebulisator har ingen eller försumbar effekt på förmågan att framföra fordon och använda maskiner.
Biverkningar
Tecken och symtom på systemiska glukokortikosteroidbiverkningar kan ibland förekomma med inhalerade glukokortiksteroider. Detta beror troligen på dos, exponeringstid, samtidig och tidigare kortiksteroidexponering och individuell känslighet.
Lista över biverkningar
Frekvenserna för biverkningarna definieras enligt följande: mycket vanliga (≥1/10); vanliga (≥1/100, <1/10); mindre vanliga (≥1/1 000, <1/100); sällsynta (≥1/10 000, <1/1 000); mycket sällsynta (<1/10 000), ingen känd frekvens (kan inte beräknas från tillgängliga data).
|
Organsystem |
Frekvens |
Biverkningar |
|---|---|---|
|
Infektioner och infestationer |
Vanliga |
Candidos i munhåla och svalg, pneumoni (hos KOL-patienter) |
|
Immunsystemet |
Sällsynta |
Omedelbara och fördröjda överkänslighetsreaktioner* inklusive utslag, kontakteksem, urtikaria, angioödem och anafylaktiska reaktioner. |
|
Endokrina systemet |
Sällsynta |
Symtom och tecken på systemeffekter av kortikosteroider, inklusive binjurebarksuppression och tillväxthämning** |
|
Psykiska störningar |
Mindre vanliga |
Ångest, depression, sömnstörningar, psykomotorisk hyperaktivitet, aggression |
|
|
Sällsynta |
Rastlöshet, nervositet, beteendestörningar (främst hos barn) |
|
Centrala och perifera nervsystemet |
Mindre vanliga |
Tremor |
|
Ögon |
Mindre vanliga |
Katarakt, dimsyn (se även avsnitt Varningar och försiktighet) |
|
|
Ingen känd frekvens |
Glaukom |
|
Andningsvägar, bröstkorg och mediastinum |
Vanliga |
Hosta, heshet, irritation i halsen |
|
Sällsynta |
Bronkospasm, dysfoni |
|
|
Magtarmkanalen |
Vanliga |
Irritation i munslemhinnan, svårigheter att svälja |
|
Hud och subkutan vävnad |
Sällsynta |
Blåmärken, hudreaktioner, pruritus, erytem |
|
Muskuloskeletala systemet och bindväv |
Mindre vanliga |
Muskelkramp |
|
|
Sällsynta |
Tillväxthämning |
|
Undersökningar |
Mycket sällsynta |
Minskad bentäthet |
* Se Beskrivning av utvalda biverkningar: hudirritation i ansiktet, nedan
** Se Pediatrisk population nedan
Beskrivning av utvalda biverkningar
Hudirritation i ansiktet, som ett exempel på en överkänslighetsreaktion, har inträffat i vissa fall när en nebulisator med en ansiktsmask använts. För att förhindra hudirritationer bör ansiktet tvättas med vatten efter användning av ansiktsmask.
Även i placebokontrollerade studier rapporterades katarakt som mindre vanlig biverkning i placebogruppen.
Kliniska studier med 13 119 patienter som använde inhalerad budesonid och 7 278 patienter som fick placebo har slagits samman. Frekvensen av ångest var 0,52 % för inhalerad budesonid och 0,63 % för placebo. Frekvensen av depression var 0,67 % för inhalerad budesonid och 1,15 % för placebo.
Det finns en ökad risk för lunginflammation hos patienter med nyligen diagnostiserad KOL som påbörjar behandling med inhalerade kortikosteroider. En sammanvägd bedömning av 8 poolade kliniska prövningar med 4643 KOL-patienter som behandlats med budesonid och 3643 patienter som randomiserats till behandling med icke inhalerade kortikosteroider (non-ICS) har dock inte visat en ökad risk för lunginflammation. Resultaten från de första 7 av dessa 8 studier har publicerats som en meta-analys.
Inhalationsbehandling med budesonid kan ge candidainfektion i mun och svalg. Erfarenheter har visat att candidainfektion förekommer mindre ofta om inhalationen utförs före måltid eller om munnen sköljs efter inhalationen. I de flesta fall svarar detta tillstånd på lokalbehandling med svampmedel utan att inhalationsbehandlingen med budesonid behöver avbrytas.
Hosta kan vanligen förebyggas genom inhalation av beta-2-stimulerare (t.ex. terbutalin) 5-10 minuter före administrering av nebuliserad budesonid.
Systemeffekter av inhalationssteroider kan förekomma, särskilt med höga doser och långa behandlingsperioder. Möjliga systemeffekter inkluderar binjuresuppression, tillväxthämning hos barn och ungdomar, minskning av bentätheten, katarakt, glaukom och infektionskänslighet. Förmågan att hantera stress kan vara nedsatt. Beskrivna systemeffekter är emellertid mindre sannolika för inhalerat budesonid än med orala kortikosteroider.
Pediatrisk population
På grund av risken för tillväxthämning hos barn bör tillväxten följas som beskrivs i avsnitt Varningar och försiktighet.
Det finns begränsad tillgänglig data gällande säkerhet och effektivitet för nebuliserad budesonid för överviktiga barn, men viktminskning är viktig parameter som måste beaktas.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till Läkemedelsverket, men alla kan rapportera misstänkta biverkningar till Läkemedelsverket, www.lakemedelsverket.se. Postadress
Läkemedelsverket
Box 26
751 03 Uppsala
Överdosering
Akut överdosering med budesonid, även i mycket höga doser, förväntas inte utgöra något kliniskt problem.
Symptom:
Den enda skadliga effekten efter höga doser spray under en kortare period är nedsatt binjurebarksfunktion. Om det rör sig om kronisk användning med mycket höga doser kan viss binjurebarksatrofi uppträda utöver binjurebarkssuppression.
Behandling:
Akut överdos: Inga behov av akuta åtgärder. Behandlingen med budesonid ska fortsätta med minsta möjliga underhållsdos och binjurebarksfunktionen kommer att återhämta sig automatiskt inom några dagar.
Kronisk överdos: Glukokortikosteroiders systemiska effekter såsom hyperkortisolim och binjuresuppression kan uppkomma hos patienter som använder kroniskt höga doser av budesonid (se avsnitt Varningar och försiktighet). Patienter som använder högre doser än rekommenderat bör övervakas noga och doseringen bör trappas ned. Patienten ska behandlas som beroende av steroider och överföras till lämplig underhållsdos med systemisk steroid, exempelvis prednisolon. När tillståndet är stabilt ska patienten fortsätta inhalationsbehandlingen med budesonid med rekommenderad dos.
Farmakodynamik
Verkningsmekanism
Budesonid är en halogenfri glukokortikosteroid med kraftig lokal antiinflammatorisk effekt och få systemiska effekter. Detta eftersom budesonid snabbt inaktiveras i levern efter absorption (se även avsnitt Farmakokinetik). Den exakta verkningsmekanismen för glukokortikoider vid behandling av astma är inte fullt klarlagd. Antiinflammatoriska effekter (inklusive T-celler, eosinofila celler och mastceller) såsom hämmad frisättning av inflammatoriska mediatorer och hämning av cytokinmedierat immunsvar, är sannolikt betydelsefulla.
Efter en initial dos av inhalerad budesonid via Turbuhaler kan förbättring av lungfunktion förväntas efter ett par timmar. Full terapeutisk effekt uppnås först efter några veckors behandling.
Farmakodynamiska effekter
En klinisk prövning med astmapatienter, hos vilka inhalerad och oralt tillförd budesonid vid doser beräknade att ge likvärdig systemisk biotillgänglighet, visade statistiskt signifikanta effekter för inhalerad, men inte för oralt tillförd, budesonid, jämfört med placebo. Den terapeutiska effekten av normalt använda doser av budesonid för inhalation kan därför huvudsakligen förklaras som en direkt effekt på luftvägarna.
Budesonid har uppvisat en anti-anafylaktisk och anti-inflammatorisk effekt i provokationstest på försöksdjur och patienter. Denna effekt har visat sig som minskad bronkobstruktion under såväl den omedelbara som den sena fasen av den allergiska reaktionen.
Det har också visats att budesonid minskar luftvägarnas histamin- och metakolinreaktivitet hos hyperreaktiva patienter. Behandling med budesonid för inhalation har använts för att effektivt förebygga ansträngningsutlöst astma.
Påverkan på plasmakortisolkoncentration
Studier på friska frivilliga med budesonid har gett en dosrelaterad effekt på plasma- och urinkortisol. Vid rekommenderade doser har budesonid signifikant mindre inverkan på binjurefunktionen än 10 mg prednison, visat med ACTH-testet.
I kliniska prövningar har budesonid visats vara effektiv vid bronkialastma och biverkningar vid underhållsbehandling är oftast milda.
Exacerbationer av KOL
Flera studier med nebuliserat budesonid 4-8 mg/dag har visat effekt vid behandling av KOL-exacerbationer.
I en dubbelblind, randomiserad, placebokontrollerad studie på 199 patienter med akuta exacerbationer av KOL behandlades patienterna med nebuliserat budesonid
8 mg/dag (2 mg fyra gånger dagligen (n=71)) eller 30 mg prednisolon oralt var 12:e timme (n=62) eller placebo (n=66) i tre dagar. Förbättring i FEV1 efter bronkdilaterare jämfört med placebo var 0,10 liter för budesonid och 0,16 liter för prednisolon; skillnaden mellan de aktiva behandlingarna var inte statistiskt signifikant.
Andelen patienter som visade klinisk förbättring i FEV1 på minst 0,15 liter efter bronkdilaterare var större i grupperna som fick nebuliserat budesonid (34 %) och prednisolon (48 %) än i placebogruppen (18 %). Skillnaderna var statistiskt signifikanta för båda aktiva behandlingarna jämfört med placebo (p < 0,05), men inte mellan de aktiva behandlingarna.
Pediatrisk population
Begränsad data från långtidsstudier pekar på att de flesta barn och ungdomar som behandlas med inhalerad budesonid slutligen når förväntad längd som vuxna. En liten, men övergående tillväxt (cirka 1 cm) har dock observerats. Detta sker vanligtvis under de första behandlingsåren (se avsnitt Varningar och försiktighet).
Kliniska studier – astma
Effekten av nebuliserad budesonid har utvärderats i ett stort antal studier och det har visats att budesonid är effektivt för både vuxna och barn som en gång eller två gånger dagligen använder läkemedlet för profylaktisk behandling av kronisk astma.
Kliniska studier – krupp
Ett antal studier av barn med krupp har jämfört nebuliserad budesonid med placebo. Exempel på representativa studier som utvärderar användning av nebuliserad budesonid för behandling av barn med krupp ges nedan.
Effekt hos barn med mild till måttlig krupp
En randomiserad, dubbelblind placebokontrollerad studie på 87 barn (i åldern 7 månader till 9 år), inlagda på sjukhus med krupp som klinisk diagnos, genomfördes för att fastställa om nebuliserad budesonid förbättrar symptomskattning för krupp eller förkortar längden på sjukhusvistelsen. En initial dos av budesonid (2 mg) eller placebo gavs följt av antingen budesonid 1 mg eller placebo gavs var 12:e timme. Budesonid förbättrade statistiskt signifikant symptomskattning vid 12 och 24 timmar samt vid 2 timmar hos patienter med en initial skattning över 3. Sjukhusvistelsens längd reducerades också med 33 %.
Effekt hos barn med måttlig till svår krupp
En randomiserad, dubbelblind, placebokontrollerad studie som jämförde effekten av
nebuliserad budesonid och placebo vid behandling av krupp hos 83 spädbarn och barn (i åldern 6 månader till 8 år) inlagda på sjukhus för krupp. Patienterna fick antingen budesonid 2 mg eller placebo var 12:e timme i högst 36 timmar eller fram tills utskrivning från sjukhuset. Den totala symptomskattningen för krupp bedömdes vid 0, 2, 6, 12, 24, 36 och 48 timmar efter första dosen. Vid 2 timmar, visade både budesonid- och placebo-gruppen en liknande förbättring av symtomskattningen, utan statistiskt signifikant skillnad mellan grupperna. Vid sex timmar, var symtomskattningen i budesonid-gruppen statistiskt signifikant bättre jämfört med placebogruppen, och denna förbättring jämfört med placebo var också tydlig vid 12 och 24 timmar.
Farmakokinetik
Absorption
Hos vuxna är den systemiska biotillgängligheten för budesonid efter administrering av nebuliserad budesonid via jetnebulisator ungefär 15 % av den nominella dosen och 40–70 % av den dos som tillförts patienten. Endast en liten del av den systemiskt tillgängliga dosen kommer från nedsvald suspension för inhalation. Den maximala plasmakoncentrationen efter administrering av en engångsdos på 2 mg uppnås 10–30 minuter efter påbörjad inhalation, och är ungefär 4 nmol/l.
Distribution
Distributionsvolymen för budesonid hos vuxna är cirka 3,0 l/kg. Plasmaproteinbindningen är ungefär 85–90 %.
Metabolism
Budesonid genomgår en omfattande (ungefär 90 %) första-passage-metabolism i levern via CYP 3A4 till metaboliter med låg glukokortikosteroid aktivitet. Glukokortikosteroidaktiviteten för huvudmetaboliterna, 6-beta-hydroxibudesonid och 16-alfa-hydroxiprednisolon, är mindre än 1% av den för budesonid.
Eliminering
Metaboliterna utsöndras i oförändrad eller konjugerad form, huvudsakligen via njurarna. Ingen oförändrad budesonid återfinns i urinen. Budesonid har hög systemisk clearance (cirka 1,2 liter/min) hos friska vuxna, och halveringstiden i eliminationsfasen efter intravenös administrering är ungefär 2-3 timmar.
Linjäritet
I kliniskt relevanta doser är farmakokinetiken för budesonid dosproportionerlig.
Pediatrisk population
Budesonid har en systemisk clearance på omkring 0,5 l/min hos barn i åldern 4-6 år med astma. Barn har ungefär 50 % högre clearance per kg kroppsvikt än vuxna. Halveringstiden för budesonid efter inhalation är omkring 2,3 timmar hos barn med astma, vilket är ungefär densamma som hos friska vuxna. Hos barn i åldern 4–6 år med astma är den systemiska biotillgängligheten för budesonid efter administrering av nebuliserad budesonid via jetnebulisator (Pari LC Jet Plus® med Pari Master®-kompressor) ungefär 6 % av den nominella dosen och 26 % av den dos som administrerats till patienten. Den systemiska biotillgängligheten hos barn är ungefär hälften jämfört med den i vuxna.
Den maximala plasmakoncentrationen efter administrering av en engångsdos på 1 mg budesonid uppnås ungefär 20 minuter efter påbörjad inhalation, och är ungefär 2,4 nmol/l hos barn mellan 4 och 6 år med astma.
Exponeringen (Cmax och AUC) av budesonid efter administrering av en engångsdos om 1 mg som ges via nebulisator till barn mellan 4-6 år är jämförbar med den för vuxna som ges samma avgivna dos i samma nebuliseringssystem.
Prekliniska uppgifter
Den akuta toxiciteten av budesonid är låg och i samma storleksordning som för andra glukokortikosteroider.
Gängse studier avseende subakut toxicitet, kronisk toxicitet, genotoxicitet och karcinogenicitet visade inte några särskilda risker för människa i det terapeutiska dosområdet.
En ökad incidens av gliom hos hanråttor har observerats i en studie, men detta kunde inte bekräftas i en upprepad studie. Tillgängliga kliniska data visar inte på att budesonid inducerar hjärntumörer eller andra primära neoplasmer hos människa.
Glukokortikosteroider, inklusive budesonid har orsakat fosterskador hos djur inklusive gomspalt och skelettmissbildningar. Liknande skador bedöms osannolika hos människa vid rekommenderade dosnivåer.
Djurstudier har också visat att prenatal överexponering för glukokortikosteroider kan ha ett samband med ökad risk för intrauterin tillväxthämning, kardiovaskulär sjukdom hos vuxna och permanenta förändringar i glukokortikosteroidreceptortäthet, neurotransmittoromsättning samt beteende, vid exponering understigande det teratogena dosintervallet.
Innehåll
Kvalitativ och kvantitativ sammansättning
Budesonide Teva Pharma 0,125 mg/ml suspension för nebulisator:
Varje endosbehållare med 2 ml suspension innehåller 0,25 mg budesonid.
Budesonide Teva Pharma 0,25 mg/ml suspension för nebulisator:
Varje endosbehållare med 2 ml suspension innehåller 0,5 mg budesonid.
Budesonide Teva Pharma 0,5 mg/ml suspension för nebulisator:
Varje endosbehållare med 2 ml suspension innehåller 1 mg budesonid.
Förteckning över hjälpämnen
Dinatriumedetat
Natriumklorid
Polysorbat 80 (E433)
Citronsyramonohydrat (E330)
Natriumcitrat (E331)
Vatten för injektionsvätskor
Blandbarhet
Detta läkemedel får inte blandas med andra läkemedel förutom de som nämns i avsnitt Hållbarhet, förvaring och hantering.
Hållbarhet, förvaring och hantering
Hållbarhet
Oöppnad: 2 år
Efter att folieförpackningen har öppnats är hållbarheten 3 månader.
Öppnad endosbehållare: används omedelbart. Kasta eventuellt överblivet innehåll.
Särskilda förvaringsanvisningar
Får ej frysas.
Förvaras stående. Förvara endosbehållaren i den öppnade folieförpackningen. Den öppnade folieförpackningen ska förvaras i ytterkartongen för skydd mot ljus. För hållbarhet för den öppnade folieförpackningen se Hållbarhet ovan.
Särskilda anvisningar för destruktion
Budesonide Teva Pharma suspension för nebulisator kan blandas med 0,9% natriumkloridlösning och med lösningar innehållande terbutalin, salbutamol, natriumkromoglikat eller ipratropiumbromid. Blandningen bör användas inom 30 minuter.
Varje ampull är endast för engångsbruk. Oanvänd suspension ska kasseras.
Produkten är steril till öppnandet.
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.




