Indikationer
Actiq används för behandling av genombrottssmärta hos patienter som redan behandlas med opioider som underhållsbehandling vid långvarig cancersmärta. Genombrottssmärta är ett övergående smärtskov som uppträder utöver en i övrigt kontrollerad långvarig smärta.
Patienter som får underhållsbehandling med opioider definieras här som de som dagligen tar minst 60 mg oralt morfin, minst 25 mikrogram transdermalt fentanyl per timme, minst 30 mg oxikodon per dag, minst 8 mg oralt hydromorfon per dag eller motsvarande analgetisk dos av en annan opioid under en vecka eller längre.
Kontraindikationer
-
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt Innehåll.
-
Patienter utan underhållsbehandling med opioider eftersom det medför en ökad risk för andningsdepression.
-
Behandling av akut smärta annan än genombrottssmärta.
-
Samtidig användning av monoaminooxidashämmare (MAO-hämmare), eller användning inom 2 veckor efter avslutad behandling med MAO-hämmare (se avsnitt Varningar och försiktighet och Interaktioner).
-
Patienter som behandlas med läkemedel som innehåller natriumoxibat.
-
Svår andningsdepression eller svår obstruktiv lungsjukdom.
Dosering
Dosering
För att minimera riskerna för opioidrelaterade biverkningar och för att identifiera optimal dos är det absolut nödvändigt att vårdpersonalen övervakar patienten noggrant under titreringsprocessen.
Actiq är inte utbytbart på mikrogram-mikrogram basis med andra kortverkande fentanylläkemedel indicerade för genombrottssmärta vid cancer, eftersom den farmakokinetiska profilen och/eller doseringsschemat för dessa produkter är helt olika.
Patienten måste instrueras om att inte samtidigt använda mer än ett kortverkande fentanylläkemedel för behandling av genombrottssmärta orsakad av cancer, och att alla andra fentanylläkemedel som skrivits ut för behandling av genombrottssmärta skall kasseras när patienten byter till Actiq. För att förhindra förväxling och eventuell överdosering bör patientens tillgång till olika styrkor av Actiq minimeras.
Eventuella oanvända Actiq–enheter som patienten inte längre behöver skall kasseras på lämpligt sätt. Patienten måste påminnas om att Actiq skall förvaras oåtkomligt för barn.
Vuxna
Dostitrering och underhållsterapi
Actiq skall titreras individuellt till optimal dos som ger adekvat analgesi och minimerar biverkningarna. I kliniska prövningar gick det inte att förutsäga optimal Actiq–dos för genombrottssmärta med utgångspunkt från den dagliga underhållsdosen av opioidanalgetika.
a) Titrering
Patientens bakomliggande långvariga smärta skall vara kontrollerad med hjälp av opioidterapi så att patienten normalt inte upplever mer än 4 episoder av genombrottssmärta per dag innan titreringen av Actiq inleds.
Initialdosen för Actiq är 200 mikrogram, och dosen titreras sedan uppåt efter behov med de tillgängliga styrkorna (200, 400, 600, 800, 1200 och 1600 mikrogram). Patienten skall övervakas noggrant tills en dos som ger adekvat analgesi med acceptabla biverkningar uppnås med användning av en dosenhet per episod av genombrottssmärta. Denna dos definieras som optimal dos.
Om man under titreringen inte uppnår adekvat analgesi inom 30 minuter efter påbörjan av den första enheten (dvs.15 minuter efter det att patienten har förbrukat en hel Actiq-enhet), kan en andra Actiq-enhet med samma styrka användas. Högst två Actiq-enheter skall användas vid behandling av en smärtepisod. Vid dosen 1600 mikrogram, förväntas en andra dos krävas endast hos en minoritet av patienterna.
Om mer än en enhet per episod krävs för behandling av på varandra följande episoder av genombrottssmärta, skall höjning av dosen till nästa tillgängliga högre styrka övervägas.
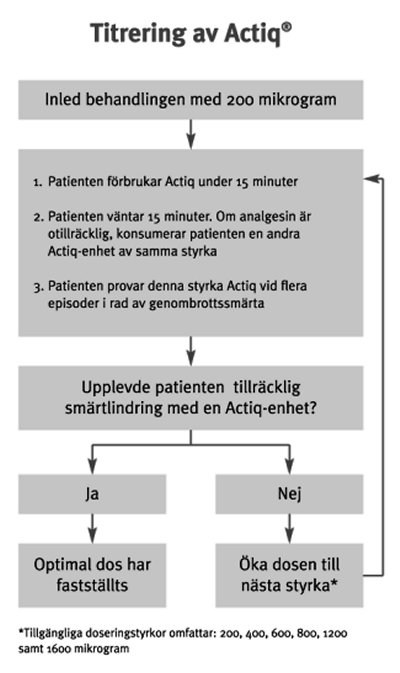
b) Underhållsbehandling
När optimal dos har fastställts (dvs. den dos som innebär att en episod i allmänhet behandlas effektivt med en enhet), skall patienten hållas på denna dos och förbrukningen begränsas till högst fyra Actiq–enheter per dag.
Patienterna skall övervakas av vårdpersonal för att se till att den maximala förbrukningen på fyra Actiq–enheter per dag inte överskrids.
Dosjustering
Dosen vid underhållsbehandlingen med Actiq bör ökas om patienten behöver mer än en dos per episod av genombrottssmärta under flera på varandra följande episoder av genombrottssmärta. Vid dosjustering gäller samma principer som beskrivits ovan för titrering.
Om patienten upplever mer än fyra episoder av genombrottssmärta per dag bör doseringen av den långtidsverkande opioiden som används för långvarig smärta omprövas. Om doseringen av den långtidsverkande opioiden för långvarig smärta ökas kan det bli nödvändigt att ompröva vilken styrka av Actiq som behövs för att behandla patientens genombrottssmärta.
Om adekvat smärtkontroll inte uppnås ska risken för hyperalgesi, tolerans och progression av den underliggande sjukdomen övervägas (se avsnitt Varningar och försiktighet).
Det är absolut nödvändigt att vårdpersonal övervakar varje omtitrering av dosen av analgetika.
Behandlingslängd och behandlingsmål
Innan behandling med Actiq inleds ska en behandlingsstrategi som omfattar behandlingslängd, behandlingsmål samt en plan för avslutande av behandlingen fastställas i samråd med patienten och i enlighet med riktlinjerna för smärtbehandling. Under behandlingen ska läkare och patient ha frekvent kontakt för bedömning av behovet av fortsatt behandling, övervägande av utsättning och för att dosjustera vid behov. Om tillräcklig smärtkontroll inte uppnås ska eventuell hyperalgesi, tolerans och progression av underliggande sjukdom övervägas (se avsnitt Varningar och försiktighet). Actiq ska inte användas under längre tid än vad som är nödvändigt.
Utsättande av terapi
Actiq skall sättas ut omedelbart om patienten inte längre upplever episoder av genombrottssmärta. Behandlingen för den långvariga bakgrundssmärtan skall fortsättas enligt ordinationen. Om det är nödvändigt att sätta ut all opioidbehandling, måste patienten följas noga av läkaren då en gradvis nedåttitrering av opioiderna är nödvändig för att undvika risken för plötsliga abstinenssymptom.
Användning hos äldre patienter
Äldre patienter har visat sig vara känsligare för effekterna av intravenöst administrerat fentanyl. Dosen måste därför titreras särskilt noggrant hos dessa patienter. Hos äldre är eliminationen av fentanyl långsammare och den terminala halveringstiden i eliminationsfasen är förlängd, vilket kan ge ackumulering av den aktiva substansen och ökad risk för biverkningar.
Formella kliniska prövningar med Actiq har inte gjorts på äldre patienter. Man har dock observerat i kliniska prövningar att patienter över 65 år behöver lägre doser av Actiq för framgångsrik lindring av genombrottssmärta.
Användning hos patienter med nedsatt njur- eller leverfunktion
Särskild försiktighet skall iakttas under titreringsprocessen hos patienter med nedsatt njur- eller leverfunktion (se avsnitt Varningar och försiktighet).
Pediatrisk population
Ungdomar 16 år och uppåt:
Följ dosen för vuxna.
Barn och ungdomar under 16 år:
Säkerhet och effekt för barnoch ungdomar under 16 år har inte fastställts. Det finns begränsad klinisk erfarenhet från användning av Actiq hos barn som redan står på underhållsbehandling med opioider (se avsnitt Farmakodynamik och Farmakokinetik). Användning i denna patientpopulation rekommenderas därför inte.
Administreringssätt
Actiq är avsett för användning i munhålan och skall därför placeras i munnen mot kinden och sedan med hjälp av applikatorn föras runt i munnen för att maximera slemhinneexponeringen för läkemedlet. Patienten skall ”suga” på Actiq-enheten, inte tugga den, eftersom absorptionen av fentanyl via kindens slemhinna sker snabbt jämfört med systemisk absorption via mag-tarmkanalen. Patienter med muntorrhet kan använda vatten för att fukta munslemhinnan.
Actiq-enheten skall förbrukas under 15 minuter. Vid tecken på kraftiga opioida effekter innan dess att Actiq-enheten är förbrukad ska den omedelbart tas ut ur munnen och en sänkning av dosen bör övervägas vid fortsatt behandling.
Varningar och försiktighet
På grund av de risker, däribland dödsfall, som är förknippade med oavsiktlig exponering, felaktig användning och missbruk, måste patienter och deras vårdgivare uppmanas att förvara Actiq på ett säkert ställe, som inte är tillgängligt för andra.
Oavsiktligt intag hos barn
Patienterna och deras vårdare måste upplysas om att Actiq innehåller en aktiv substans i en mängd som kan vara livshotande för barn. Dödsfall har rapporterats hos barn som oavsiktligt har fått i sig Actiq. Patienter och deras vårdare måste instrueras om att de skall förvara alla sugtabletter utom syn- och räckhåll för barn och att öppnade och oöppnade enheter skall kasseras enligt gällande anvisningar. För varje patient som behandlas utanför sjukhus bör en bedömning göras angående risken för att barn exponeras av misstag.
Underhållsbehandling med opioider
Läkemedlet får inte ges till patienter som inte behandlas med opioider som underhållsbehandling eftersom det finns en ökad risk för andningsdepression och död. Det är viktigt att underhållsbehandlingen med opioiden som används för behandling av patientens långvariga smärta är stabiliserad innan behandling med Actiq inleds och att patienten fortsätter med sin underhållsbehandling med opioiden under behandlingen med Actiq.
Tolerans och opioidberoende (missbruk och beroende)
Tolerans, fysiskt beroende och psykologiskt beroende kan uppstå vid upprepad administrering av opioider. Fentanyl kan missbrukas på ett sätt som liknar det för andra opioider och alla patienter som behandlas med opioder måste övervakas för tecken på missbruk och beroende. Patienter som löper ökad risk för opioidmissbruk kan fortfarande få lämplig behandling med opioider, men dessa patienter kommer att kräva ytterligare övervakning för tecken på felanvändning, missbruk eller beroende.
Upprepad användning av Actiq kan leda till opioidberoende. Högre dos och längre behandlingstid med opioider kan öka risken för att utveckla opioidberoende. Missbruk eller avsiktlig felanvändning av Actiq kan resultera i överdos och/eller dödsfall. Risken för att utveckla opioidberoende är förhöjd hos patienter med en personlig anamnes eller en familjeanamnes (föräldrar eller syskon) på drogberoende (inklusive alkoholberoende), hos patienter som använder tobak eller hos patienter med andra psykiska sjukdomar i anamnesen (t.ex. egentlig depression, ångest och personlighetsstörning).
Innan behandling med Actiq inleds och under behandlingen ska behandlingsmål och utsättningsplan fastställas i samråd med patienten (se avsnitt Dosering). Före och under behandlingen ska patienten också informeras om riskerna för och tecknen på opioidberoende. Patienterna ska uppmanas att kontakta läkare om sådana tecken skulle uppträda.
Patienterna ska övervakas för tecken på drogsökande beteende (t.ex. för tidiga önskemål om påfyllning). Detta inkluderar en genomgång av opioider och psykoaktiva läkemedel (såsom bensodiazepiner) som används samtidigt. Hos patienter med tecken och symtom på opioidberoende ska konsultation med en beroendespecialist övervägas.
Läkemedelsberoende och risk för missbruk
Tolerans, fysiskt beroende och psykologiskt beroende kan uppstå vid upprepad administrering av opioider. Iatrogent beroende efter opioidadministrering kan uppkomma. Fentanyl kan missbrukas på ett sätt som liknar det för andra opioider och alla patienter som behandlas med opioder måste övervakas för tecken på missbruk och beroende. Patienter som löper ökad risk för opioidmissbruk kan fortfarande få lämplig behandling med opioider, men dessa patienter kommer att kräva ytterligare övervakning för tecken på felanvändning, missbruk eller beroende.
Upprepad användning av Actiq kan leda till opioidberoende. Missbruk eller avsiktlig felanvändning av Actiq kan resultera i överdos och/eller dödsfall. Risken för att utveckla opioidberoende är förhöjd hos patienter med en personlig anamnes eller en familjeanamnes (föräldrar eller syskon) på drogberoende (inklusive alkoholberoende), hos patienter som använder tobak eller hos patienter med andra psykiska sjukdomar i anamnesen (t.ex. egentlig depression, ångest och personlighetsstörning).
Patienterna ska övervakas för tecken på drogsökande beteende (t.ex. för tidiga önskemål om påfyllning). Detta inkluderar en genomgång av opioider och psykoaktiva läkemedel (såsom bensodiazepiner) som används samtidigt. Hos patienter med tecken och symtom på opioidberoende ska konsultation med en beroendespecialist övervägas.
Hyperalgesi
Liksom med andra opioider ska risken för opioidinducerad hyperalgesi övervägas om patienten inte uppnår tillräcklig smärtkontroll trots ökad dos fentanyl. I sådana fall kan en sänkning av fentanyldosen eller utsättning av fentanylbehandlingen vara indicerad.
Endokrina effekter
Opioider kan påverka hypotalamus‑hypofys‑binjure- eller hypotalamus‑hypofys‑gonad‑axeln. Exempel på förändringar som har observerats är en ökning av prolaktin i serum och en minskad halt kortisol och testosteron i plasma. Kliniska symtom kan uppträda på grund av dessa hormonförändringar.
Fall av binjuresvikt har rapporterats vid opioidanvändning, inklusive användning av sugtabletter med fentanyl. Dessa fall var vanligare efter användning längre än en månad. Patienter ska avvänjas från opioiden för att låta binjurefunktionen återhämta sig och fortsätta med kortikosteroidanvändning tills binjurefunktionen återhämtat sig (se avsnitt Biverkningar).
Andningsdepression
Liksom för alla opioider är användning av Actiq förenad med en risk för kliniskt signifikant andningsdepression. Patienterna ska övervakas med detta i åtanke.
Särskild försiktighet skall iakttas vid titrering av Actiq hos patienter med icke allvarlig kronisk obstruktiv lungsjukdom eller annat medicinskt tillstånd som ökar risken för andningsdepression, eftersom även normala terapeutiska doser av Actiq kan sätta ned andningsreflexen till den grad att andningsstillestånd inträder.
Sömnrelaterade andningsstörningar
Opioider kan orsaka sömnrelaterade andningsstörningar såsom central sömnapné och sömnrelaterad hypoxemi. Risken för central sömnapné ökar med dosen. Överväg att minska den totala dosen opioider till patienter med central sömnapné.
Alkohol
Samtidig användning av alkohol och fentanyl kan ge ökad dämpande effekt vilket kan resultera i dödlig utgång (se avsnitt Interaktioner).
Risker vid samtidig administrering med bensodiazepiner eller relaterade läkemedel
Samtidig användning av opioider, inklusive Actiq, med bensodiazepiner eller relaterade läkemedel kan leda till djup sedering, andningsdepression, koma och dödsfall. På grund av dessa risker ska samtidig förskrivning av opioider och bensodiazepiner eller relaterade läkemedel bara ske till patienter för vilka alternativa behandlingsalternativ är otillräckliga.
Om ett beslut fattas att förskriva Actiq samtidigt med bensodiazepiner eller relaterade läkemedel ska lägsta effektiva dos under kortast möjliga samtidiga användning väljas. Patienter ska övervakas noggrant för tecken och symtom på andningsdepression och sedering (se avsnitt Interaktioner).
Intrakraniella effekter av koldioxidretention, nedsatt medvetandegrad och skallskada
Actiq skall ges med extrem försiktighet till patienter som kan vara särskilt känsliga för intrakraniella effekter av CO2-retention, till exempel patienter med tecken på ökat intrakraniellt tryck eller nedsatt medvetandegrad. Opioider kan maskera det kliniska förloppet hos en patient med skallskada och skall endast användas när det är kliniskt motiverat.
Bradyarytmier
Fentanyl kan ge upphov till bradykardi. Fentanyl bör användas med försiktighet till patienter med tidigare eller befintliga bradyarytmier.
Nedsatt lever- eller njurfunktion
Actiq skall dessutom ges med försiktighet till patienter med nedsatt lever- eller njurfunktion. Påverkan på läkemedlets farmakokinetik vid nedsatt lever- eller njurfunktion har inte studerats, men när det ges intravenöst har det visats att clearance för fentanyl är förändrat vid lever- och njursjukdom på grund av förändringar i metaboliskt clearance och plasmaproteiner. Efter administrering av Actiq kan nedsatt lever- och njurfunktion både öka biotillgängligheten hos fentanyl som svalts och minska systemiskt clearance, vilket kan leda till förstärkta och förlängda opioideffekter. Därför skall särskild försiktighet iakttas under titreringsprocessen hos patienter med måttligt svår eller allvarlig lever- eller njursjukdom.
Hypovolemi och hypotension
Speciell försiktighet bör iakttas hos patienter med hypovolemi och hypotension.
Karies
Normal munhygien rekommenderas för att minska potentiella skador på tänderna. Eftersom Actiq innehåller cirka 2 gram socker kan frekvent användning öka risken för karies. Muntorrhet som har samband med användning av opioidläkemedel kan bidra till att öka risken. Regelbundna tandläkarbesök rekommenderas under behandlingen med Actiq.
Serotonergt syndrom
Försiktighet bör iakttas när Actiq administreras samtidigt med läkemedel som påverkar det serotonerga signalsubstanssystemet.
Ett eventuellt livshotande serotonergt syndrom kan uppkomma vid samtidig användning av serotonerga läkemedel som selektiva serotoninåterupptagshämmare (SSRI) och selektiva serotonin noradrenalinåterupptagshämmare (SNRI), och med läkemedel som påverkar metabolismen av serotonin (t.ex.monoaminoxidashämmare [MAO hämmare]) (se avsnitt Kontraindikationer). Detta kan uppkomma med den rekommenderade dosen.
Serotonergt syndrom kan omfatta förändringar av mental status (t.ex. agitation, hallucinationer, koma), autonom instabilitet (t.ex. takykardi, instabilt blodtryck, hypertermi), neuromuskulära avvikelser (t.ex. hyperreflexi, inkoordination, stelhet) och/eller gastrointestinala symtom (t.ex. illamående, kräkningar, diarré).
Vid misstanke om serotonergt syndrom ska behandlingen med Actiq sättas ut.
Anafylaxi och överkänslighet
Anafylaxi och överkänslighet har rapporterats i samband med användning av orala transmukosala fentanylprodukter (se avsnitt Biverkningar).
Pediatrisk population
Actiq rekommenderas inte för användning hos barn och ungdomar under 16 år på grund av brist på data avseende säkerhet och effekt (se avsnitt Farmakodynamik och Farmakokinetik).
Hjälpämnen
Glukos
Innehåller ca 1,89 g glukos per dos. Detta bör beaktas av patienter med diabetes mellitus.
Patienter med följande sällsynta tillstånd bör inte ta detta läkemedel: glukosgalaktosmalabsorption.
Kan vara skadligt för tänderna.
Sackaros
Patienter med något av följande sällsynta, ärftliga tillstånd bör inte använda detta läkemedel: fruktosintolerans, glukosgalaktosmalabsorption eller sukras-isomaltas-brist.
Kan vara skadligt för tänderna.
Natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per sugtablett, d.v.s. är näst intill “natriumfritt”.
Interaktioner
Substanser som påverkar CYP3A4-aktivitet
CYP3A4-hämmare
Fentanyl metaboliseras av isoenzymet CYP3A4 i levern och tarmslemhinnan. Potenta hämmare av CYP3A4 såsom makrolidantibiotika, (t. ex erytromycin), antimykotika av azoltyp (t. ex. ketokonazol, itrakonazol och flukonazol) och vissa proteashämmare (t. ex ritonavir), kan öka biotillgängligheten hos svalt fentanyl och kan även minska systemiskt clearance, vilket kan leda till förstärkta eller förlängda opioideffekter. Liknande effekter kan ses efter samtidigt intag av grapefruktjuice, som man vet hämmar cytokrom CYP3A4. Därför rekommenderas försiktighet när fentanyl ges tillsammans med CYP3A4–hämmare.
CYP3A4-inducerare
Samtidig användning av medel som inducerar 3A4-aktivitet kan minska effekten av Actiq.
Substanser som kan öka CNS-dämpande effekter
Samtidigt administrering med fentanyl och andra CNS-dämpande läkemedel, inklusive andra opioider, sedativa eller hypnotika, (inklusive bensodiazepiner), allmänanestetika, fentiaziner, lugnande medel, muskelrelaxantia, sederande antihistaminer, gabapentinoider (gabapentin och pregabalin) och alkohol kan ge additiv dämpande effekt vilket kan resultera i andningsdepression, hypotoni, djup sedering, koma eller dödlig dödlig utgång (se avsnitt Varningar och försiktighet).
Sedativa läkemedel såsom bensodiazepiner eller relaterade läkemedel
Samtidig användning av opioider med sedativa läkemedel såsom bensodiazepiner eller relaterade läkemedel ökar risken för sedering, andningsdepression, koma och dödsfall på grund av additiv CNS‑depressiv effekt. Dosen och varaktigheten av samtidig användning ska begränsas (se avsnitt Varningar och försiktighet).
Partiella opioidagonister/-antagonister
Samtidig användning av partiella opioidagonister/opioidantagonister (t.ex. buprenorfin, nalbufin, pentazocin) rekommenderas inte. Dessa har hög affinitet till opioidreceptorer med relativt låg egen aktivitet och motverkar därför delvis fentanyls analgetiska effekt och kan inducera abstinenssymtom hos opioidberoende patienter.
Serotonerga preparat
Samtidig administrering av fentanyl med ett serotonergt preparat t.ex.en selektiv serotoninåterupptagshämmare (SSRI), en selektiv serotonin - noradrenalinåterupptagshämmare (SNRI) eller en monoaminoxidashämmare (MAO-hämmare), kan öka risken för serotonergt syndrom, ett potentiellt livshotande tillstånd.
Natriumoxabat
Samtidig användning av läkemedel som innehåller natriumoxibat och fentanyl är kontraindicerad (se avsnitt Kontraindikationer). Behandling med natriumoxabat ska avslutas innan behandling med Actiq påbörjas.
Graviditet
Det finns inga eller begränsade data från behandling av gravida kvinnor med fentanyl. Djurstudier har visat reproduktionstoxikologiska effekter (se avsnitt Prekliniska uppgifter). Opioidanalgetika kan ge neonatal andningsdepression. Vid långtidsbruk av fentalyl under graviditet finns det risk för opiodrelaterad abstinenssyndrom hos det nyfödda barnet, vilket kan vara livshotande om det inte upptäcks och behandlas och vilket kräver behandling enligt protokoll utvecklade av experter inom neonatalogi. Actiq skall användas under graviditet endast då det är absolut nödvändigt. Vid långvarig opiodanvändning under graviditet ska patienten informeras om risken för opiodrelaterat abstinenssyndrom hos det nyfödda barnet och tillgång till lämplig behandling säkerställas (se avsnitt Biverkningar).
Användning av fentanyl under förlossning (inklusive kejsarsnitt) avrådes eftersom fentanyl passerar över placenta och kan orsaka andningsdepression hos fostret.. Placentaövergångskvoten är 0,44 (foster/moder-kvot 1,00/2,27).
Amning
Fentanyl passerar över i bröstmjölk och kan orsaka sedering och andningsdepression hos det ammade barnet. Fentanyl ska inte användas av ammande kvinnor och amning bör inte återupptas tidigast 5 dagar efter den sista administreringen av fentanyl.
Fertilitet
Det finns inga data tillgängliga avseende fertilitet hos människa. I djurstudier försämrades fertilitet hos handjur (se avsnitt Prekliniska uppgifter).
Trafik
Inga studier av effekterna hos Actiq på förmågan att framföra fordon och använda maskiner har utförts. Opioidanalgetika kan dock sätta ned den mentala och/eller fysiska förmåga som krävs för att utföra potentiellt farliga uppgifter (t ex köra bil eller använda maskiner). Patienter ska rekommenderas att inte köra bil eller använda maskiner om de upplever dåsighet, yrsel, dimsyn eller dubbelseende när de använder Actiq.
Biverkningar
Typiska opioida biverkningar kan förväntas vid Actiq–behandling. Ofta upphör eller avtar intensiteten av dessa vid fortsatt användning av produkten när patienten har titrerats till lämplig dos. De allvarligaste biverkningarna är emellertid andningsdepression (som kan leda till apné eller andningsstillestånd), kardiovaskulär påverkan, hypotension och chock. Alla patienter bör följas med avseende på dessa symtom.
Reaktioner vid appliceringsstället, såsom tandköttsblödning, irritation, smärta och sår har rapporterats efter användning.
Eftersom de kliniska prövningarna av Actiq var utformade för att utvärdera säkerhet och effekt vid behandling av genombrottssmärta, tog alla patienter samtidigt också opioider, såsom morfin i depot–beredning eller transdermalt fentanyl, för långvarig smärta. Det är därför inte möjligt att definitivt skilja ut effekterna av enbart Actiq.
Följande biverkningar har rapporterats med Actiq och/eller andra föreningar som innehåller fentanyl under kliniska studier och efter godkännandet för försäljning. Biverkningarna presenteras nedan indelade efter organsystem och frekvens i enlighet med MedDRA terminologin (frekvenserna definieras som: mycket vanliga (≥1/10), vanliga (≥1/100, <1/10), mindre vanliga (≥1/1 000, <1/100), ingen känd frekvens (kan inte beräknas från tillgängliga data):
|
MedDRA organklass |
Mycket vanliga |
Vanliga |
Mindre vanliga |
Ingen känd frekvens |
|
Immunsystemet |
|
|
|
Anafylaktisk reaktion, tungödem, läppödem |
|
Metabolism och nutrition |
|
anorexi |
|
|
|
Endokrina systemet |
|
|
|
Binjuresvikt Androgenbrist |
|
Psykiska störningar |
|
Förvirrings-tillstånd ångest, hallucinationer, depression, emotionell labilitet |
onormala drömmar, depersonal-isation, onormala tankar, eufori |
Hyposomni läkemedelsberoende, läkemedelsmissbruk (se avsnitt Varningar och försiktighet), delirium |
|
Centrala och perifera nervsystemet |
somnolens, yrsel, huvudvärk |
medvetandeförlust, konvulsion, vertigo, myoklonus, sedation, parestesi (inklusive hyperestesi/cirkum-oral parestesi), gångrubbning/dålig koordination, smakförändring |
koma sluddrigt tal |
|
|
Ögon |
|
synförändringar (dimsyn, dubbelseende) |
|
|
|
Blodkärl |
|
|
vasodilatation |
rodnad, värmevallningar |
|
Andningsvägar, bröstkorg och mediastinum |
dyspné |
|
|
faryngealt ödem, andnings-depression, sömnapnésyndrom |
|
Magtarmkanalen |
illamående, kräkningar, förstopp-ning, buksmärta |
muntorrhet, dyspepsi, stomatit, tungbesvär (t.ex. brännande känsla, sår), flatulens, uppsvälld mage |
ileus, orala sår karies, tandkötts-blödning |
tandlossning, tandköttsfickor, tandkötts-inflammation, diarré |
|
Hud och subkutan vävnad |
|
pruritus, svettning, utslag |
urtikaria |
|
|
Njurar och urinvägar |
|
urinretention |
|
|
|
Allmänna symtom och/eller symtom vid administreringsstället |
asteni |
reaktioner vid appliceringsstället inklusive irritation, smärta och sår sjukdomskänsla |
|
trötthet, perifert ödem, pyrexi abstinens-syndrom*, abstinenssyndromhos nyfödda (se avsnitt Graviditet), läkemedelstolerans, blödning på appliceringsstället |
|
Undersökningar |
|
viktminskning |
|
|
|
Skador och förgiftningar och behandlings komplikationer |
|
olycksfall (t.ex. fall) |
|
|
*Symtom på opiatabstinens såsom illamående, kräkning, diarré, ångest, frossa, tremor och svettning har setts vid transmukosalt fentanyl.
Beskrivning av utvalda biverkningar
Tolerans
Tolerans kan utvecklas vid upprepad användning.
Läkemedelsberoende
Upprepad användning av Actiq kan leda till läkemedelsberoende, även vid terapeutiska doser. Risken för läkemedelsberoende kan variera beroende på en patients individuella riskfaktorer, dosering och opioidbehandlingens längd (se avsnitt Varningar och försiktighet).
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till Läkemedelsverket, men alla kan rapportera misstänkta biverkningar till Läkemedelsverket, www.lakemedelsverket.se. Postadress
Läkemedelsverket
Box 26
751 03 Uppsala
Överdosering
Symtom
Symtomen på överdosering av fentanyl förväntas likna de symtom som uppträder vid överdosering av intravenöst fentanyl och andra opioider. Dessa symtom kan härledas till de farmakologiska effekterna hos fentanyl, av vilka förändrat sinnestillstånd, medvetslöshet, koma, hjärtstillestånd, andningsdepression, andnöd, och andningssvikt är de allvarligaste signifikanta effekterna vilka i vissa fall har orsakat dödsfall.
Fall av Cheynes-Stokes andning har observerats vid överdosering av fentanyl, särskilt hos patienter med hjärtsvikt i anamnesen.
Toxisk leukoencefalopati har också observerats vid överdosering av fentanyl.
Behandling
Vid överdosering av en opioid vidtas följande åtgärder: Ta med hjälp av applikatorn omedelbart ut Actiq-enheten ur patientens mun, om den fortfarande är kvar där. Kontrollera att patientens luftvägar är öppna, stimulera patienten fysiskt och verbalt, bedöm medvetandegraden, liksom ventilations- och cirkulationsstatus, och sätt vid behov in assisterad ventilation (ventilationsstöd).
Överdosering (oavsiktligt intag) hos opiodnaiva personer
Vid behandling av överdos (oavsiktligt intag) hos en person som inte tidigare behandlats med någon opioid anläggs en intravenös kanyl för administrering av naloxon eller annan opioidantagonist efter kliniskt behov. Efter en överdos kan andningsdepressionens duration vara längre än effekterna av opioidantagonistens verkan (naloxons halveringstid varierar t.ex. mellan 30 och 81 minuter) och det kan därför bli nödvändigt med upprepad administrering. Läs produktresumén för den aktuella opioidantagonisten för närmare upplysningar.
Överdosering hos patienter på underhållsbehandling med opioider
Vid behandling av överdosering hos en patient som underhålls med opioider anläggs en intravenös kanyl. I vissa fall kan det vara motiverat med en användning av naloxon eller annan opioidantagonist, men sådan administrering är förenad med risk för akut abstinenssyndrom.
Trots att muskelrigiditet som påverkar andningen inte har iakttagits efter användning av Actiq, kan det förekomma i samband med behandling med fentanyl och andra opioider. Sådana tillstånd behandlas med assisterad ventilation, en opioidantagonist, eller, som sista alternativ, ett neuromuskulärt blockerande medel.
Farmakodynamik
Fentanyl, som är en ren opioidagonist, verkar primärt genom interaktion med my-opioida receptorer i hjärnan, ryggmärgen och glatt muskulatur. Den primära terapeutiska effekten är en påverkan på det centrala nervsystemet (CNS). Den kliniskt mest användbara farmakologiska effekten av interaktionen mellan fentanyl och my-opioida receptorer är analgesi. De analgetiska effekterna hos fentanyl är relaterade till läkemedlets koncentration i blodet, om vederbörlig hänsyn tas till fördröjningen i samband med läkemedlets väg in i och ut ur CNS (en process med en halveringstid på 3–5 minuter). Hos personer som inte tidigare behandlats med opioider uppnås analgesi vid blodkoncentrationer av den aktiva substansen på 1–2 ng/ml, medan blodkoncentrationer på 10–20 ng/ml förväntas ge kirurgisk anestesi och djup andningsdepression.
Hos patienter med långvarig cancersmärta som stod på stabila doser av regelbundet administrerade opioider för att kontrollera kronisk smärta, gav Actiq signifikant bättre lindring av genombrottssmärta jämfört med placebo 15, 30, 45, och 60 minuter efter administrering.
Till de sekundära effekterna hör en ökning av tonus och en minskning av kontraktionerna hos glatt muskulatur i mag–tarmkanalen, vilket leder till en förlängd passagetid i mag–tarmkanalen, och kan vara orsaken till opioidernas förstoppande effekt.
Medan opioider vanligen ökar tonus i glatt muskulatur i urinvägarna, tenderar den totala effekten att variera, och ger i vissa fall urinträngningar och i andra fall svårighet att urinera.
Alla opioida my–receptoragonister, inklusive fentanyl, ger dosberoende andningsdepression. Risken för andningsdepression är mindre hos patienter med smärta och hos patienter som får kronisk opioidterapi och utvecklar tolerans för andningsdepression och andra opioida effekter. Hos personer som inte utvecklat tolerans ses maximal effekt på andningen vanligen 15–30 minuter efter administrering av Actiq, och effekten kan kvarstå i flera timmar.
Opioider kan påverka hypotalamus-hypofys-binjure- eller hypotalamus-hypofys-gonad-axeln. Exempel på förändringar som har observerats är en ökning av prolaktin i serum och en minskad halt kortisol och testosteron i plasma. Kliniska symtom kan uppträda på grund av dessa hormonförändringar (se även avsnitt Biverkningar).
Ytterligare sekundära farmokologiska effekter inkluderar mios.
Pediatrisk population
Erfarenhet av Actiq hos barn under 16 år är begränsad. I en klinisk studie behandlades 15 (av 38) barn i åldrarna 5 till 15 år, och som redan stod på underhållsbehandling med opioider, för genombrottssmärta med Actiq. Studien var för liten för att kunna dra några slutsatser beträffande säkerhet och effekt i denna patientpopulation.
Farmakokinetik
Allmän introduktion
Fentanyl är starkt lipofilt och kan absorberas mycket snabbt via munslemhinnan och långsammare via konventionell gastrointestinal tillförsel. Det genomgår hepatisk och intestinal första passage–metabolism och metaboliterna bidrar inte till den terapevtiska effekten hos fentanyl.
Absorption
Absorptionen av fentanyl från Actiq sker genom en kombination av dels, en snabb absorption från munslemhinnan, dels en långsammare absorption i mag–tarmkanalen av fentanyl som svalts. Cirka 25% av den totala dosen av Actiq absorberas snabbt från munslemhinnan. Resterande 75% av den totala dosen sväljs med saliven och absorberas sedan långsamt från mag–tarmkanalen. Cirka 1/3 av denna mängd (25% av totaldosen) undgår hepatisk och intestinal första passage–elimination och blir systemiskt tillgänglig. Den absoluta biotillgängligheten är 50% jämfört med intravenöst fentanyl, lika fördelad mellan snabb absorption i munslemhinnan och långsammare gastrointestinal absorption. Cmax varierar mellan 0,39 och 2,51 ng/ml efter administrering av 200–1600 mg Actiq. Tiden till maximal plasmakoncentration (Tmax) är 20–40 minuter efter påbörjat intag av Actiq–enheten (spridning 20–480 minuter).
Distribution
Data från djurstudier visar att fentanyl efter absorption distribueras snabbt till hjärna, hjärta, lungor, njurar och mjälte varefter en långsammare redistribution sker till muskler och fett. Plasmaproteinbindningen hos fentanyl är 80–85%. Den huvudsakliga proteinbindningen sker till alfa–1–glykoprotein, men även albumin och lipoproteiner bidrar i viss grad. Den fria fraktionen av fentanyl ökar vid acidos. Den genomsnittliga distributionsvolymen vid steady state (Vss) är 4 l/kg.
Metabolism
Fentanyl metaboliseras i levern och tarmslemhinnan till norfentanyl via isoenzymet CYP 3A4. I djurstudier har norfentanyl visats vara farmakologiskt inaktivt. Mer än 90% av den givna dosen elimineras genom biotransformation till N–dealkylerade och hydroxylerade inaktiva metaboliter.
Eliminering
Mindre än 7% av dosen utsöndras oförändrat i urin, och endast cirka 1% utsöndras oförändrat i feces. Metaboliterna utsöndras huvudsakligen i urin, medan utsöndringen i feces är av mindre betydelse. Totalt plasmaclearance av fentanyl är 0,5 l/timme/kg (spridning 0,3–0,7 l/timme/kg). Efter administrering av Actiq är den terminala halveringstiden i eliminationsfasen cirka 7 timmar.
Linjäritet/icke-linjäritet
Dosproportionalitet har visats för Actiq över det tillgängliga dosområdet (200 mikrogram–1600 mikrogram).
Pediatrisk population
I en klinisk studie behandlades 15 barn i åldrarna 5-15 år, som redan stod på underhållsbehandling med opioider, för genombrottssmärta med Actiq i dosområdet 200 mikrogram-600 mikrogram. Värdena för area under-kurvan baserat på observerade koncentrationer var 2-faldigt högre hos yngre barn än hos ungdomar (5,25 jämfört med 2,65 ng.timme/ml) och 4-faldigt högre hos yngre barn jämfört med vuxna (5,25 jämfört med 1,20 ng.timme/ml). På en viktanpassad basis var clearance och distributionsvolym likartade i hela åldersgruppen.
Prekliniska uppgifter
Gängse studier avseende säkerhetsfarmakologi, allmäntoxicitet, genotoxicitet och karcinogenicitet visade inte några särskilda risker för människa.
I toxicitetsstudier som undersökte embryofetal utveckling hos råttor och kaniner sågs ingen missbildning eller onormal utveckling som kunde härledas till preparatet när det administrerades under organogenesen.
I en studie av fertilitet och tidig embryonal utveckling hos råttor sågs en effekt överförd av handjuren vid höga doser (300 mikrogram/kg/dag subkutant) som var förenlig med fentanyls sedativa effekt i djurförsök.
I studier av pre- och postnatala utvecklingen hos råttor blev avkommans överlevnad signifikant reducerad vid doser som orsakar allvarlig toxicitet hos mödrarna. Övriga fynd efter administrering av doser som är toxiska för mödrarna, till F1-avkomman var hämmad fysisk utveckling, sensoriska funktioner, reflexer och beteende. Dessa effekter kan antingen vara indirekta effekter som beror på förändringar i honans omvårdnad och/eller nedsatt amningsförmåga eller en direkt effekt av fentanyl på avkomman.
Karcinogenicitetsstudier (26 veckor dermalt alternativ bioassay hos Tg.AC-transgena möss, två års subkutan karcinogenicitetsstudie på råttor) med fentanyl visade inga fynd med onkogen potential. Bedömning av bilder av hjärnan från karcinogenicitetsstudien på råttor visade hjärnlesioner på djur som fått höga doser av fentanylcitrat. Relevansen av dessa fynd för människor är okänd.
Innehåll
Kvalitativ och kvantitativ sammansättning
Actiq 200 mikrogram komprimerad sugtablett med applikator.
En sugtablett innehåller 200 mikrogram fentanyl (som citrat).
Actiq 400 mikrogram komprimerad sugtablett med applikator.
En sugtablett innehåller 400 mikrogram fentanyl (som citrat).
Actiq 600 mikrogram komprimerad sugtablett med applikator.
En sugtablett innehåller 600 mikrogram fentanyl (som citrat).
Actiq 800 mikrogram komprimerad sugtablett med applikator.
En sugtablett innehåller 800 mikrogram fentanyl (som citrat).
Actiq 1200 mikrogram komprimerad sugtablett med applikator.
En sugtablett innehåller 1200 mikrogram fentanyl (som citrat).
Actiq 1600 mikrogram komprimerad sugtablett med applikator.
En sugtablett innehåller 1600 mikrogram fentanyl (som citrat).
Hjälpämnen med känd effekt:
En sugtablett innehåller ca 1,89 g glukos och 20-36 mg sackaros.
Förteckning över hjälpämnen
Sugtablett:
Hydrerade dextrater (innehållande glukos)
Citronsyra
Dinatriumfosfat
Artificiellt bärsmakämne (maltodextrin (innehåller glukos), propylenglykol, artificiella smakämnen och trietylcitrat)
Magnesiumstearat
Ätligt bindemedel som används till att fästa sugtabletten vid applikatorn:
Modifierad majsbaserad livsmedelsstärkelse, (E 1450)
Florsocker (innehåller sackaros och majsstärkelse)
Vatten, renat
Märkbläck:
Avjoniserat vatten
Avparaffinerat vitt shellack
Propylenglykol
Briljantblått (E 133)
Ammoniumhydroxid (E527) för justering av pH
Hållbarhet, förvaring och hantering
Förvaras vid högst 30°C.
Förvaras i skyddande blister tills det ska användas.
Sugtabletter med kvarvarande aktiv substans får inte kastas i soporna. Ej använt läkemedel och avfall skall kasseras enligt gällande anvisningar.
Egenskaper hos läkemedelsformen
Actiq består av en vit till benvit komprimerad sugtablett som med hjälp av ett ätligt bindemedel är fäst vid en applikator av plast. Applikatorn är svår att bryta av, synlig vid röntgen och märkt med styrkan.





