Indikationer
Oral antikonception
Vid beslut att förskriva Estron ska den enskilda kvinnans riskfaktorer beaktas, framför allt de för venös tromboembolism (VTE), och risken för VTE med Estron jämfört med andra kombinerade hormonella preventivmedel (se avsnitt Kontraindikationer och Varningar och försiktighet).
Kontraindikationer
Kombinerade p-piller ska inte användas vid nedanstående tillstånd. Om något av dessa tillstånd uppstår för första gången under användningen av kombinerade p-piller, bör behandlingen upphöra omgående.
• Överkänslighet mot de aktiva substanserna eller mot något hjälpämne som anges i avsnitt Innehåll
• Förekomst av eller risk för venös tromboembolism (VTE)
o Venös tromboembolism – pågående VTE (på antikoagulantia) eller anamnes på (t.ex. djup ventrombos [DVT] eller lungemboli [PE])
o Känd ärftlig eller förvärvad predisposition för venös tromboembolism, t.ex. APC resistens (inklusive Faktor V Leiden), antitrombin III brist, protein C brist, protein S brist
o Större kirurgiskt ingrepp med långvarig immobilisering (se avsnitt Varningar och försiktighet)
o Hög risk för venös tromboembolism på grund av förekomst av flera riskfaktorer (se avsnitt Varningar och försiktighet)
• Förekomst av eller risk för arteriell tromboembolism (ATE)
o Arteriell tromboembolism – pågående arteriell tromboembolism, anamnes på arteriell tromboembolism (t.ex. myokardiell infarkt) eller prodromalsymtom (t.ex. angina pectoris)
o Cerebrovaskulär sjukdom – pågående stroke, anamnes på stroke eller prodromalsymtom (t.ex. transitorisk ischemisk attack, TIA)
o Känd ärftlig eller förvärvad predisposition för arteriell tromboembolism, t.ex. hyperhomocysteinemi och antifosfolipidantikroppar (antikardiolipinantikroppar, lupus antikoagulant)
o Migrän med fokala neurologiska symtom i anamnesen
o Hög risk för arteriell tromboembolism på grund av flera riskfaktorer (se avsnitt Varningar och försiktighet) eller på grund av förekomst av en allvarlig riskfaktor som:
• diabetes mellitus med vaskulära symtom
• allvarlig hypertoni
• allvarlig dyslipoproteinemi
• Pågående eller tidigare allvarlig leversjukdom, så länge leverfunktionsvärdena inte återgått till de normala
• Allvarlig njurinsufficiens eller akut njursvikt
• Pågående eller tidigare levertumör, (godartad eller malign)
• Känt eller misstänkt malignt tillstånd i genitalier eller bröst, om detta är könshormonberoende
• Odiagnostiserad vaginalblödning
Estron är kontraindicerat vid samtidig användning med läkemedel som innehåller ombitasvir/paritaprevir/ritonavir och dasabuvir, läkemedel som innehåller glekaprevir/pibrentasvir eller sofosbuvir/velpatasvir/voxilaprevir (se avsnitt Interaktioner).
Dosering
Dosering
Hur används Estron?
Tabletterna bör tas vid ungefär samma tid varje dag, om nödvändigt tillsammans med lite vätska, och fortlöpande i den ordning som visas på blisterförpackningen. En tablett tas dagligen i 28 dagar. Varje nästkommande förpackning påbörjas dagen efter man tog sista tabletten på föregående karta. Bortfallsblödningen börjar vanligen på dag 2-3 efter påbörjat intag av placebo-tabletterna (sista raden) och har i vissa fall inte upphört innan nästa blisterförpackning påbörjas.
Hur man börjar ta Estron
• Om inte något hormonellt preventivmedel använts under den senaste månaden
Tablettintaget skall påbörjas på dag 1 i kvinnans naturliga menstruationscykel (d.v.s. den första blödningsdagen).
• Vid byte från ett kombinerat hormonellt preventivmedel (kombinerat oralt preventivmedel, vaginalring eller transdermalt plåster)
Kvinnan bör helst påbörja intaget av Estron-dagen efter den sista aktiva tabletten (den sista tabletten som innehåller aktiv substans) med det tidigare p-pillret, men senast dagen efter den tablettfria perioden alternativt efter perioden med placebotabletter av det tidigare p-pillret. Om en vaginalring eller ett transdermalt plåster har använts bör kvinnan helst påbörja intaget av Estron samma dag som ringen eller plåstret tas bort, och allra senast när nästa behandling/applicering skulle ha inletts.
• Vid byte från metod med enbart gestagen (minipiller, injektion, implantat) eller ett gestagenutsöndrande intrauterint system (IUS)
Det går att byta när som helst från minipiller (från ett implantat eller spiral på dagen för dess avlägsnande, från ett injicerbart preventivmedel vid tidpunkten för nästa injektion), men kvinnan bör rådas att i dessa fall använda barriärmetod de första 7 dagarna av tablettintag
• Efter abort i första trimestern
Intaget kan påbörjas med det samma. I detta fall behövs inget ytterligare skydd.
• Efter förlossning eller abort i andra trimestern
Kvinnan bör rådas att påbörja behandlingen mellan dag 21 och 28 efter förlossningen eller aborten i andra trimestern. Om hon börjar intaget senare bör hon rådas att dessutom använda en barriärmetod under de första sju dagarna. Har samlag redan ägt rum bör graviditet uteslutas innan p-pilleranvändningen påbörjas eller så måste kvinnan invänta sin första mens.
För ammande kvinnor, se avsnitt Graviditet.
Om man har glömt att ta tabletter
Glömda tabletter från den sista raden på blisterkartan är placebo-tabletter och detta kan förbises. Dessa bör kastas bort för att undvika en oavsiktlig förlängning av perioden med placebo-tabletter.
Följande råd avser endast om man glömt aktiva tabletter (rad 1-3 på blisterkartan):
Om det har gått högst 12 timmar sedan tabletten skulle ha tagits är det preventiva skyddet inte nedsatt. Tabletten bör tas så snart som möjligt och nästa tablett tas sedan vid ordinarie tidpunkt.
Om det har gått mer än 12 timmar sedan tabletten skulle ha tagits, kan den preventiva säkerheten vara nedsatt. Följande två grundregler gäller vid glömd tablett:
1. tablettuppehållet får aldrig överskrida 7 dagar
2. 7 dagars oavbrutet tablettintag krävs för att uppnå tillräcklig hämning av hypotalamus-hypofys-ovarie axeln.
I enlighet med detta kan följande råd användas i allmän praxis:
• Vecka 1
Den senast glömda tabletten ska tas så snart som kvinnan kommer ihåg, även om detta innebär att hon tar två tabletter vid samma tillfälle. Därefter fortsätter hon att ta tabletterna på ordinarie tidpunkt. En barriärmetod som kondom bör användas de närmaste sju dagarna. Har samlag ägt rum under de föregående sju dagarna, bör möjligheten av en graviditet övervägas. Ju fler glömda tabletter och ju närmare de är perioden med placebo-tabletterna, desto större är risken för graviditet.
• Vecka 2
Den senast glömda tabletten ska tas så snart som möjligt, även om detta innebär att två tabletter tas vid samma tillfälle. Därefter tas tabletterna på ordinarie tidpunkt. Under förutsättning att tabletterna tagits vid rätt tidpunkt de föregående sju dagarna, behövs inget ytterligare skydd. Om mer än 1 tablett är glömd bör kompletterande skydd användas under sju dagar.
• Vecka 3
Risken för minskad tillförlitlighet är överhängande med tanke på den kommande 7-dagars perioden med placebo-tabletter. Genom att justera schemat för tablettintaget, går det emellertid att förhindra att skyddseffekten minskar. Följer man något av följande två alternativ behövs därför inget extra skydd, under förutsättning att alla tabletterna togs på rätt tid under de sju dagarna precis innan den första glömda tabletten.
Om så inte är fallet, bör det första alternativet följas och extra skydd bör användas även under de kommande sju dagarna.
1. Den senast glömda tabletten bör tas så snart som möjligt, även om detta innebär att två tabletter tas vid samma tidpunkt. Därefter tas tabletterna på ordinarie tidpunkt tills alla aktiva tabletterna har tagits. De sju tabletterna från sista raden (placebo-tabletterna) kastas. Nästa blisterförpackning måste påbörjas med en gång. Kvinnan kommer troligtvis inte få någon bortfallsblödning förrän alla aktiva tabletterna på den andra förpackningen har tagits, men spotting eller genombrottsblödning kan uppträda under dagar då tabletter tas.
2. Kvinnan kan också rådas att avbryta intaget av aktiva tabletter från den aktuella blisterkartan. Därefter ska hon ta tabletter från den sista tablettraden (placebo-tabletter) i upp till sju dagar, inklusive de dagar hon glömt tabletter, och därefter fortsätta med nästa förpackning.
Vid glömda tabletter och vid utebliven bortfallsblödning under dagarna med placebo-tabletter, bör möjligheten för graviditet beaktas.
Råd vid gastrointestinala sjukdomstillstånd
Vid kraftiga gastrointestinala störningar (t.ex. kräkningar eller diarré) kan absorptionen vara ofullständig och ytterliggare preventiva åtgärder bör vidtas. Vid kräkningar inom 3-4 timmar efter intag av aktiva tabletter, skall en ny tablett (ersättningstablett) tas så snart som möjligt. Den nya tabletten skall om möjligt tas inom 12 timmar från den vanliga tiden för tablettintag. Om mer än 12 timmar passerat gäller de råd vid glömda tabletter som ges i avsnitt Dosering ”Om man har glömt att ta tabletter”. Om kvinnan inte vill ändra sitt normala schema för intag av tabletter, måste de extra tabletterna tas från en annan blisterkarta.
Att förskjuta menstruationen
För att förskjuta menstruationen bör kvinnan fortsätta med nästa blisterkarta Estron utan att ta placebo-tabletterna från den ursprungliga tablettkartan. Förskjutningen kan pågå fram till att den andra förpackningens aktiva tabletter är slut. Under förskjutningen kan genombrottsblödning eller spotting uppträda. Normalt intag av Estron återupptas sedan efter dagarna med placebo-tabletter.
För att ändra blödningsdag till en annan veckodag än den vanliga, kan perioden med intag av placebo-tabletter förkortas med önskat antal dagar. Ju kortare uppehåll, desto större risk att bortfallsblödningen uteblir och att kvinnan får en genombrottsblödning och spotting under intag från efterföljande karta (på samma sätt som vid förskjutning av menstruationen).
Ytterligare information om särskilda patientgrupper
Pediatrisk population
Estron är endast indicerat efter menarke.
Äldre
Estron är inte indicerat efter menopaus.
Patienter med nedsatt leverfunktion
Estron är kontraindicerad hos kvinnor med allvarlig leversjukdom, se även avsnitt Kontraindikationer och Farmakokinetik.
Patienter med nedsatt njurfunktion
Estron är kontraindicerad hos kvinnor med kraftigt nedsatt njurfunktion eller akut njursvikt, se även avsnitt Kontraindikationer och Farmakokinetik.
Administreringssätt
Oral användning
Varningar och försiktighet
Varningar
Vid förekomst av någon av de tillstånd eller riskfaktorer som anges nedan, bör lämpligheten av Estron diskuteras med kvinnan.
Om något av dessa tillstånd eller riskfaktorer förvärras eller uppträder för första gången, ska kvinnan ta kontakt med sin läkare/barnmorska. Läkare/barnmorska ska då besluta om användningen ska avbrytas.
Vid misstänkt eller bekräftad VTE eller ATE bör användningen av kombinerade p-piller avbrytas. I fall där terapi med antikoagulantia inleds bör lämpligt alternativt preventivmedel sättas in på grund av teratogeniciteten i antikoagulationsterapin (kumariner).
Cirkulationsrubbningar
Risk för venös tromboembolism (VTE)
Användning av ett kombinerat hormonellt preventivmedel ökar risken för venös tromboembolism (VTE) jämfört med icke-användning. Produkter som innehåller levonorgestrel, norgestimat eller noretisteron förknippas med den lägsta risken för VTE. Det är ännu inte känt hur hög risken är med Estron jämfört med dessa produkter med lägre risk. Beslutet att använda en annan produkt än den med den lägsta risken för VTE ska tas först efter en diskussion med kvinnan för att säkerställa att hon känner till risken för VTE med kombinerade hormonella preventivmedel, hur hennes riskfaktorer påverkar den här risken, och att hennes VTE risk är störst under det första året hon använder produkten. Det finns också vissa belägg för att risken är större när ett kombinerat hormonellt preventivmedel används igen efter ett uppehåll på 4 veckor eller längre.
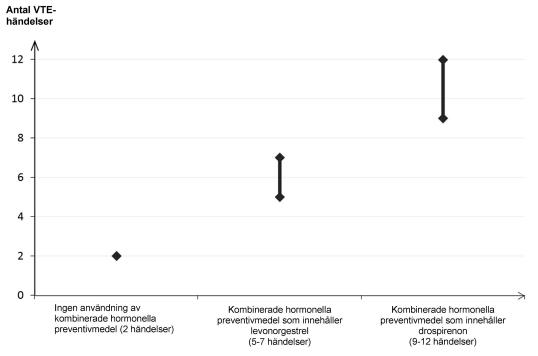
Hos kvinnor som inte använder ett kombinerat hormonellt preventivmedel och som inte är gravida kommer cirka 2 av 10 000 att utveckla en VTE under en period om ett år. Hos en enskild kvinna kan dock risken vara betydligt högre, beroende på hennes underliggande riskfaktorer (se nedan).
Man uppskattar1 att av 10 000 kvinnor som använder kombinerade hormonella preventivmedel innehållande drospirenon kommer mellan 9 och 12 kvinnor att utveckla en VTE under ett år; detta kan jämföras med cirka 62 kvinnor som använder kombinerade hormonella preventivmedel som innehåller levonorgestrel.
I båda fallen är antalet VTE-händelser per år färre än det antal händelser som förväntas hos kvinnor under graviditet eller under postpartumperioden.
VTE kan vara dödligt i 1 2 % av fallen.
1 Dessaförekomster uppskattades från samtliga epidemiologiska studiedata med hjälp av relativa risker för de olika produkterna jämfört med kombinerade hormonella preventivmedel som innehåller levonorgestrel.
2Genomsnittsintervallet är på 57 per 10 000 kvinnoår, baserat på en relativ risk för kombinerade hormonella preventivmedel som innehåller levonorgestrel jämfört med en icke användning på cirka 2,3 till 3,6
I extremt sällsynta fall har trombos rapporterats hos användare av kombinerade hormonella preventivmedel i andra blodkärl, t.ex. i hepatiska, mesenteriska, renala eller retinala vener och artärer.
Riskfaktorer för VTE
Risken för venösa tromboemboliska komplikationer hos användare av kombinerade hormonella preventivmedel kan öka betydligt hos kvinnor med ytterligare riskfaktorer, framför allt om flera riskfaktorer föreligger (se tabell).
Estron är kontraindicerat om en kvinna har flera riskfaktorer som innebär att hon löper hög risk för venösa tromboser (se avsnitt Kontraindikationer). Om en kvinna har mer än en riskfaktor är det möjligt att risken är större än summan av de enskilda faktorerna – i detta fall bör hennes totala risk för VTE beaktas. Om förhållandet nytta risk anses vara negativt ska ett kombinerat hormonellt preventivmedel inte förskrivas (se avsnitt Kontraindikationer).
Tabell: Riskfaktorer för VTE
|
Riskfaktor |
Kommentar |
|---|---|
|
Fetma (BMI över 30 kg/m2) |
Risken ökar betydligt när BMI ökar. Detta är särskilt viktigt att beakta om det också finns andra riskfaktorer. |
|
Långvarig immobilisering , större kirurgiskt ingrepp, alla operationer i ben eller bäcken, neurokirurgi eller omfattande skada Anm: tillfällig immobilisering inklusive flygresor >4 timmar kan också vara en riskfaktor för VTE, särskilt hos kvinnor med andra riskfaktorer |
I dessa situationer är det lämpligt att göra ett uppehåll i användningen av p pillret (vid elektiv kirurgi minst fyra veckor i förväg) och inte återuppta användningen förrän två veckor efter fullständig remobilisering. En annan preventivmetod bör användas för att undvika oavsiktlig graviditet. Antitrombotisk behandling bör övervägas om Estron inte har satts ut i förväg. |
|
Positiv familjeanamnes (venös tromboembolism hos ett syskon eller förälder i relativt unga år, t.ex. före 50 års ålder). |
Om man misstänker en hereditär predisposition, ska kvinnan remitteras till en specialist för rådgivning innan hon beslutar sig för att använda någon form av kombinerade hormonella preventivmedel. |
|
Andra medicinska tillstånd som förknippas med VTE |
Cancer, systemisk lupus erythematosus, hemolytiskt uremiskt syndrom, kronisk inflammatorisk tarmsjukdom (Crohns sjukdom eller ulcerös kolit) och sicklecell sjukdom. |
|
Stigande ålder |
Framför allt hos kvinnor över 35 år. |
Det råder inte enighet om den eventuella betydelsen av varicer och ytlig tromboflebit har för uppkomst eller progression av venös trombos.
Den ökade risken för tromboembolism vid graviditet, och framför allt 6 veckorsperioden i puerperiet måste beaktas (för information om ”Graviditet och amning” se avsnitt Graviditet.)
Symtom på VTE (djup ventrombos och lungemboli)
Vid symtom ska kvinnan rådas att omedelbart söka läkare och informera vårdpersonalen om att hon tar kombinerade hormonella preventivmedel.
Symtom på djup ventrombos (DVT) kan omfatta:
- unilateral svullnad av ben och/eller fot eller längs en ven i benet
- smärta eller ömhet i benet som bara känns vid stående eller gående
- ökade värme i det drabbade benet med rödfärgning eller missfärgning av benet.
Symtom på lungemboli (PE) kan omfatta:
- plötslig debut av oförklarlig andfåddhet eller snabb andning
- plötslig hosta som kan förknippas med hemoptys
- kraftig bröstsmärta
- kraftig ostadighetskänsla eller yrsel
- snabba eller oregelbundna hjärtslag.
En del av dessa symtom (t.ex. andfåddhet och hosta) är icke specifika och kan feltolkas som mer vanliga eller mindre allvarliga händelser (t.ex. luftvägsinfektioner).
Andra tecken på vaskulär ocklusion kan omfatta: plötslig smärta, svullnad och lätt blå missfärgning av en extremitet.
Om ocklusionen uppkommer i ögonen kan symtomen variera från smärtfri dimsyn som kan utvecklas till synförlust. Ibland kan synförlust uppkomma nästa omedelbart.
Risk för arteriell tromboembolism (ATE)
Epidemiologiska studier har också visat ett samband mellan användning av kombinerade hormonella preventivmedel och en ökad risk för arteriell tromboembolism (myokardinfarkt) eller cerebrovaskulär händelse (t.ex. transitorisk ischemisk attack, stroke). Arteriella tromboemboliska händelser kan vara dödliga.
Riskfaktorer för ATE
Risken för arteriella tromboemboliska komplikationer eller för en cerebrovaskulär händelse hos användare av kombinerade hormonella preventivmedel ökar hos kvinnor med riskfaktorer (se tabell). Estron är kontrainidcerat om kvinnan har en allvarlig eller flera riskfaktorer som innebär att hon löper hög risk för ATE (se avsnitt Kontraindikationer). Om kvinnan har mer än en riskfaktor är det möjligt att riskökningen är större än summan av de enskilda faktorerna – i detta fall bör hennes totala risk beaktas. Om förhållandet nytta risk anses vara negativt ska ett kombinerat hormonellt preventivmedel inte förskrivas (se avsnitt Kontraindikationer).
Tabell: Riskfaktorer för ATE
|
Riskfaktor |
Kommentar |
|---|---|
|
Stigande ålder |
Framför allt hos kvinnor över 35 år |
|
Rökning |
Kvinnor över 35 år bör starkt rekommenderas att sluta röka om de vill använda ett kombinerat hormonellt preventivmedel. Kvinnor över 35 år som fortsätter att röka ska starkt rekommenderas att använda en annan preventivmetod. |
|
Hypertoni | |
|
Fetma (BMI över 30 kg/m2) |
Risken ökar betydligt när BMI ökar. Detta är särskilt viktigt för kvinnor med ytterligare riskfaktorer. |
|
Positiv familjeanamnes (arteriell tromboembolism hos ett syskon eller förälder i relativt unga år, t.ex. före 50 års ålder). |
Om man misstänker en hereditär predisposition, ska kvinnan remitteras till en specialist för rådgivning innan hon beslutar sig för att använda någon form av kombinerade hormonella preventivmedel. |
|
Migrän |
En ökning av frekvens eller svårighetsgrad av migrän vid användning av kombinerade hormonella preventivmedel (som kan vara prodromalsymtom på en cerebrovaskulär händelse) kan vara ett skäl för omedelbart utsättande. |
|
Andra medicinska tillstånd som förknippas med negativa vaskulära händelser |
Diabetes mellitus, hyperhomocysteinemi, hjärtklaffssjukdom och förmaksflimmer, dyslipoproteinemi och systemisk lupus erythematosus. |
Symtom på ATE
Vid symtom ska kvinnan rådas att omedelbart söka läkare och informera hälso- och sjukvårdpersonalen om att hon tar kombinerade hormonella preventivmedel.
Symtom på en cerebrovaskulär händelse kan omfatta:
- plötslig domning eller svaghet i ansikte, armar eller ben, speciellt på en sida av kroppen
- plötsliga problem med att gå, yrsel, förlorad balans eller koordination
- plötslig förvirring, svårigheter att tala eller förstå
- plötsliga synproblem i ett eller båda ögonen
- plötslig, svår eller långvarig huvudvärk utan känd orsak
- medvetslöshet eller svimning med eller utan anfall.
Tillfälliga symtom som tyder på att händelsen är en transitorisk ischemisk attack (TIA).
Symtom på en hjärtinfarkt kan vara:
- smärta, obehag, tryck, tyngdkänsla, tryck eller fyllnadskänsla i bröstet, armen eller nedanför bröstbenet
- obehag som strålar mot ryggen, käken, halsen, armen, magen
- mättnadskänsla, matsmältningsbesvär eller kvävning
- svettning, illamående, kräkningar eller yrsel
- extrem svaghet, ångest eller andfåddhet
- snabba eller oregelbundna hjärtslag.
• Tumörer
En ökad risk för cervixcancer hos kvinnor som använt kombinerade p-piller under lång tid (> 5 år) har rapporterats i vissa epidemiologiska studier, men fortsatt oenighet råder om i vilken omfattning detta kan vara resultat av ett sexuellt beteende och andra faktorer såsom humant papillomavirus (HPV).
En metaanalys från 54 epidemiologiska studier visade på en något ökad relativ risk (RR = 1,24) att få bröstcancer diagnostiserad hos kvinnor som använder kombinerade p-piller. Den ökade risken försvinner gradvis under loppet av tio år efter avslutad användning. Eftersom bröstcancer är ovanligt hos kvinnor under 40 års ålder är den ökade risken för bröstcancerdiagnos hos användare och före detta användare av kombinerade p-piller liten i jämförelse med den generella risken för bröstcancer. Dessa studier visar inte på något kausalt samband. Det observerade mönstret för ökad risk kan bero på att bröstcancer diagnostiseras tidigare hos kvinnor som använder kombinerade p-piller, de biologiska effekterna av kombinerade p-piller eller av en kombination av dessa. Bröstcancer som diagnostiseras hos de som någon gång använt p-piller tenderar att vara mindre kliniskt avancerade jämfört med cancer hos de som aldrig använt p-piller.
I sällsynta fall har godartade levertumörer, och ännu mer sällan, maligna levertumörer rapporterats hos användare av kombinerade p-piller. I enstaka fall har dessa tumörer lett till livshotande intra-abdominella blödningar. Levertumör bör övervägas som differentialdiagnos när svår smärta i övre delen av buken, leverförstoring eller tecken på intra-abdominell blödning uppträder hos kvinnor som använder kombinerade p-piller.
Användning av högdoserade kombinerade p-piller (50 µg etinylestradiol) minskar risken för endometrie- och ovariecancer. Om detta även gäller för lågdoserade kombinerade p-piller är ännu inte bekräftat.
• Övriga tillstånd
Den gestagena komponenten i Estron är en aldosteronantagonist med kaliumsparande effekt. I de flesta fall förväntas ingen ökning av kaliumnivåerna. I en klinisk studie sågs dock en liten men inte signifikant ökning av serumkaliumnivåerna under behandling med drospirenon, hos patienter med lätt eller måttlig njurfunktionsnedsättning och samtidig användning av kaliumsparande läkemedel. Kontroll av serumkalium rekommenderas därför under den första behandlingscykeln hos patienter med njurinsufficiens och där serumkalium före behandling ligger i övre delen av referensområdet, särskilt vid samtidig användning av kaliumsparande läkemedel. Se även avsnitt Interaktioner.
Kvinnor med hypertriglyceridemi eller sådan i familjeanamnesen kan ha en förhöjd risk för pankreatit vid användning av kombinerade p-piller.
Även om små höjningar av blodtrycket har rapporterats hos många kvinnor som använder kombinerade p-piller, är kliniskt relevanta höjningar sällsynta. Endast i dessa sällsynta fall finns skäl för att omedelbart avbryta användningen av kombinerade p-piller. Stiger blodtrycksvärden konstant eller en kliniskt signifikant blodtrycksökning inte svarar tillräckligt på blodtryckssänkande behandling hos kvinnor som redan har hypertoni, måste det kombinerade p-pillret sättas ut. När så anses lämpligt kan användningen av ett kombinerat p-piller återupptas om normala blodtrycksvärden uppnås med blodtryckssänkande terapi.
Följande tillstånd har rapporterats förekomma eller förvärras både i samband med graviditet och användning av kombinerade p-piller, men det finns inte övertygande bevis för ett samband med användning av kombinerade p-piller: gulsot och/eller klåda relaterad till kolestas, gallsten, porfyri, systemisk lupus erythematosus, hemolytiskt uremiskt syndrom, Sydenhams korea, herpes gestationis, otosklerosrelaterad hörselnedsättning.
Hos kvinnor med ärftligt angioödem kan exogena östrogener inducera eller förvärra symtomen av angioödem.
Akuta eller kroniska störningar av leverfunktionen kan göra det nödvändigt att sätta ut behandlingen av kombinerade p-piller tills värdena för leverfunktionen återgår till de normala. Recidiv av kolestatisk gulsot och/eller kolestasrelaterad klåda som tidigare uppträtt under en graviditet eller under tidigare användning av könshormoner gör det nödvändigt att avbryta användningen av kombinerade p-piller.
Även om kombinerade p-piller kan påverka den perifera insulinresistansen och glukostoleransen, finns det inga bevis för att det är nödvändigt att ändra doseringen hos diabetiker som använder kombinerade p-piller (innehållande < 0,05 mg etinylestradiol). Kvinnor som har diabetes bör dock stå under noggrann läkarkontroll, speciellt under den första tiden med kombinerade p-piller.
Försämring av epilepsi, Crohns sjukdom och ulcerös kolit, har rapporterats under användning av kombinerade p-piller.
Ibland kan kloasma förekomma, särskilt hos kvinnor som haft kloasma under tidigare graviditet. Kvinnor med benägenhet för kloasma bör undvika solexponering eller exponering för ultraviolett ljus under användning av kombinerade p-piller.
Nedstämdhet och depression är välkända biverkningar vid användning av hormonella preventivmedel (se avsnitt Biverkningar). Depressioner kan vara allvarliga och är en välkänd riskfaktor för självmordsbeteende och självmord. Kvinnor ska rådas att kontakta läkare vid humörförändringar och depressiva symtom, också direkt efter inledd behandling.
Läkarundersökning/konsultation
Innan användning av Estron påbörjas eller används igen ska en fullständig anamnes (inklusive hereditet) tas och graviditet uteslutas. Blodtrycket ska tas och en läkarundersökning ska utföras baserad på kontraindikationerna (se avsnitt Kontraindikationer) och varningar (se avsnitt Varningar och försiktighet). Det är viktigt att informera kvinnan om venösa och arteriella tromboser, inklusive risken med Estron jämfört med andra kombinerade hormonella preventivmedel, symtomen på VTE och ATE, de kända riskfaktorerna och vad hon ska göra i händelse av en misstänkt trombos.
Kvinnan ska också informeras om att noggrant läsa igenom bipacksedeln och följa anvisningarna. Frekvensen och typen av undersökningar ska baseras på fastställda riktlinjer och anpassas individuellt till varje kvinna.
Kvinnan ska informeras om att hormonella preventivmedel inte skyddar mot hiv infektioner (AIDS) och andra sexuellt överförbara sjukdomar.
Minskad effekt
Säkerheten hos kombinerade p-piller kan försämras t.ex. vid glömd aktiv tablett (se avsnitt Dosering) vid gastrointestinal störning (se avsnitt Dosering) vid intag av aktiv tablett eller vid samtidig användning av andra läkemedel (se avsnitt Interaktioner).
Försämrad cykelkontroll
Oregelbundna blödningar (spotting eller genombrottsblödning) kan förekomma med alla kombinerade p-piller, särskilt under de första månadernas användning och en tillvänjningsperiod på ca tre cykler behövs innan en utvärdering kan göras.
Kvarstår de oregelbundna blödningarna eller om de uppträder efter tidigare regelbundna cykler, bör icke-hormonella orsaker övervägas och malignitet eller graviditet uteslutas. Abrasio kan också bli aktuellt.
Hos vissa kvinnor kan bortfallsblödningen utebli under perioden med placebo-tabletter. Om p-pillret har tagits enligt anvisningarna i avsnitt Dosering, är kvinnan sannolikt inte gravid. Har p-pillret däremot inte tagits enligt anvisningarna före den första uteblivna bortfallsblödningen eller om två bortfallsblödningar uteblivit, måste graviditet uteslutas innan kvinnan fortsätter använda kombinerade p-piller.
Estron innehåller laktos och natrium
Varje rosa tablett av detta läkemedel innehåller 44 mg laktos per tablett, varje vit tablett innehåller 89,5 mg. Patienter med sällsynta ärftliga sjukdomar som galaktosintolerans, total laktasbrist eller glukos-galaktos malabsorption bör inte ta detta läkemedel.
Detta läkemedel innehåller mindre än 1 mmol natrium (23 mg) per tablett, dvs. är i stort sett ”natriumfritt”.
Interaktioner
Observera: Produktresumé för andra, samtidigt använda, läkemedel, skall konsulteras för att identifiera potentiella interaktioner.
• Andra läkemedels påverkan på Estron
Interaktioner kan förekomma med läkemedel som inducerar mikrosomala enzymer vilket kan resultera i ökad clearance av könshormoner och som kan leda till genombrottsblödningar och/eller utebliven preventiv effekt.
Hantering
Enzyminducering kan observeras redan efter några dagars behandling. Maximal enzyminduktion ses vanligtvis inom några veckor. Efter avslutad behandling kan enzyminduktionen upprätthållas under ca 4 veckor.
Korttidsbehandling
Kvinnor som behandlas med enzyminducerande läkemedel bör temporärt använda en barriärmetod eller annan preventivmetod i tillägg till kombinerade p-piller. Barriärmetoden måste användas under hela tiden för samtidig läkemedelsbehandling och 28 dagar efter avslutad behandling. Om läkemedelsbehandlingen löper längre än till slutet av tabletterna i p-pillerkartan, ska placebotabletterna kastas och nästa p-pillerkarta påbörjas direkt.
Långtidsbehandling
Hos kvinnor som står på långtidsbehandling med leverenzyminducerande aktiva substanser rekommenderas en annan pålitlig icke-hormonell preventivmetod.
Följande interaktioner har rapporterats i litteraturen
Substanser som ökar clearance av kombinerade p-piller (minskad effekt av kombinerade p-piller genom enzyminduktion), exempelvis:
Barbiturater, bosentan, karbamazepin, fenytoin, primidon, rifampicin, och HIV-läkemedlen ritonavir, nevirapin och efavirenz och eventuellt även felbamat, griseofulvin, oxkarbazepin, topiramat och produkter som innehåller naturläkemedlet Johannesört (hypericum perforatum).
Substanser med varierande effekt på clearance av kombinerade p-piller:
Vid samtidig administrering med kombinerade p-piller kan många kombinationer av HIV-proteashämmare och icke-nukleosid omvänt transkriptas-hämmare, inklusive kombinationer med HCV-hämmare, öka eller minska plasmakoncentrationen av östrogen eller progesteron. Nettoeffekten av dessa förändringar kan vara kliniskt relevant i vissa fall.
Därför bör produktinformationen för samtidiga HIV/HCV läkemedel konsulteras för att identifiera potentiella interaktioner och eventuella tillhörande rekommendationer. I tveksamma fall bör ytterligare barriärmetod användas av kvinnor som behandlas med proteashämmare eller icke-nukleosid omvänt transkriptas-hämmare.
Substanser som minskar clearance av kombinerade p-piller (ensymhämmare).
Den kliniska relevansen av potentiella interaktionermed ensymhämmare är fortfarande okänd.
Samtidig administrering av starka CYP3A4-hämmare kan öka plasmakoncentrationerna av östrogenet eller gestagenet eller båda.
En multipel dosstudie med drospirenon (3mg/dag)/ etinylestradiol (0,02 mg/dag) visar att samtidig administrering av den starka CYP3A4-hämmaren ketokonazol i 10 dagar ökar AUC (0-24 h) av drospirenon och etinylestradiol 2,7 gånger respektive 1,4 gånger.
När doser med etoricoxib 60-120 mg/dag tas samtidigt med ett kombinationspreparat som innehåller 35 mikrogram etinylestradiol ökar plasmakoncentrationen av etinylestradiol 1,4-1,6 gånger.
• Inverkan av Estron på andra läkemedel
Orala antikonceptiva medel kan påverka metabolismen av vissa andra aktiva substanser. Följaktligen kan koncentrationen i plasma och vävnad antingen öka (t.ex. ciklosporin) eller minska (t.ex. lamotrigin).
Baserat på in vivo-interaktionsstudier på kvinnliga frivilliga försökspersoner som använder omeprazol, simvastatin eller midazolam som markörsubstrat är en kliniskt relevant interaktion av drospirenon vid doser på 3 mg med cytokrom P-450 medierad metabolism hos andra aktiva substanser osannolik.
Kliniska data tyder på att etinylestradiol inhiberar clearance av CYP1A2 substrat som leder till en svag (t ex teofyllin) eller måttlig (t.ex. tizanidin) ökning av deras plasmakoncentration.
• Farmakodynamiska interaktioner
I kliniska studier med patienter som behandlas för hepatit C-virusinfektioner (HCV) med läkemedel som innehåller ombitasvir/paritaprevir/ritonavir och dasabuvir, med eller utan ribavirin, sågs en alanintransaminasstegring (ALAT) som var mer än 5 gånger högre än den normala övre gränsen. ALAT-stegringen inträffade signifikant oftare hos kvinnor som använde etinylestradiolinnehållande läkemedel, såsom kombinerade preventivmedel (CHCs). ALAT-stegringar har också observerats hos patienter som behandlas med glekaprevir/pibrentasvir eller sofosbuvir/velpatasvir/voxilaprevir och använder läkemedel innehållande etinylestradiol såsom CHCs (se avsnitt Kontraindikationer).
Därför måste användare av Estron byta till en alternativ preventivmedelsmetod (t ex läkemedel som endast innehåller gestagen eller icke-hormonella metoder) innan behandlingen med dessa läkemedelskombinationer påbörjas. Estron kan påbörjas igen 2 veckor efter avslutad behandling med dessa läkemedelskombinationer
• Övriga interaktioner
Hos patienter utan njurinsufficiens visade ett samtidigt intag av drosperinon och ACE-hämmare eller NSAID preparat ingen signifikant effekt på serumkalium. Samtidig användning av Estron och aldosteronantagonister eller kaliumsparande diuretika är dock ej undersökt. I detta fall bör serumkalium testas under första behandlingscykeln. Se även avsnitt Varningar och försiktighet.
• Laboratorietester
Användningen av steroider för antikonception kan påverka resultaten av vissa laboratorietest, inklusive biokemiska parametrar för lever-, sköldkörtel-, binjure- och njurfunktioner, plasmanivåer för (bärar-) proteiner, till exempel kortikosteroidbindande globulin och lipid-lipoprotein-fraktioner, parametrar för kolhydratmetabolism och parametrar för koagulation och fibrinolys. Förändringarna ligger vanligtvis inom normala laboratorievärden. Genom sin svagt anti-mineralkortikoida aktivitet medför drospirenon en ökad aktivitet hos plasma-renin och plasma-aldosteron.
Graviditet
Graviditet
Estron skall inte användas under graviditet.
Om graviditet inträffar under användning av Estron skall behandlingen omedelbart avslutas. Omfattande epidemiologiska studier har inte visat på en förhöjd risk för medfödda missbildningar hos barn födda av kvinnor som använde kombinerade p-piller före graviditet, inte heller på fosterskadande effekter när kombinerade p-piller oavsiktligt användes under graviditeten.
Djurstudier har visat biverkningar under graviditet och amning (se avsnitt Prekliniska uppgifter). Baserat på data från djurstudier kan biverkningar på grund av hormonell verkan av de aktiva substanserna inte uteslutas. Risken för biverkningar för människa bedöms som liten grundat på erfarenhet av användning av kombinerade p-piller under graviditet.
Tillgängliga data från användning av Estron under graviditet är för begränsade för att några slutsatser skall kunna göras avseende eventuellt negativa effekter av Estron på graviditet eller på fostrets eller den nyföddas hälsa. Tillförlitliga epidemiologiska data från behandling av gravida kvinnor med Estron saknas hittills.
Den ökade risken för VTE under postpartumperioden ska beaktas vid återinsättning av Estron (se avsnitt Dosering och Varningar och försiktighet).
Amning
Amningen kan påverkas av kombinerade p-piller eftersom dessa kan reducera mängden och ändra sammansättningen på mjölken. Därför bör användning av kombinerade p-piller vanligtvis inte rekommenderas förrän kvinnan slutat amma. Små mängder av hormonerna och/eller deras metaboliter kan utsöndras i bröstmjölken vid användning av kombinerade p-piller. Dessa mängder kan påverka barnet.
Trafik
Inga studier har gjorts där påverkan på förmågan att framföra fordon och använda maskiner studerats. Inga effekter på förmågan att köra och använda maskiner har observerats hos användare av kombinerade p-piller.
Biverkningar
För allvarliga biverkningar hos användare av kombinerade p-piller, se avsnitt Varningar och försiktighet.
Följande biverkningar har rapporterats vid användning av Estron.
Tabellen nedan rapporterar biverkningar efter MedDRA organsystem klassificering. Biverkningfrekvenserna är baserade på data från kliniska studier.
|
Organsystem |
Biverkningsfrekvens | |||
|---|---|---|---|---|
|
Vanliga ≥1/100, <1/10 |
Mindre vanliga ≥1/1 000, < 1/100 |
Sällsynta ≥1/10 000, <1/1 000 |
Ingen känd frekvens kan inte beräknas från tillgängliga data |
|
|
Infektioner och infestationer |
Candidiasis Herpes simplex | |||
|
Immunsystemet |
Allergiska reaktioner |
Astma |
Förvärrade symtom av ärftligt eller förvärvat angioödem. |
|
|
Metabolism och nutrition |
Ökad aptit | |||
|
Psykiska störningar |
Emotionell instabilitet |
Depression Nervositet Sömnrubbningar | ||
|
Centrala och perifera nervsystemet |
Huvudvärk |
Parestesier Vertigo | ||
|
Ögon |
|
Synrubbningar |
| |
|
Öron och balansorgan |
Hypakusi | |||
|
Hjärtat |
Extraslag Takykardi | |||
|
Blodkärl |
Lungemboli Hypertension Hypotension Migrän, Åderbråck |
Venös tromboembolism (VTE) Arteriell tromboembolism (ATE) | ||
|
Andningsvägar, bröstkorg och mediastinum |
Faryngit | |||
|
Magtarmkanalen |
Buksmärta |
Illamående Kräkning Gastroenterit Diarré Förstoppning Gastrointestinala besvär | ||
|
Hud och subkutan vävnad |
Acne |
Angioödem Alopeci Eksem Klåda Utslag Torr hud Seborré Hudåkommor |
Erytema nodosum Erytema multiforme | |
|
Muskuloskeletala systemet och bindväv |
Nacksmärta Smärta i extremiteter Muskelkramper | |||
|
Njurar och urinvägar |
Cystit | |||
|
Reproduktionsorgan och bröstkörtel |
Smärta i brösten Bröstförstoring Ömmande bröst Dysmenoré Metrorragi |
Brösttumörer Bröstcystor Laktation Ovarialcystor Blodvallning Menstruella besvär Amenorré Menorragi Vaginal candidiasis Vaginit Vaginal flytning Vulvovaginala besvär Vaginal torrhet Bäckensmärta Misstänkta vaginalutstryck Minskad libido | ||
|
Allmänna symtom och/eller symtom vid administrerings-stället |
Ödem Asteni Smärta Svår törst Ökad svettning | |||
|
Undersökningar |
Viktökning |
Viktminskning | ||
Den lämpligaste MedDRA termen används för att beskriva en viss biverkning och dess synonymer och relaterade tillstånd.
Beskrivning av utvalda biverkningar
En ökad risk för arteriella och venösa trombotiska och trombemboliska händelser, t.ex. myokardiell infarkt, stroke, transitoriska ischemiska attacker, venös trombos och lungemboli har observerats hos kvinnor som använder kombinerade hormonella preventivmedel, vilket diskuteras mer i detalj i avsnitt Varningar och försiktighet.
Följande biverkningar har rapporterats hos användare av kombinerade p-piller, se text under avsnitt Varningar och försiktighet:
• Venösa tromboemboliska sjukdomar;
• Arteriella tromboemboliska sjukdomar;
• Högt blodtryck;
• Levertumörer;
• Förekomst eller försämring av tillstånd där ett samband med användning av kombinerade p-piller inte är säkerställt: Crohns sjukdom, ulcerativ kolit, epilepsi, uterint myom, porfyri, systemisk lupus erythematosus, herpes gestationis, Sydenhams chorea, hemolytisk uremiskt syndrom, kolestasisk gulsot;
• Kloasma;
• Akut eller kroniskt nedsatt leverfunktion kan göra det nödvändigt att avbryta behandlingen med kombinerade p-piller tills värdena i leverfunktionstester åter är normala;
Frekvensen av diagnosticerad bröstcancer är något ökad bland användare av kombinerade p-piller. Eftersom bröstcancer är sällsynt hos kvinnor under 40 år är denna ökning av antalet fall liten jämfört med den totala risken att drabbas av bröstcancer. Sambandet med användning av kombinerade p-piller är okänt. För ytterligare information, se avsnitten Kontraindikationer samt 4.4.
Interaktioner
Genombrottsblödningar och/eller utebliven preventiv effekt kan bli följden av interaktioner med andra läkemedel (enzyminducerare) och p-piller (se avsnitt Interaktioner)
Överdosering
Det finns hittills inga erfarenheter från överdosering med Estron. Baserat på allmänna erfarenheter av orala kombinations p-piller, är de symtom som kan tänkas uppträda vid överdos av aktiva tabletter: illamående, kräkningar samt, bortfallsblödning. Bortfallsblödning kan även ske hos flickor före den första menstruationen, om de av misstag tagit läkemedlet. Det finns ingen antidot och behandling bör vara symtomatisk.
Farmakodynamik
Pearl-index för metodmisslyckande: 0,11 (övre tvåsidig 95% konfidensgräns: 0,60).
Övergripande pearl-index (metodmisslyckande + patientmisslyckande): 0,31 (övre tvåsidig 95% konfidensgräns: 0,91)
Verkningsmekanism
Den preventiva effekten av Estron baseras på ett samspel av olika faktorer, av vilka de viktigaste är ovalutionshämning och förändringarna i endometriet.
Farmakodynamiska effekter
Estron är ett oralt kombinerat preventivmedel innehållande etinylestradiol och gestagenet drospirenon. Vid terapeutisk dosering har drospirenon också antiandrogena och svagt antimineralkortikoida egenskaper, men inga östrogena, glukokortikoida eller antiglukokortikoida egenskaper. Detta ger drospirenon en farmakologisk profil som i mycket liknar det naturliga hormonet progesteron.
Resultat från kliniska studier tyder på att Estron har en svagt antimineralkortikoid effekt.
Farmakokinetik
Drospirenon
Absorption
Drospirenon som administreras oralt absorberas snabbt och nästan fullständigt. Efter en engångsdos uppnås maximala serumnivåer av den aktiva substansen på ca 38 ng/ml inom 1-2 timmar efter intag. Biotillgängligheten är mellan 76 och 85%. Biotillgängligheten av drospirenon påverkas ej av samtidigt födointag.
Distribution
Efter oral tillförsel minskar drospirenonnivåerna i serum med en slutlig halveringstid på 31 timmar. Drospirenon binds till serumalbumin och binder varken till SHBG (sex hormone binding globulin) eller CBG (corticoid binding globulin). Endast 3 - 5% av de totala koncentrationerna av aktiv substans i serum är fritt. Den etinylestradiolinducerade ökningen av SHBG påverkar inte bindningen av drospirenon till serumprotein. Den genomsnittliga skenbara distributionsvolymen för drospirenon är 3,7 ±1,2 l/kg.
Metabolism
Drospirenon metaboliseras nästan fullständigt efter oral administrering. De stora metaboliterna i plasma är drospirenon i syreform, som bildas av att laktonringen öppnas, och 4,5-dihydro-drospirenon-3-sulfat, bildad genom reduktion och efterföljande sulfatisering. Drospirenon kan också genomgå oxidativ metabolism katalyserad av CYP3A4.
Drospirenon är in vitro kapabel att hämma cytokrom P450 enzymerna CYP1A1, CYP2C9, CYP2C19 och CYP3A4 svagt till måttligt.
Eliminering
Clearance för drospirenon i serum är 1,5 ± 0,2 ml/min/kg. Endast spårmängder av drospirenon utsöndras i oförändrad form. Metaboliterna av drospirenon utsöndras i feces och urinen i förhållandet ca 1,2 till 1,4. Halveringstiden för utsöndringen av metaboliter via urin och feces är ca 40 timmar.
Steady state
Under behandlingscykeln uppnås de maximala jämviktskoncentrationerna för drospirenon i serum på ca 70 ng/ml efter cirka 8 dagars behandling. Nivåerna av drospirenon i serum ackumulerades med en faktor på ca 3 till följd av förhållandet mellan terminal halveringstid och doseringsintervall.
Särskilda patientgrupper
Effekter vid nedsatt njurfunktion
Hos kvinnor med lätt nedsatt njurfunktion (kreatinclearance CLcr, 50-80 ml/min) var steady-state serumkoncentration av drospirenon jämförbar med den hos kvinnor med normal njurfunktion. Serumkoncentrationen av drospirenon var i genomsnitt 37% högre hos kvinnor med måttligt nedsatt njurfunktion (CLcr, 30-50 ml/min) jämfört med den hos kvinnor med normal njurfunktion. Behandling med drospirenon tolererades väl av kvinnor med mild och måttligt nedsatt njurfunktion. Drospirenonbehandlingen visade inte på någon kliniskt signifikant påverkan på koncentrationen av serumkalium.
Effekt vid nedsatt leverfunktion
I en singeldosstudie minskade oral clearance (CL/F) med ungefär 50% hos försökspersoner med måttligt nedsatt leverfunktion jämfört med personer med normal leverfunktion. Den observerade minskningen av drospirenonclearance hos försökspersoner med måttligt nedsatt leverfunktion medför uppenbarligen ingen skillnad i serumkoncentration av kalium. Även vid diabetes och samtidig behandling med spironolakton (två faktorer vilka kan predisponera för hyperkalemi hos patienter) kunde inte någon ökning av serumkoncentrationen av kalium till den övre normalgränsen konstateras. Det kan konkluderas att drospirenon tolereras väl hos patienter med mild eller måttligt nedsatt leverfunktion (Child-Pugh B).
Etniska grupper
Inga kliniskt relevanta skillnader i farmakokinetiken av drospirenon eller etinylestradiol har observerats mellan japanska eller kaukasiska kvinnor.
Etinylestradiol
Absorption
Etinylestradiol absorberas snabbt och fullständigt efter oralt intag. Efter ett intag av en peroral engångdos uppnås maximal plasmakoncentration 33 pg/ml efter 1-2 timmar. Den absoluta biotillgängligheten är, beroende på presystemisk konjugering och first-pass metabolism ca 60%. Samtidigt intag av föda reducerade biotillgängligheten av etinylestradiol med omkring 25% hos de undersökta personerna medan denna förändring ej kunde ses hos andra.
Distribution
Koncentrationen av serumetinylestradiol minskar i två faser, där den terminala distributionsfasen karaktäriseras av en halveringstid på 24 timmar. Etinylestradiol är i hög grad, men icke specifikt, bundet till plasmaproteiner (ca 98%). Etinylestradiol inducerar en ökning av plasmakoncentrationen av SHBG och Corticoid Binding Globulin (CBG). Etinylestradiol har en skenbar distributionsvolym på 5 l/kg.
Metabolism
Etinylestradiol genomgår en betydande första passage metabolism i mag-tarmkanalen och i levern.
Etinylestradiol metaboliseras primärt genom aromatisk hydroxylering, men ett stort antal olika hydroxylerade och metylerade metaboliter bildas, och dessa finns närvarande som fria metaboliter och som konjugationer med glukoronider och sulfat. Metabolisk elimineringshastighet för etinylestradiol är cirka 5 ml/min/kg.
Etinylestradiol är in vitro en reversibel hämmare av CYP2C19, CYP1A1 och CYP1A2 samt även en mekanismbaserad hämmare av CYP3A4/5, CYP2C8 och CYP2J2.
Eliminering
Etinylestradiol utsöndras inte i oförändrad form i någon större omfattning. Metaboliterna av etinylestradiol utsöndras i urin och galla i förhållandet 4:6. Halveringstiden för utsöndringen är ca 1 dag.
Steady state
Jämvikt uppnås under andra hälften av en behandlingscykel och serumnivåerna för etinylestradiol ackumuleras med en faktor av ca 2,0 till 2,3.
Prekliniska uppgifter
Effekterna av drospirenon och etinylestradiol hos laboratoriedjur begränsade sig till de som har samband med känd farmakologisk verkan. Reproduktionstoxikologiska studier visade på embryo- och fostertoxicitet hos djur vilka anses artspecifika. Vid exponering för halter vilka överstiger de som uppnås av Estron -användare, observerades effekter på differentiering av fortplantningsorganen hos råtta men inte hos apa.
Miljöriskbedömningsstudier har visat att etinylestradiol och drospirenon kan utgöra en risk mot vattenmiljön (se avsnitt Särskilda anvisningar för destruktion.).
Innehåll
Kvalitativ och kvantitativ sammansättning
Rosa tabletter (innehåller aktiv substans):
Varje filmdragerad tablett innehåller 0,02 mg etinylestradiol och 3 mg drospirenon.
Hjälpämnen med känd effekt: Varje filmdragerad tablett innehåller 44 mg laktosmonohydrat.
Vita tabletter (placebotabletter):
Tabletten innehåller inga aktiva substanser.
Hjälpämnen med känd effekt: Varje filmdragerad tablett innehåller 89,5 mg laktos.
För fullständig förteckning över hjälpämnen se Innehåll.
Förteckning över hjälpämnen
Aktiva tabletter (rosa):
Tablettkärna:
Laktosmonohydrat
Stärkelse, pregelatiniserad (majs)
Povidon
Kroskarmellosnatrium
Polysorbat 80
Magnesiumstearat
Tablettdragering:
Delvis hydrolyserad polyvinylkohol
Titandioxid (E 171)
Macrogol 3350
Talk
Gul järnoxid (E 172)
Röd järnoxid (E 172)
Svart järnoxid (E172)
Placebotabletter (vita tabletter):
Tablettkärna:
Vattenfri laktos
Povidon
Magnesiumstearat
Tablettdragering:
Delvis hydrolyserad polyvinylkohol
Titandioxid (E 171)
Macrogol 3350
Talk
Hållbarhet, förvaring och hantering
Hållbarhet
3 år
Särskilda förvaringsanvisningar
Inga särskilda förvaringsanvisningar
Särskilda anvisningar för destruktion
Detta läkemedel kan utgöra en risk mot miljön (se avsnitt Prekliniska uppgifter).
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Egenskaper hos läkemedelsformen
Filmdragerad tablett.
Tablett med aktiv substans: Rosa, runda filmdragerade tabletter.
Placebotabletter: Vita, runda filmdragerade tabletter.




