Indikationer
Vidaza är indicerat för behandling av vuxna patienter, som ej är lämpliga för hematopoetisk stamcellstransplantation (HSCT), med:
-
myelodysplastiskt syndrom (MDS) klassificerat som intermediär-2-risk eller högrisk enligt IPSS (International Prognostic Scoring System),
-
kronisk myelomonocytär leukemi (CMML) med 10–29% benmärgsblaster utan myeloproliferativ sjukdom,
-
akut myeloid leukemi (AML) med 20–30% benmärgsblaster och multilinjär dysplasi, enligt Världshälsoorganisationens (WHO) klassificering,
-
AML med > 30% benmärgsblaster enligt WHO:s klassificering.
Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt Innehåll
Framskridna maligna levertumörer (se avsnitt Varningar och försiktighet).
Amning (se avsnitt Graviditet).
Dosering
Behandling med Vidaza ska initieras och övervakas under överinseende av läkare med erfarenhet av användningen av kemoterapeutiska medel. Patienter ska förmedicineras med antiemetika för illamående och kräkning.
Dosering
För alla patienter, oavsett hematologiska laboratorievärden vid baseline, är den rekommenderade startdosen i den första behandlingscykeln 75 mg/m2 kroppsyta, injicerad subkutant dagligen i 7 dagar följt av en viloperiod om 21 dagar (28-dagars behandlingscykel).
Det rekommenderas att patienter behandlas i minst 6 cykler. Behandling ska pågå så länge som patienten har nytta av den eller fram till sjukdomsprogression.
Patienter ska övervakas med avseende på hematologiskt svar/toxicitet och njurtoxiciteter (se avsnitt Varningar och försiktighet); det kan bli nödvändigt att skjuta upp påbörjandet av nästa cykel eller minska dosen enligt beskrivning nedan.
Vidaza ska inte användas omväxlande med oralt azacitidin. Dosering- och schemarekommendationer för oralt azacitidin skiljer sig från injicerbart azacitidin på grund av skillnader i exponering. Det rekommenderas att hälso- och sjukvårdspersonal verifierar läkemedlets namn, dos samt administreringsväg.
Laboratorievärden
Leverfunktionsvärden, serumkreatinin och serumbikarbonat ska bestämmas innan behandling sätts in och före varje behandlingscykel. Fullständig blodkroppsräkning ska göras innan behandling inleds och efter behov, men åtminstone före varje behandlingscykel för att övervaka svar och toxicitet.
Dosjustering på grund av hematologisk toxicitet
Hematologisk toxicitet föreligger när det lägsta värdet (nadir) under en viss cykel för trombocyttalet sjunker ≤ 50,0 x 109/l och/eller nadir för det absoluta neutrofiltalet (absolute neutrophil count, ANC) sjunker ≤ 1 x 109/l.
Återhämtning definieras som en ökning av den/de celllinje(r) för vilka hematologisk toxicitet observerades till nadirvärdet plus minst hälften av den absoluta skillnaden mellan nadir och baselinevärdet (dvs. återhämtning av blodkroppsvärden ≥ nadirvärdet + (0,5 x [| baselinevärdet – nadirvärdet |]).
Patienter utan sänkta blodkroppsvärden vid baseline (dvs. vita blodkroppar (White Blood Cells, WBC) ≥ 3,0 x 109/l och ANC ≥ 1,5 x 109/l och trombocyter ≥ 75,0 x 109/l) före den första behandlingen
Om hematologisk toxicitet observeras efter behandling med Vidaza ska nästa behandlingscykel skjutas upp tills dess att trombocyttalet och ANC har återhämtat sig. Om återhämtning uppnås inom 14 dagar behövs ingen dosjustering. Om återhämtning inte har uppnåtts inom 14 dagar, ska dosen sänkas enligt följande tabell. Efter dosändring ska cykelns duration återgå till 28 dagar.
|
Cykel, nadirvärde |
Dos under nästa cykel, om återhämtning* inte uppnås inom 14 dagar (%) |
|
|---|---|---|
|
ANC (x 109/l) |
Trombocyter (x 109/l) |
|
|
≤ 1,0 |
≤ 50,0 |
50% |
|
> 1,0 |
> 50,0 |
100% |
*Återhämtning = värde ≥ nadirvärdet + (0,5 x [baselinevärdet – nadirvärdet])
Patienter med sänkta blodkroppsvärden vid baseline (dvs. WBC < 3,0 x 109/l, ANC < 1,5 x 109/l, eller trombocyter < 75,0 x 109/l) före den första behandlingen
Nästa cykel ska inte skjutas upp och ingen dosjustering göras om sänkningen av WBC eller ANC eller trombocyttalet efter behandling med Vidaza, jämfört med värdena före behandling, är ≤ 50%, eller större än 50% men med en förbättring av differentieringen i någon cellinje.
Om sänkningen av WBC eller ANC eller trombocyter är större än 50% av värdet före behandling utan någon förbättring av differentieringen i någon cellinje, ska nästa behandlingscykel med Vidaza skjutas upp tills dess att trombocyttalet och ANC har återhämtat sig. Om återhämtning uppnås inom 14 dagar behövs ingen dosjustering. Om återhämtning inte har uppnåtts inom 14 dagar, ska benmärgens cellularitet bestämmas. Om benmärgens cellularitet är > 50%, ska ingen dosjustering göras. Om benmärgens cellularitet är ≤ 50%, ska behandlingen skjutas upp och dosen sänkas enligt följande tabell:
|
Benmärgens cellularitet |
Dos under nästa cykel om återhämtning inte uppnås inom 14 dagar (%) |
|
|---|---|---|
|
Återhämtning* ≤ 21 dagar |
Återhämtning* > 21 dagar |
|
|
15-50% |
100% |
50% |
|
< 15% |
100% |
33% |
*Återhämtning = värde ≥ nadirvärdet + (0,5 x [baselinevärdet – nadirvärdet])
Efter dosändring ska nästa cykels duration återgå till 28 dagar.
Särskilda populationer
Äldre personer
Inga särskilda dosjusteringar rekommenderas för äldre. Eftersom det är troligare att äldre patienter har nedsatt njurfunktion, kan det vara bra att kontrollera njurfunktionen.
Patienter med nedsatt njurfunktion
Azacitidin kan ges till patienter med nedsatt njurfunktion utan initial dosjustering (se avsnitt Farmakokinetik). Om serumbikarbonat utan förklaring sjunker till under 20 mmol/l, ska dosen sänkas med 50% vid nästa cykel. Om serumkreatinin eller blodureakväve (BUN) utan förklaring stiger till ≥ 2 gånger högre än baselinevärdet och högre än övre normalgräns (ULN), ska nästa cykel skjutas upp till dess att värdena har återgått till det normala, eller baselinevärdet, och dosen ska sänkas med 50% vid nästa behandlingscykel (se avsnitt Varningar och försiktighet).
Patienter med nedsatt leverfunktion
Inga formella studier har utförts på patienter med nedsatt leverfunktion (se avsnitt Varningar och försiktighet). Patienter med gravt nedsatt leverfunktion ska övervakas noga med avseende på biverkningar. Inga särskilda ändringar av startdosen rekommenderas för patienter med nedsatt leverfunktion före behandlingsstart; efterföljande dosändringar ska baseras på hematologiska laboratorievärden. Vidaza är kontraindicerat hos patienter med framskridna maligna levertumörer (se avsnitt Kontraindikationer och Varningar och försiktighet).
Pediatrisk population
Säkerhet och effekt för Vidaza för barn i åldern 0–17 år har ännu inte fastställts. För närvarande tillgänglig information finns i avsnitt Biverkningar, Farmakodynamik och Farmakokinetik, men ingen doseringsrekommendation kan fastställas.
Administreringssätt
Berett Vidaza ska injiceras subkutant i överarmen, låret eller buken. Injektionsstället ska roteras. Nya injektioner ska ges minst 2,5 cm från det tidigare injektionsstället och aldrig i områden där stället ömmar eller där blåmärken, rodnad eller förhårdnad föreligger.
Suspensionen ska inte filtreras efter beredning. Anvisningar om beredning av läkemedlet före administrering finns i avsnitt Hållbarhet, förvaring och hantering.
Varningar och försiktighet
Hematologisk toxicitet
Behandling med azacitidin är förenad med anemi, neutropeni och trombocytopeni, särskilt under de första två cyklerna (se avsnitt Biverkningar). Fullständig blodkroppsräkning ska göras efter behov, men åtminstone före varje behandlingscykel för att övervaka svar och toxicitet. Efter administrering av den rekommenderade dosen i den första cykeln ska dosen för efterföljande cykler sänkas eller administreringen skjutas upp baserat på nadirvärden och hematologiskt svar (se avsnitt Dosering). Patienterna ska uppmanas att omedelbart rapportera feberepisoder. Patienter och läkare uppmanas också att vara observanta på tecken och symtom på blödning.
Nedsatt leverfunktion
Inga formella studier har utförts på patienter med nedsatt leverfunktion. Progredierande leverkoma och död har rapporterats under behandling med azacitidin hos patienter med omfattande tumörbörda på grund av metastaserande sjukdom, i synnerhet hos patienter med baselinealbumin i serum < 30 g/l. Azacitidin är kontraindicerat hos patienter med framskridna maligna levertumörer (se avsnitt Kontraindikationer).
Nedsatt njurfunktion
Njurabnormiteter, från förhöjt serumkreatinin till njursvikt och död, har rapporterats hos patienter som behandlats med intravenöst azacitidin i kombination med andra kemoterapeutiska medel. Hos 5 försökspersoner med kronisk myeloisk leukemi (KML) som behandlades med azacitidin och etoposid utvecklades dessutom renal tubulär acidos, definierad som en sänkning av serumbikarbonat till < 20 mmol/l med alkalisk urin och hypokalemi (serumkalium < 3 mmol/l). Om serumbikarbonat sjunker utan förklaring (< 20 mmol/l) eller om serumkreatinin eller BUN stiger, ska dosen sänkas eller administreringen skjutas upp (se avsnitt Dosering).
Patienter ska uppmanas att omedelbart rapportera oliguri och anuri till läkaren.
Även om inga kliniskt relevanta skillnader i biverkningsfrekvensen noterades mellan försökspersoner med normal njurfunktion jämfört med dem med nedsatt njurfunktion, ska patienter med nedsatt njurfunktion övervakas noga med avseende på toxicitet eftersom azacitidin och/eller dess metaboliter huvudsakligen utsöndras via njurarna (se avsnitt Dosering).
Laboratorievärden
Leverfunktionsvärden, serumkreatinin och serumbikarbonat ska bestämmas innan behandling sätts in och före varje behandlingscykel. Fullständig blodkroppsräkning ska göras innan behandling inleds och efter behov, men åtminstone före varje behandlingscykel för att övervaka svar och toxicitet, se även avsnitt Biverkningar.
Hjärt- och lungsjukdom
Patienter med grav kongestiv hjärtsvikt, kliniskt instabil hjärtsjukdom eller lungsjukdom i anamnesen uteslöts från de pivotala registreringsstudierna (AZA PH GL 2003 CL 001 och AZA-AML-001) och således har azacitidins säkerhet och effekt hos dessa patienter inte fastställts. Nya data från en klinisk studie på patienter med känd anamnes på hjärt- eller lungsjukdom visade en signifikant ökad förekomst av hjärthändelser med azacitidin (se avsnitt Biverkningar). Det rekommenderas därför att försiktighet iakttas vid förskrivning av azacitidin till dessa patienter. Utvärdering av hjärta och lungor före och under behandlingen bör övervägas.
Nekrotiserande fasciit
Nekrotiserande fasciit, inklusive fatala fall, har rapporterats hos patienter som behandlats med Vidaza. Behandling med Vidaza ska avbrytas hos patienter som utvecklar nekrotiserande fasciit och lämplig behandling ska omedelbart påbörjas.
Tumörlyssyndrom
De patienter som löper risk att utveckla tumörlyssyndrom är de med stor tumörbörda före behandlingen. Dessa patienter ska övervakas noga och lämpliga försiktighetsåtgärder vidtas.
Differentieringssyndrom
Fall av differentieringssyndrom (även kallat retinoidsyrasyndrom) har rapporterats hos patienter som fått injicerbart azacitidin. Differentieringssyndrom kan ha dödlig utgång, och symtom och kliniska fynd inkluderar dyspné, lunginfiltrat, feber, utslag, lungödem, perifert ödem, snabb viktuppgång, pleurautgjutningar, perikardiella utgjutningar, hypotoni och nedsatt njurfunktion (se avsnitt Biverkningar). Behandling med kortikosteroider intravenöst i höga doser och hemodynamisk övervakning ska övervägas vid första symtom eller tecken som tyder på differentieringssyndrom. Tillfällig utsättning av injicerbart azacitidin ska övervägas tills symtomen har gått tillbaka och vid eventuell återinsättning ska försiktighet iakttas.
Interaktioner
Baserat på in vitro-data förefaller metabolismen av azacitidin inte medieras av cytokrom P450-isoenzymer (CYP:er), UDP-glukuronosyltransferaser (UGT:er), sulfotransferaser (SULT:er) eller glutationtransferaser (GST:er); interaktioner relaterade till dessa metaboliserande enzymer in vivo anses därför osannolika.
Det är inte troligt att azacitidin har några kliniska signifikant hämmande eller inducerande effekter på cytokrom P450-enzymer (se avsnitt Farmakokinetik).
Inga formella kliniska interaktionsstudier med azatidicin har utförts.
Graviditet
Fertila kvinnor/Födelsekontroll hos män och kvinnor
Fertila kvinnor måste använda effektiv preventivmetod under och minst 6 månader efter behandling. Män ska uppmanas att inte avla barn under behandlingen och måste använda en effektiv preventivmetod under och minst 3 månader efter behandling.
Graviditet
Adekvata data från behandling av gravida kvinnor med azacitidin saknas. Studier på mus har visat reproduktionstoxikologiska effekter (se avsnitt Prekliniska uppgifter). Risken för människa är okänd. Baserat på resultat från djurstudier och verkningsmekanismen bör azacitidin inte användas under graviditet, särskilt inte under första trimestern, om det inte är klart nödvändigt. I varje enskilt fall ska nyttan med behandlingen vägas mot den möjliga risken för fostret.
Amning
Det är inte känt om azacitidin/metaboliter utsöndras i bröstmjölk. På grund avpotentiella allvarliga biverkningar hos det ammade barnet är amning kontraindicerad under behandling med azacitidin.
Fertilitet
Det finns inga data om azacitidins effekt på fertiliteten hos människa. Biverkningar av azacitidin på hanars fertilitet har dokumenterats i djurförsök (se avsnitt Prekliniska uppgifter). Manliga patienter ska uppmanas att före behandlingsstart söka rådgivning beträffande lagring av sperma.
Trafik
Azacitidin har mindre eller måttlig effekt på förmågan att framföra fordon och använda maskiner. Trötthet har rapporteras vid användning av azacitidin. Därför rekommenderas försiktighet vid framförande av fordon eller användning av maskiner.
Biverkningar
Sammanfattning av säkerhetsprofilen
Vuxen population med MDS, CMML och AML (20–30% benmärgsblaster)
Biverkningar som anses vara möjligen eller troligen relaterade till administreringen av Vidaza har förekommit hos 97% av patienterna.
De vanligaste allvarliga biverkningarna som observerades i den pivotala studien (AZA PH GL 2003 CL 001) inbegrep febril neutropeni (8,0%) och anemi (2,3%), vilket även rapporterades i de understödjande studierna (CALGB 9221 och CALGB 8921). Andra allvarliga biverkningar från dessa 3 studier inkluderade infektioner som neutropen sepsis (0,8%) och pneumoni (2,5%) (i vissa fall med dödlig utgång), trombocytopeni (3,5%), överkänslighetsreaktioner (0,25%) och blödningar (t.ex. cerebral blödning [0,5%], gastrointestinal blödning [0,8%] och intrakraniell blödning [0,5%]).
De vanligast rapporterade biverkningarna vid azacitidinbehandling var hematologiska reaktioner (71,4%) däribland trombocytopeni, neutropeni och leukopeni (vanligen grad 3–4), gastrointestinala händelser (60,6%) däribland illamående, kräkning (vanligen grad 1–2) och reaktioner vid injektionsstället (77,1%; vanligen grad 1–2).
Vuxen population i åldern 65 år eller äldre med AML med > 30% benmärgsblaster
De vanligaste allvarliga biverkningarna (≥ 10%) som observerades i AZA-AML-001 inom azacitidinbehandlingsarmen inbegrep febril neutropeni (25,0%), pneumoni (20,3%) och pyrexi (10,6%). Andra mindre ofta rapporterade allvarliga biverkningar i azacitidinbehandlingsarmen inbegrep sepsis (5,1%), anemi (4,2%), neutropen sepsis (3,0%), urinvägsinfektion (3,0%), trombocytopeni (2,5%), neutropeni (2,1%), cellulit (2,1%), yrsel (2,1%) och dyspné (2,1%).
De vanligast rapporterade biverkningarna (≥ 30%) vid azacitidinbehandling var gastrointestinala händelser, inklusive förstoppning (41,9%), illamående (38,9%) och diarré (36,9%; vanligen grad 1–2), allmänna symtom och/eller symtom vid administreringsstället inklusive pyrexi (37,7%) (vanligen grad 1–2) och hematologiska händelser, inklusive febril neutropeni (32,2%) och neutropeni (30,1%; vanligen grad 3–4).
Biverkningslista i tabellform
Tabell 1 nedan innehåller biverkningar, förenade med azacitidinbehandling, vilka har setts i de kliniska huvudstudierna för MDS och AML och vid uppföljning efter godkännande.
Frekvenserna definieras som: mycket vanliga (≥ 1/10), vanliga (≥ 1/100, < 1/10), mindre vanliga (≥ 1/1 000, < 1/100), sällsynta (≥ 1/10 000, < 1/1 000), mycket sällsynta (< 1/10 000), ingen känd frekvens (kan inte beräknas från tillgängliga data). Biverkningarna presenteras inom varje frekvensområde efter fallande allvarlighetsgrad. Biverkningar presenteras i tabellen nedan enligt den högsta frekvensen som observerats i någon av de kliniska huvudstudierna.
Tabell 1: Biverkningar som rapporterats hos patienter med MDS eller AML som behandlats med azacitidin (kliniska studier och efter godkännandet)
|
Organsystemklass |
Mycket vanliga |
Vanliga |
Mindre vanliga |
Sällsynta |
Ingen känd frekvens |
|---|---|---|---|---|---|
|
Infektioner och infestationer |
pneumoni*, (inklusive bakteriell, viral och fungös), nasofaryngit |
sepsis* (inklusive bakteriell, viral och fungös), neutropen sepsis*, luftvägsinfektion (inkluderar övre och bronkit), urinvägsinfektion, cellulit, divertikulit, oral svampinfektion, sinuit, faryngit, rinit, herpes simplex, hudinfektion |
nekrotiserande fasciit* |
||
|
Neoplasier; benigna, maligna och ospecificerade (samt cystor och polyper) |
differentieringssyndrom*,a |
||||
|
Blodet och lymfsystemet |
febril neutropeni*, neutropeni, leukopeni, trombocytopeni, anemi |
pancytopeni*, benmärgssvikt | |||
|
Immunsystemet |
överkänslighets-reaktioner | ||||
|
Metabolism och nutrition |
anorexi, nedsatt aptit, hypokalemi |
dehydrering |
tumörlyssyndrom | ||
|
Psykiska störningar |
insomni |
förvirringstillstånd, ångest | |||
|
Centrala och perifera nervsystemet |
yrsel, huvudvärk |
intrakraniell blödning*, synkope, somnolens, letargi | |||
|
Ögon |
ögonblödning, konjunktival blödning | ||||
|
Hjärtat |
|
Perikardiell effusion |
perikardit |
|
|
|
Blodkärl |
hypotoni*, hypertoni, ortostatisk hypotoni, hematom | ||||
|
Andningsvägar, bröstkorg och mediastinum |
dyspné, epistaxis |
pleuraeffusion, dyspné vid ansträngning, faryngolaryngeal smärta |
interstitiell lungsjukdom | ||
|
Magtarmkanalen |
diarré, kräkning, förstoppning, illamående, buksmärta (inkluderar övre och obehag i buken) |
gastrointestinal blödning* (inkluderar blödning i munnen), hemorrojdblödning, stomatit, gingival blödning, dyspepsi | |||
|
Lever och gallvägar |
leversvikt*, progredierande leverkoma | ||||
|
Hud och subkutan vävnad |
petekier, pruritus (inkluderar generaliserad), utslag, ecchymos |
purpura, alopeci, urtikaria, erytem, makulära utslag |
akut febril neutrofil dermatos, pyoderma gangrenosum |
kutan vaskulit |
|
|
Muskuloskeletala systemet och bindväv |
artralgi, muskuloskeletal smärta (inklusive smärta i rygg, skelett och extremitet) |
muskelspasmer, myalgi | |||
|
Njurar och urinvägar |
njursvikt*, hematuri, förhöjt serumkreatinin |
renal tubulär acidos | |||
|
Allmänna symtom och/eller symtom vid administreringsstället |
pyrexi*, trötthet, asteni, bröstsmärta, erytem vid injektionsstället, smärta vid injektionsstället, reaktion vid injektionsstället (ospecificerad) |
blåmärke, hematom, induration, utslag, pruritus, inflammation, missfärgning, knöl och blödning (vid injektionsstället), allmän sjukdomskänsla, frossa, blödning vid kateterstället |
nekros vid injektionsstället (vid injektionsstället) | ||
|
Undersökningar |
viktminskning |
|
* = fatal utgång har rapporterats i sällsynta fall
a= se avsnitt Varningar och försiktighet
Beskrivning av utvalda biverkningar
Hematologiska biverkningar
De vanligast rapporterade (≥ 10%) hematologiska biverkningarna i samband med azacitidinbehandling inkluderar anemi, trombocytopeni, neutropeni, febril neutropeni och leukopeni, som vanligen var av grad 3 eller 4. Risken är större att dessa händelser inträffar under de första 2 cyklerna, varefter de inträffar mindre ofta hos patienter med återställd hematologisk funktion. De flesta hematologiska biverkningarna hanterades med rutinkontroll med fullständig blodkroppsräkning och uppskjuten administrering av azacitidin under nästa cykel, profylaktiskt antibiotika och/eller stödbehandling med tillväxtfaktor (t.ex. G-CSF) för neutropeni och transfusioner för anemi eller trombocytopeni efter behov.
Infektioner
Myelosuppression kan leda till neutropeni och ökad infektionsrisk. Allvarliga biverkningar som sepsis, inklusive neutropen sepsis och pneumoni rapporterades hos patienter som fick azacitidin, i vissa fall med dödlig utgång. Infektioner kan behandlas med infektionsläkemedel plus stödbehandling med tillväxtfaktor (t.ex. G-CSF) för neutropeni.
Blödningar
Blödning kan förekomma hos patienter som får azacitidin. Allvarliga biverkningar som gastrointestinal blödning och intrakraniell blödning har rapporterats. Patienter ska övervakas för tecken och symtom på blödning, i synnerhet de med preexisterande eller behandlingsrelaterad trombocytopeni.
Överkänslighet
Allvarliga överkänslighetsreaktioner har rapporterats hos patienter som får azacitidin. I händelse av en anafylaxiliknande reaktion ska behandlingen med azacitidin omedelbart avbrytas och lämplig symtomatisk behandling sättas in.
Biverkningar i hud och subkutan vävnad
Biverkningar i magtarmkanalen
De vanligast rapporterade biverkningarna i magtarmkanalen i samband med azacitidinbehandling inbegrep förstoppning, diarré, illamående och kräkning. Dessa biverkningar behandlades symtomatiskt med antiemetika för illamående och kräkning, med antidiarroika mot diarré och med laxermedel och/eller avföringsuppmjukande medel för förstoppning.
Biverkningar i njurarna
Njurproblem från förhöjt serumkreatinin och hematuri till renal tubulär acidos, njursvikt och dödsfall har rapporterats hos patienter som behandlats med azacitidin (se avsnitt Varningar och försiktighet).
Biverkningar i levern
Patienter med omfattande tumörbörda på grund av metastassjukdom har rapporterats drabbas av leversvikt, progredierande leverkoma och dödsfall under behandling med azacitidin (se avsnitt Varningar och försiktighet).
Hjärthändelser
Data från en klinisk studie där rekrytering av patienter med känd anamnes på hjärt- eller lungsjukdom tilläts visade en ökning av hjärthändelser hos patienter med nyligen diagnostiserad AML som behandlades med azacitidin (se avsnitt Varningar och försiktighet).
Äldre population
Det finns begränsat med säkerhetsinformation tillgänglig med azacitidin för patienter ≥ 85 år (med 14 [5,9%] patienter ≥ 85 år som behandlats i studien AZA-AML-001).
Pediatrisk population
I studien AZA-JMML-001 behandlades 28 pediatriska patienter (ålder från 1 månad till yngre än 18 år) med Vidaza för MDS (n = 10) eller juvenil myelomonocytisk leukemi (JMML) (n = 18) (se avsnitt Farmakodynamik).
Alla 28 patienterna upplevde minst 1 biverkning och 17 (60,7%) upplevde minst en behandlingsrelaterad biverkning. De vanligaste rapporterade biverkningarna i den övergripande pediatriska populationen var pyrexi, hematologiska biverkningar inklusive anemi, trombocytopeni och febril neutropeni samt gastrointestinala biverkningar, inklusive förstoppning och kräkningar.
Tre (3) patienter upplevde en behandlingsutlöst biverkning som ledde till att läkemedlet sattes ut (pyrexi, sjukdomsprogression och buksmärta).
I studien AZA-AML-004 behandlades 7 pediatriska patienter (ålder från 2 till 12 år) med Vidaza för AML i molekylärt återfall efter första kompletta remissionen [CR1] (se avsnitt Farmakodynamik).
Alla 7 patienterna upplevde minst en behandlingsrelaterad biverkning. De vanligaste rapporterade biverkningarna var neutropeni, illamående, leukopeni, trombocytopeni, diarré och ökat alanin-aminotransaminas (ALAT). Två patienter upplevde en behandlingsrelaterad händelse som ledde till att läkemedlet sattes ut (febril neutropeni, neutropeni).
Inga nya säkerhetssignaler identifierades hos det begränsade antalet pediatriska patienter som behandlades med Vidaza under den kliniska studien. Den övergripande säkerhetsprofilen överensstämde med den vuxna populationens.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till Läkemedelsverket, men alla kan rapportera misstänkta biverkningar till Läkemedelsverket, www.lakemedelsverket.se. Postadress
Läkemedelsverket
Box 26
751 03 Uppsala
Överdosering
Ett fall av överdosering rapporterades under kliniska studier. En patient upplevde diarré, illamående och kräkning efter att ha fått en intravenös enkeldos om ca 290 mg/m2, nästan 4 gånger den rekommenderade startdosen.
I händelse av överdosering ska patienten övervakas med lämpliga blodkroppsräkningar, och ska ges understödjande behandling efter behov. Det finns ingen känd specifik antidot mot överdosering av azacitidin.
Farmakodynamik
Verkningsmekanism
Azacitidin anses utöva sina antineoplastiska effekter genom multipla mekanismer, däribland cytotoxicitet på abnorma hematopoetiska celler i benmärgen och hypometylering av DNA. Azacitidins cytotoxiska effekter kan vara resultatet av multipla mekanismer, däribland hämning av DNA-, RNA- och proteinsyntesen, inkorporering i RNA och DNA och aktivering av DNA-skadande vägar. Icke-prolifererande celler är relativt okänsliga för azacitidin. Inkorporering av azacitidin i DNA resulterar i inaktivering av DNA-metyltransferaser, vilket leder till hypometylering av DNA. DNA-hypometylering av avvikande metylerade gener som är involverade i normal cellcykelreglering, differentiering och dödsvägar kan resultera i återuttryck av gener och återställande av cancerhämmande funktioner i cancerceller. Den relativa betydelsen av DNA-hypometylering jämfört med cytotoxicitet eller azacitidins andra aktiviteter för kliniska resultat har inte fastställts.
Klinisk effekt och säkerhet
Vuxen population (MDS, CMML och AML [20–30% benmärgsblaster])
Vidazas effekt och säkerhet studerades i en internationell, kontrollerad, öppen, randomiserad jämförande fas 3-multicenterstudie med parallella grupper (AZA PH GL 2003 CL 001) på vuxna patienter med: MDS klassificerad som intermediär-2-risk eller högrisk enligt IPSS (International Prognostic Scoring System), refraktär anemi med överskott av blaster (refractory anaemia with excess blasts, RAEB), refraktär anemi med överskott av blaster i transformation (refractory anaemia with excess blasts in transformation, RAEB-T) och modifierad kronisk myelomonocytär leukemi (mCMML) enligt det fransk-amerikansk-brittiska (FAB) klassificeringssystemet. RAEB T-patienter (21-30% blaster) betraktas nu som patienter med AML enligt WHO:s nuvarande klassificeringssystem. Azacitidin plus bästa understödjande behandling (best supportive care, BSC) (n = 179) jämfördes med konventionella behandlingsregimer (conventional care regimens, CCR). CCR bestod av enbart BSC (n = 105), lågdos-cytarabin plus BSC (n = 49) eller induktionskemoterapi av standardtyp plus BSC (n = 25). Patienterna valdes av sina läkare i förväg ut till att få en av de tre CCR före randomiseringen. De patienter som inte randomiserades till Vidaza fick denna förvalda regim. I inklusionskriterierna ingick att patienterna måste ha en performance status på 0–2 enligt ECOG (Eastern Cooperative Oncology Group). Patienter med sekundärt MDS uteslöts från studien. Studiens primära effektmått var total överlevnad. Vidaza gavs som en subkutan dos om 75 mg/m2 dagligen i 7 dagar följt av en viloperiod om 21 dagar (28-dagars behandlingscykel) i ett medianantal cykler om 9 (intervall = 1–39) och ett genomsnittligt antal cykler om 10,2. I Intent to Treat-populationen (ITT) var medianålder 69 år (intervall 38–88 år).
ITT-analysen av 358 patienter (179 azacitidin och 179 CCR) visade att behandling med Vidaza var associerad med en medianöverlevnad på 24,46 månader jämfört med 15,02 månader för dem som fick en behandling med CCR, en skillnad om 9,4 månader med ett stratifierat log-rank p värde på 0,0001. Riskkvoten (Hazard ratio, HR) för denna behandlingseffekt var 0,58 (95% CI: 0,43; 0,77). Tvåårsöverlevnaden var 50,8% hos de patienter som fick azacitidin jämfört med 26,2% hos de patienter som fick CCR (p < 0,0001).
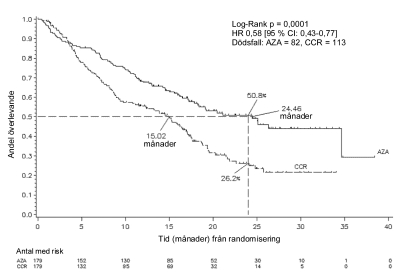
NYCKEL: AZA = azacitidin; CCR = conventional care regimens; CI = konfidensintervall; HR = hazard ratio
Vidazas överlevnadsnytta var konsekvent oavsett vilken CCR (enbart BSC, lågdos-cytarabin plus BSC eller induktionskemoterapi av standardtyp plus BSC) som användes i kontrollarmen.
Vid analys av IPSS cytogenetiska subgrupper observerades likartade fynd i alla grupper (bra, intermediär, bristfällig cytogenetik, inklusive monosomi 7) vad gäller medianvärdet för total överlevnad.
Vid analys av ålderssubgrupper observerades en ökning av medianvärdet för total överlevnad i alla grupper (< 65 år, ≥ 65 år och ≥ 75 år).
Behandling med Vidaza var förenad med en mediantid till död eller transformation till AML om 13,0 månader jämfört med 7,6 månader för dem som behandlades med CCR, en förbättring med 5,4 månader med ett stratifierat log-rank p värde på 0,0025. Behandling med Vidaza var också förenad med en minskning av cytopenier med tillhörande symtom. Behandling med Vidaza ledde till minskat behov av transfusioner av erytrocyter och trombocyter. Av de patienter i azacitidingruppen som var beroende av erytrocyttransfusioner vid baseline, blev 45,0% oberoende av erytrocyttransfusioner under behandlingsperioden, jämfört med 11,4% av patienterna i den samlade grupp som fick CCR (en statistiskt signifikant (p < 0,0001) skillnad om 33,6% (95% CI: 22,4; 44,6)). Hos patienter som var beroende av erytrocyttransfusioner vid baseline och som blev oberoende, var mediandurationen av oberoendet av erytrocyttransfusioner 13 månader i azacitidingruppen.
Behandlingssvaret bedömdes av prövaren eller av den oberoende granskningskommittén (Independent Review Committee, IRC). Det samlade behandlingssvaret (komplett svar + partiellt svar) var enligt prövarens bedömning 29% i azacitidingruppen och 12% i den samlade grupp som fick CCR (p = 0,0001). Enligt granskningskommitténs bedömning var det samlade behandlingssvaret (komplett svar + partiellt svar) i studien AZA PH GL 2003 CL 001 7% (12/179) i azacitidingruppen jämfört med 1% (2/179) i den samlade grupp som fick CCR (p = 0,0113). Skillnaden mellan granskningskommitténs och prövarens bedömningar av behandlingssvaret var en följd av International Working Group (IWG) kriterier, som kräver att perifera blodkroppsvärden ska förbättras och att förbättringarna ska kvarstå i minst 56 dagar. En överlevnadsnytta demonstrerades också hos patienter som inte hade uppnått ett fullständigt/partiellt svar efter azacitidinbehandling. Enligt granskningskommitténs bedömning uppnåddes hematologisk förbättring (större eller mindre) hos 49% av patienterna som fick azacitidin jämfört med 29% av de samlade patienterna som behandlades med CCR (p < 0,0001).
Hos patienter med en eller fler cytogenetiska abnormiteter vid baseline var procentandelen patienter med ett kraftigt cytogenetiskt svar likartad i azacitidingruppen och i grupperna som fick CCR. Svagare cytogenetiskt svar var statistiskt signifikant (p = 0,0015) högre i azacitidingruppen (34%) jämfört med den samlade grupp som fick CCR (10%).
Vuxen population i åldern 65 år eller äldre med AML med > 30% benmärgsblaster
Resultaten som visas nedan representerar intent-to-treat-populationen som undersöktes i AZA-AML-001 (se avsnitt Indikationer för den godkända indikationen).
Effekten och säkerheten för Vidaza studerades i en internationell, kontrollerad, öppen multicenterstudie i fas 3 med parallella grupper på patienter som var 65 år och äldre med nyligen diagnostiserad de novo eller sekundär AML med > 30% benmärgsblaster enligt WHO:s klassificering, som inte var lämpliga för HSCT. Vidaza plus BSC (n = 241) jämfördes med CCR. CCR bestod av enbart BSC (n = 45), låg dos av cytarabin plus BSC (n = 158), eller intensiv kemoterapi av standardtyp med cytarabin och antracyklin plus BSC (n = 44). Patienter valdes ut i förväg av sin läkare till en av de tre CCR-grupperna före randomisering. Patienter fick den förvalda regimen om de inte randomiserades till Vidaza. Som del av inklusionskriterierna måste patienterna ha ett ECOG-funktionsstatus på 0–2 och cytogenetiska avvikelser med intermediär risk eller ”poor risk”. Studiens primära effektmått var total överlevnad.
Vidaza administrerades som en subkutan dos på 75 mg/m2/dag i 7 dagar, följt av en viloperiod på 21 dagar (28 dagars behandlingscykel), under en median på 6 cykler (intervall: 1 till 28), patienter som enbart fick BSC under en median på 3 cykler (intervall: 1 till 20), patienter som fick låg dos av cytarabin under en median på 4 cykler (intervall: 1 till 25) och patienter som fick intensiv kemoterapi av standardtyp under en median på 2 cykler (intervall: 1 till 3, induktionscykel plus 1 eller 2 konsolideringscykler).
De individuella baseline-parametrarna var jämförbara mellan Vidaza- och CCR-grupperna. Medianåldern för patienterna var 75,0 år (intervall: 64 till 91 år), 75,2% var kaukasier och 59,0% var män. Vid baseline klassificerades 60,7% som AML utan närmare specifikation, 32,4% som AML med myelodysplasirelaterade förändringar, 4,1% som terapirelaterade myeloida neoplasmer och 2,9% som AML med återkommande genetiska avvikelser enligt WHO:s klassificering.
Vid ITT-analysen av 488 patienter (241 Vidaza och 247 CCR) associerades Vidaza-behandlingen med en medianöverlevnad på 10,4 månader mot 6,5 månader för patienter som fick CCR-behandling, en skillnad på 3,8 månader, med ett stratifierat log-rank p-värde på 0,1009 (tvåsidigt). Riskkvoten för behandlingseffekten var 0,85 (95% KI = 0,69; 1,03). De ettåriga överlevnadsfrekvenserna var 46,5% för patienter som fick Vidaza mot 34,3% för patienter som fick CCR.
Cox proportionella riskmodell, justerad för förspecificerade prognostiska faktorer vid baseline, definierade en HR för Vidaza jämfört med CCR på 0,80 (95% KI = 0,66; 0,99; p = 0,0355).
Trots att studien inte var utformad för att visa en statistiskt signifikant skillnad när man jämförde azacitidin med de förvalda CCR-behandlingsgrupperna, var dessutom överlevnaden för Vidaza-behandlade patienter längre jämfört med CCR-behandlingsalternativen enbart BSC, låg dos av cytarabin plus BSC, och likartade jämfört med intensiv kemoterapi av standardtyp plus BSC.
I alla förspecificerade subgrupper (ålder [< 75 år och ≥ 75 år], kön, etnisk tillhörighet, ECOG-funktionsstatus [0 eller 1 och 2], cytogenetisk risk vid baseline [intermediär och ”poor”], geografiskt område, WHO:s klassificering av AML [inklusive AML med myelodysplasirelaterade förändringar], antal vita blodkroppar vid baseline [≤ 5 x109/liter och > 5 x 109/liter], benmärgsblaster vid baseline [≤ 50% och > 50%] och tidigare anamnes på MDS), fanns det en tendens till OS-fördel som gynnade Vidaza. I några förspecificerade subgrupper nådde HR för OS statistisk signifikans inkluderande patienter med ”poor” cytogenetisk risk, patienter med AML med myelodysplasirelaterade förändringar, patienter < 75 år, kvinnliga patienter och icke-asiatiska patienter.
Hematologiska och cytogenetiska svar bedömdes av prövaren och av IRC med likartade resultat. Total svarsfrekvens (fullständig remission [CR] + fullständig remission med ofullständig återhämtning av blodkroppsantal [CRi]) enligt vad som bestämts av IRC var 27,8% i Vidaza-gruppen och 25,1% i den kombinerade CCR-gruppen (p = 0,5384). För patienter som uppnådde CR eller CRi var medianvärdet för remissionsvaraktighet 10,4 månader (95% KI = 7,2; 15,2) för Vidaza-patienterna och 12,3 månader (95% KI = 9,0; 17,0) för CCR-patienterna. En överlevnadsfördel påvisades även för patienter som inte hade uppnått ett fullständigt svar för Vidaza jämfört med CCR.
Vidaza-behandling förbättrade perifera blodkroppsvärden och ledde till ett minskat behov av RBC- och trombocyttransfusioner. En patient betraktades som beroende av RBC- eller trombocyttransfusion vid baseline om patienten hade fått en eller flera RBC- eller trombocyttransfusioner under de 56 dagarna (8 veckorna) vid eller före randomisering. En patient betraktades som oberoende av RBC- eller trombocyttransfusion under behandlingsperioden om patienten inte hade fått några RBC- eller trombocyttransfusioner under 56 dagar i följd under rapporteringsperioden.
Av patienterna i Vidaza-gruppen som var beroende av RBC-transfusion vid baseline blev 38,5% (95% KI = 31,1; 46,2) av dessa patienter oberoende av RBC-transfusion under behandlingsperioden, jämfört med 27,6% (95% KI = 20,9; 35,1) av patienterna i de kombinerade CCR-grupperna. För patienter som var beroende av RBC-transfusion vid baseline och uppnådde transfusionsoberoende under behandling var medianvaraktigheten för oberoende av RBC-transfusion 13,9 månader i Vidaza-gruppen och uppnåddes inte i CCR-gruppen.
Av patienterna i Vidaza-gruppen som var beroende av trombocyttransfusion vid baseline blev 40,6% (95% KI = 30,9; 50,8) av dessa patienter oberoende av trombocyttransfusion under behandlingsperioden, jämfört med 29,3% (95% KI = 19,7; 40,4) av patienterna i de kombinerade CCR-grupperna. För patienter som var beroende av trombocyttransfusion vid baseline och uppnådde transfusionsoberoende under behandling var medianvaraktigheten för oberoende av trombocyttransfusion 10,8 månader i Vidaza-gruppen och 19,2 månader i CCR-gruppen.
Hälsorelaterad livskvalitet (HRQoL) bedömdes med hjälp av frågeformuläret EORTC QLQ-C30 (European Organization for Research and Treatment of Cancer Core Quality of Life Questionnaire). HRQoL-data kunde analyseras för en delgrupp av hela studiepopulationen. Det finns begränsningar i analysen, men tillgängliga data tyder på att patienter inte får någon betydande nedsättning av livskvaliteten under behandling med Vidaza.
Pediatrisk population
Studien AZA-JMML-001 var en internationell öppen multicenterstudie i fas 2 för att utvärdera farmakokinetik, farmakodynamik, säkerhet och effekt av Vidaza före HSCT hos pediatriska patienter med nyligen diagnosticerad framskriden MDS eller JMML. Det primära effektmåttet för den kliniska studien var att utvärdera effekten av Vidaza med avseende på respons frekvens vid cykel 3, dag 28.
Patienterna (MDS, n = 10; JMML, n = 18, 3 månader till 15 år, 71% av manligt kön) behandlades intravenöst med Vidaza 75 mg/m², dagligen på dag 1 till 7 i en 28-dagarscykel under minst 3 cykler och högst 6 cykler.
Inklusionen i MDS-studien stoppades efter 10 MDS-patienter på grund av bristande effekt, inga bekräftade behandlingssvar registrerades för dessa 10 patienter.
I studiegruppen för JMML registrerades 18 patienter (13 PTPN11, 3 NRAS, 1 KRAS somatiska mutationer och 1 klinisk diagnos av neurofibromatos typ 1 [NF‑1]). 16 patienter slutförde 3 behandlingscykler och 5 av dem slutförde 6 cykler. Sammanlagt 11 JMML-patienter hade uppnått klinisk respons vid cykel 3, dag 28, av dessa 11 patienter hade 9 (50%) bekräftad klinisk respons (3 patienter med cCR och 6 patienter med cPR). I den kohort av JMML-patienter som behandlades med Vidaza hade 7 patienter (43,8%) bestående trombocyt respons (värden på ≥ 100 × 109/l) och 7 patienter (43,8%) behövde transfusioner vid HSCT. 17 av 18 patienter fortsatte till HSCT.
På grund av studiens design (lågt patientantal och flertalet förväxlingsfaktorer) kan inga slutsatser dras av denna kliniska studie om Vidaza före HSCT förbättrar överlevnaden hos JMML-patienter.
Studien AZA-AML-004 var en öppen multicenterstudie i fas 2 för att utvärdera säkerhet, farmakodynamik och effekt av Vidaza jämfört med ingen cancerbehandling av barn och unga vuxna med AML i molekylärt återfall efter CR1.
Sju patienter (medianålder 6,7 år [ålder mellan 2 till 12 år], 71,4% av manligt kön) behandlades med intravenöst Vidaza 100 mg/m², dagligen på dag 1 till 7 i en
28-dagarscykel under högst 3 cykler.
Fem patienter genomgick en MRD-bedömning (minimal residual disease) på dag
84 varav 4 patienter antingen uppnådde molekylär stabilisering (n = 3) eller molekylär förbättring (n = 1) och en patient hade ett kliniskt återfall. Sex av sju patienter
(90% [95% CI = 0,4, 1,0]) som behandlats med azacitidin genomgick blodstamcellstransplantation (HSCT).
På grund av lågt patientantal kan effekten av Vidaza i pediatrisk AML inte fastställas.
Se avsnitt Biverkningar för säkerhetsinformation.
Farmakokinetik
Absorption
Efter subkutan administrering av en singeldos om 75 mg/m2 absorberades azacitidin snabbt med maximala koncentrationer i plasma på 750 ± 403 ng/ml vid 0,5 tim efter dosering (första provtagningen). I förhållande till intravenös administrering var den absoluta biotillgängligheten av subkutant administrerat azacitidin (singeldoser om 75 mg/m2) ca 89% baserat på ytan under kurvan (area under the curve, AUC).
Ytan under kurvan och den maximala plasmakoncentrationen (Cmax) vid subkutan administrering av azacitidin var ungefär proportionella inom dosintervallet 25 till 100 mg/m2.
Distribution
Efter intravenös administrering var den genomsnittliga distributionsvolymen 76 ± 26 l och systemisk clearance var 147 ± 47 l/tim.
Metabolism
Baserat på in vitro-data förefaller metabolismen av azacitidin inte medieras av cytokrom P450-isoenzymer (CYP:er), UDP-glukuronosyltransferaser (UGT:er), sulfotransferaser (SULT:er) eller glutationtransferaser (GST:er).
Azacitidin undergår spontan hydrolys och deaminering medierad av cytidindeaminas. I humana lever-S9-fraktioner var bildningen av metaboliter oberoende av NADPH, vilket implicerar att metabolismen av azacitidin inte medierades av cytokrom P450–isoenzymer. En in vitro-studie av azacitidin med odlade humana hepatocyter indikerar att azacitidin i koncentrationer om 1,0 µM till 100 µM (dvs. upp till ca 30 gånger högre än kliniskt uppnåbara koncentrationer) inte inducerar CYP 1A2, 2C19 eller 3A4 eller 3A5. I studier för att skatta hämningen av en rad P450-isoenzymer (CYP 1A2, 2B6, 2C8, 2C9, 2C19, 2D6, 2E1 och 3A4) orsakades inte hämning av upp till 100 µM azacitidin. Således är det inte troligt att azacitidin inducerar eller hämmar CYP-enzymer vid kliniskt uppnåbara plasmakoncentrationer.
Eliminering
Azacitidin elimineras snabbt från plasma med en genomsnittlig elimineringshalveringstid (t½) om 41 ± 8 minuter efter subkutan administrering. Det sker ingen ackumulering efter subkutan administrering av 75 mg/m2 azacitidin en gång dagligen i 7 dagar. Utsöndring via urinen är den primära eliminationsvägen för azacitidin och/eller dess metaboliter. Efter intravenös och subkutan administrering av 14C azacitidin, återfanns 85 respektive 50% av den administrerade radioaktiviteten i urinen medan < 1% återfanns i feces.
Särskilda populationer
Inga formella studier har gjorts av effekterna av nedsatt leverfunktion (se avsnitt Dosering), kön, ålder eller etnisk tillhörighet på azacitidins farmakokinetik.
Pediatrisk population
I studien AZA-JMML-001,genomfördes farmakokinetisk analys från 10 pediatriska MDS- och 18 pediatriska JMML-patienter på dag 7 i cykel 1 (se avsnitt Farmakodynamik). Medianåldern (intervallet) på MDS-patienterna var 13,3 (1,9–15) år och 2,1 (0,2–6,9) år för JMML-patienterna.
Efter intravenös administrering av en dos på 75 mg/m2 uppnådde Vidaza snabbt Cmax inom 0,083 timmar hos både MDS- och JMML-populationen. Geometriskt genomsnittligt Cmax var 1 797,5 och 1 066,3 ng/ml och geometriskt genomsnittligt AUC0-∞ var 606,9 och 240,2 ng°h/ml för MDS- respektive JMML-patienterna. Den geometriska genomsnittliga distributionsvolymen hos MDS- och JMML-patienterna var 103,9 respektive 61,1 l. Det visade sig att den totala plasmaexponeringen för Vidaza var högre hos MDS-patienterna, men en måttlig till hög variabilitet mellan patienterna observerades för både AUC och Cmax.
Geometrisk genomsnittlig t½ var 0,4 och 0,3 timmar, och geometrisk genomsnittlig clearance var 166,4 respektive 148,3 l/h för MDS respektive JMML.
Farmakokinetiska data från studien AZA-JMML-001 sammanfördes och jämfördes med farmakokinetiska data från 6 vuxna MDS patienter som administrerats med 75 mg/m2 Vidaza intravenöst i studien AZA‑2002-BA-002. Genomsnittligt Cmax och AUC0-t för Vidaza var liknande hos vuxna och pediatriska patienter efter intravenös administrering (2 750 ng/ml kontra 2 841 ng/ml respektive 1 025 ng°h/ml kontra 882,1 ngºh/ml).
I studien AZA-AML-004 genomfördes farmakokinetisk analys från 6 av de
7 pediatriska patienterna, som fått minst en mätbar farmakokinetisk koncentration efter dosering (se avsnitt Farmakodynamik). Medianåldern (intervallet) på AML-patienterna
var 6,7 (2–12) år.
Efter flera doser på 100 mg/m2 observerades geometrisk median för Cmax och
AUC0-tau i cykel 1, dag 7 på 1 557 ng/ml respektive 899,6 ng°h/ml med hög interindividuell variation (CV% på 201,6% respektive 87,8%). Azacitidin uppnådde snabbt Cmax, med en mediantid på 0,090 timmar efter intravenös administrering och minskade med den genomsnittliga medianen t1/2 av 0,380 timmar. Den geometriska medianen för clearance och volym var 127,2 L/h respektive 70,2 L.
Farmakokinetisk (azacitidin) exponering observerad hos barn med AML i molekylärt återfall efter CR1 var jämförbar med samlade exponeringsdata för 10 barn med MDS och 18 barn med JMML och även jämförbar med azacitidinexponering hos vuxna med MDS.
Nedsatt njurfunktion
Nedsatt njurfunktion har ingen större effekt på den farmakokinetiska exponeringen av azacitidin efter enstaka eller flera subkutana administreringar. Efter subkutan administrering av en enda dos på 75 mg/m2 ökade de genomsnittliga exponeringsvärdena (AUC och Cmax) hos försökspersoner med lätt, måttligt och gravt nedsatt njurfunktion med 11-21%, 15-27% respektive 41-66% jämfört med försökspersoner med normal njurfunktion. Exponeringen låg dock inom samma generella spridning för exponeringsvärden som observerats hos försökspersoner med normal njurfunktion. Azacitidin kan ges till patienter med nedsatt njurfunktion utan initial dosjustering förutsatt att dessa patienter övervakas med avseende på toxicitet, eftersom azacitidin och/eller dess metaboliter huvudsakligen utsöndras via njurarna.
Farmakogenomik
Effekten av kända polymorfismer hos cytidindeaminas på azacitidins metabolism har inte formellt undersökts.
Prekliniska uppgifter
Azacitidin inducerar både genmutationer och kromosomavvikelser i bakterie- och däggdjurscellsystem in vitro. Azacitidins potentiella karcinogenicitet utvärderades hos mus och råtta. Azacitidin framkallade tumörer i det hematopoetiska systemet hos honmöss när det administrerades intraperitonealt 3 gånger i veckan i 52 veckor. En ökad incidens av tumörer i det lymforetikulära systemet, lungor, mjölkkörtlar och hud observerades hos möss som behandlades med azacitidin som administrerades intraperitonealt i 50 veckor. En tumorigenicitetsstudie på råtta visade en ökad incidens av testikeltumörer.
Studier av tidig embryotoxicitet hos möss visade en frekvens av intrauterin embryonal död (ökad resorption) på 44% efter en intraperitoneal enkelinjektion av azacitidin under organogenesen. Utvecklingsavvikelser i hjärnan har påvisats hos möss som gavs azacitidin vid eller före slutningen av den hårda gommen. Hos råtta framkallade azacitidin inga biverkningar när det gavs före implantationen, men var tydligt embryotoxiskt när det gavs under organogenesen. Fosterabnormiteter under organogenesen hos råtta inkluderade: CNS-anomalier (exencefali/encefalocele), extremitetsanomalier (mikromeli, klubbfot, syndaktyli, oligodaktyli) och andra (mikroftalmi, mikrognati, gastroschis, ödem och revbensabnormiteter).
Administrering av azacitidin till hanmöss före parning med obehandlade honmöss resulterade i minskad fertilitet och förlust av avkommor under efterföljande embryonal och postnatal utveckling. Behandling av hanråttor resulterade i minskad testikel- och bitestikelvikt, minskat spermietal, minskade dräktighetsfrekvenser, ökat antal abnorma embryon och ökad förlust av embryon hos parade honråttor (se avsnitt Graviditet).
Innehåll
Kvalitativ och kvantitativ sammansättning
Varje injektionsflaska innehåller 100 mg azacitidin. Efter beredning innehåller varje ml av suspensionen 25 mg azacitidin.
Förteckning över hjälpämnen
Mannitol (E421)
Blandbarhet
Detta läkemedel får inte blandas med andra läkemedel förutom de som nämns i avsnitt Hållbarhet, förvaring och hantering.
Hållbarhet, förvaring och hantering
Hållbarhet
Oöppnad injektionsflaska med pulver:
4 år
Efter beredning:
När Vidaza bereds med användning av oavkylt vatten för injektionsvätska har kemisk och fysikalisk stabilitet under användning av det beredda läkemedlet visats i 45 minuter vid 25 °C och i 8 timmar vid 2–8 °C.
Det beredda läkemedlets hållbarhet kan förlängas genom beredning med avkylt (2–8 °C) vatten för injektionsvätska. När Vidaza bereds med användning av avkylt (2–8 °C) vatten för injektionsvätska, har kemisk och fysikalisk stabilitet under användning av det beredda läkemedlet visats i 22 timmar vid 2–8 °C.
Av mikrobiologiska skäl bör den beredda produkten användas omedelbart. Om den inte används omedelbart, är tiden och förhållandena för förvaring före användning användarens ansvar, och får inte vara längre än 8 timmar vid 2–8 °C, när den har beretts med användning av oavkylt vatten för injektionsvätska och inte längre än 22 timmar när den har beretts med avkylt (2–8 °C) vatten för injektionsvätska.
Särskilda förvaringsanvisningar
Oöppnade injektionsflaskor
Inga särskilda förvaringsanvisningar.
Färdigberedd suspension
Förvaringsanvisningar för läkemedlet efter beredning finns i avsnitt Hållbarhet.
Särskilda anvisningar för destruktion och övrig hantering
Rekommendationer för säker hantering
Vidaza är ett cytotoxiskt läkemedel och, liksom för andra potentiellt toxiska föreningar, ska försiktighet iakttas vid hantering och beredning av azacitidinsuspensioner. Rutiner för korrekt hantering och omhändertagande av cancerläkemedel ska följas.
Om berett azacitidin kommer i kontakt med hud, skölj omedelbart och noga med vatten och tvål. Vid kontakt med slemhinnor, skölj noga med vatten.
Beredning
Vidaza ska beredas med vatten för injektionsvätska. Det beredda läkemedlets hållbarhet kan förlängas genom beredning med avkylt (2–8 °C) vatten för injektionsvätska. Anvisningar om förvaring av den beredda produkten ges nedan.
-
Följande artiklar ska läggas fram:
Injektionsflaska(or) med azacitidin; injektionsflaska(or) med vatten för injektionsvätska; osterila operationshandskar; spritkompresser; 5 ml injektionsspruta(or) med injektionsnål(ar).
-
4 ml vatten för injektionsvätska ska dras upp i sprutan. Se till att tömma sprutan på all luft.
-
Injektionsnålen på sprutan innehållande 4 ml vatten för injektionsvätska ska stickas in genom gummiproppen på injektionsflaskan med azacitidin följt av injektion av vattnet för injektionsvätska i injektionsflaskan.
-
Efter att sprutan och injektionsnålen har tagits bort ska injektionsflaskan skakas kraftigt tills en enhetlig, grumlig suspension erhållits. Efter beredning innehåller varje ml av suspensionen 25 mg azacitidin (100 mg/4 ml). Den beredda produkten är en homogen, grumlig suspension utan agglomerat. Suspensionen ska kasseras om den innehåller stora partiklar eller agglomerat. Filtrera inte den färdigberedda suspensionen eftersom den aktiva substansen då kan avlägsnas. Man måste tänka på att det kan finnas filter i vissa adaptrar, spikes och slutna system. Sådana system ska därför inte användas till administrering av det färdigberedda läkemedlet.
-
Gummiproppen ska tvättas och en ny spruta med injektionsnål stickas in i injektionsflaskan. Injektionsflaskan ska sedan vändas upp-och-ned. Se till att injektionsnålspetsen är under vätskenivån. Kolven ska därefter dras tillbaka för att dra upp erforderlig mängd läkemedel för rätt dos. Se till att sprutan töms på all luft. Sprutan med injektionsnålen ska därefter dras ut ur injektionsflaskan och injektionsnålen kasseras.
-
En ny injektionsnål (25 gauge rekommenderas) för subkutan injektion ska därefter sättas fast på sprutan. Ingen suspension ska tryckas ut ur injektionsnålen före injektion för att minska incidensen av lokala reaktioner vid injektionsstället.
-
När det behövs mer än 1 injektionsflaska ska ovanstående steg för beredning av suspensionen upprepas. För doser som kräver mer än 1 injektionsflaska ska lika stora doser ges, t.ex. 150 mg dos = 6 ml, 2 sprutor med 3 ml i vardera sprutan. På grund av retentionen i injektionsflaskan och injektionsnålen är det eventuellt inte möjligt att dra ut hela suspensionen ur injektionsflaskan.
-
Innehållet i doseringssprutan måste resuspenderas omedelbart före administrering. Sprutan som är fylld med beredd suspension ska tas ut ur kylskåpet 30 minuter före administrering för att anta en temperatur på ca 20–25°C. Om längre tid än 30 minuter förflyter, ska suspensionen kasseras på lämpligt sätt och en ny dos beredas. Resuspendering åstadkoms genom att sprutan rullas kraftigt mellan handflatorna tills en enhetlig, grumlig suspension erhålls. Suspensionen ska kasseras om den innehåller stora partiklar eller agglomerat.
Förvaring av den beredda produkten
Förvaringsanvisningar för läkemedlet efter beredning finns i avsnitt Hållbarhet.
Beräkning av en individuell dos
Den totala dosen efter kroppsyta (body surface area, BSA) kan beräknas enligt följande:
Total dos (mg) = Dos (mg/m2) x BSA (m2)
Följande tabell tillhandahålls endast som ett exempel på hur individuella azacitidindoser, baserade på ett genomsnittligt BSA-värde om 1,8 m2, beräknas.
|
Dos mg/m2 (% av rekommenderad startdos) |
Total dos baserad på BSA-värdet 1,8 m2 |
Erforderligt antal injektionsflaskor |
Total volym beredd suspension som erfordras |
|---|---|---|---|
|
75 mg/m2 (100%) |
135 mg |
2 injektionsflaskor |
5,4 ml |
|
37,5 mg/m2 (50%) |
67,5 mg |
1 injektionsflaska |
2,7 ml |
|
25 mg/m2 (33%) |
45 mg |
1 injektionsflaska |
1,8 ml |
Administreringssätt
Berett Vidaza ska injiceras subkutant (injektionsnålen sticks in i 45-90° vinkel) med en 25 gauge injektionsnål i överarmen, låret eller buken.
Högre doser än 4 ml ska injiceras på två skilda ställen.
Injektionsstället ska roteras. Nya injektioner ska ges minst 2,5 cm från det tidigare injektionsstället och aldrig i områden där stället ömmar eller där blåmärken, rodnad eller förhårdnad föreligger.
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Egenskaper hos läkemedelsformen
Pulver till injektionsvätska, suspension.
Vitt, frystorkat pulver.
Förpackningsinformation
Pulver till injektionsvätska, suspension 25 mg/ml
Vitt frystorkat pulver
4 milliliter rekonstituerad injektionsflaska (fri prissättning), tillhandahålls ej
Följande produkter har även parallelldistribuerade förpackningar:
Pulver till injektionsvätska, suspension 25 mg/ml




