Indikationer
Behandling av genombrottssmärta hos vuxna patienter som redan behandlas med opioider för långvarig cancersmärta. Genombrottssmärta är ett övergående smärtskov under en i övrigt kontrollerad långvarig smärta.
Kontraindikationer
Överkänslighet mot den aktiva substansen eller mot något hjälpämne som anges i avsnitt Innehåll.
Patienter utan underhållsbehandling med opioider eftersom det medför ökad risk för andningsdepression.
Uttalad andningsdepression eller grava obstruktiva lungsjukdomar.
Behandling av akut smärta annan än genombrottssmärta.
Patienter som behandlas med läkemedel innehållande natriumoxibat.
Dosering
Abstral skall endast administreras till patienter som betraktas som toleranta mot den opioidbehandling de får mot sin ihållande cancersmärta. Patienter kan betraktas som opioidtoleranta om de tar minst 60 mg oralt morfin dagligen, minst 25 mikrogram fentanyl transdermalt per timme, minst 30 mg oxikodon dagligen, minst 8 mg oralt hydromorfon dagligen eller en ekvianalgetisk dos av någon annan opioid under en vecka eller längre.
Administreringssätt:
Abstral sublinguala resoribletter skall administreras direkt under tungan, i den djupaste delen. Abstral sublinguala resoribletter får inte sväljas, utan skall i stället få tid att lösas upp helt och hållet i den sublinguala kaviteten utan att tuggas eller sugas. Patienterna skall rekommenderas att inte äta eller dricka någonting förrän den sublinguala resoribletten är fullständigt upplöst.
Patienter med torr mun kan använda vatten för att fukta buckalslemhinnan innan de tar Abstral.
Dostitrering:
Målet med dostitrering är att identifiera en optimal underhållsdos för fortgående behandling av episoder av genombrottssmärta. Denna optimala dos ska ge adekvat smärtlindring med en acceptabel förekomst av biverkningar.
Den optimala dosen av Abstral bestäms genom en upptitrering, individuellt anpassad för varje patient. Flera olika doser finns tillgängliga för användning under dostitreringsfasen. Initialt bör en Abstral-dos på 100 mikrogram användas, och därefter titreras upp efter behov med de olika tillgängliga dosstyrkorna.
Patienterna skall övervakas noggrant tills en optimal dos erhålls.
Ett byte från andra läkemedel som innehåller fentanyl till Abstral får inte vara 1:1 på grund av olika absorptionsprofiler. Om patienten byter från ett annat läkemedel som innehåller fentanyl krävs en ny dostitrering med Abstral.
Följande dosregim rekommenderas för titrering, även om behandlande läkare i varje enskilt fall skall ta hänsyn till patientens kliniska behov, ålder och övriga sjukdomar.
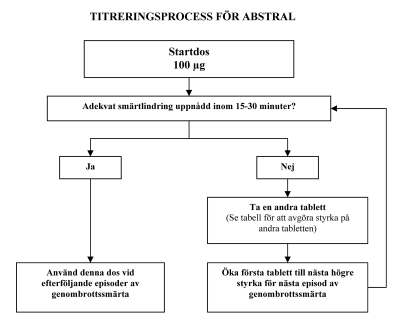
Samtliga patienter måste inleda behandlingen med en enstaka 100 mikrogram sublingual resoriblett. Om adekvat analgesi inte erhålles inom 15–30 minuter från administreringen av en enda sublingual resoriblett, kan en extra (andra) 100 mikrogram sublingual resoriblett administreras. Om adekvat analgesi inte erhålles inom 15-30 minuter efter den första dosen bör en dosökning till nästa högre tillgängliga tablettstyrka övervägas vid nästa episod av genombrottssmärta. (Se nedanstående figur).
Man bör fortsätta med en stegvis dosupptrappning till dess adekvat analgesi med tolerabla biverkningar uppnås. Dosstyrkan för den extra (andra) sublinguala resoribletten bör ökas från 100 till 200 mikrogram vid doser på 400 mikrogram och högre. Detta illustreras i tabellen nedan. Under titreringsfasen skall inte fler än två (2) doser administreras för varje enskild episod av genombrottssmärta.
|
Styrka (mikrogram) för den första sublinguala resoribletten vid varje episod av genombrottssmärta |
Styrka (mikrogram) för den extra (andra) sublinguala resoribletten, som vid behov tas 15–30 minuter efter den första resoribletten |
|
100 |
100 |
|
200 |
100 |
|
300 |
100 |
|
400 |
200 |
|
600 |
200 |
|
800 |
- |
Om adekvat analgesi uppnås med den högre dosen, men biverkningarna bedöms som oacceptabla, kan en intermediär dos administreras (vid behov med hjälp av sublinguala resoribletter på 100 mikrogram).
Under titreringen kan patienterna instrueras att använda flera 100 mikrogramstabletter och/eller 200 mikrogramstabletter för en enskild dos. Inte fler än fyra (4) tabletter skall användas vid något tillfälle.
Effekt och säkerhet med doser över 800 mikrogram har inte utvärderats hos patienter i kliniska studier.
För att minimera risken för opioidrelaterade biverkningar och identifiera optimal dos är det absolut nödvändigt att patienten övervakas noga av sjukvårdspersonal under titreringsprocessen.
Under titreringen skall patienterna vänta minst 2 timmar innan de behandlar ännu en episod av genombrottssmärta med Abstral.
Underhållsbehandling:
När optimal dos har fastsällts, eventuellt omfattande mer än en tablett, skall patienten underhållsbehandlas med denna dos, dock begränsad till maximalt fyra doseringstillfällen med Abstral per dag.
Under underhållsperioden skall patienterna vänta minst 2 timmar innan de behandlar ännu en episod av genombrottssmärta med Abstral.
Dosjusteringar:
Om behandlingssvaret (analgesi eller oönskade reaktioner) på den titrerade Abstral-dosen märkbart förändras, kan det vara nödvändigt med dosjustering för att säkerställa att en optimal dos bibehålls. Om patienten har fler än fyra episoder av genombrottssmärta per dag under mer än fyra dagar i följd, skall dosen av den långverkande opioiden mot ihållande smärta utvärderas på nytt. Om den långtidsverkande opioiden byts ut eller om doseringen av den långtidsverkande opioiden höjs, kan dosen av Abstral behöva omprövas och omtitreras för att säkerställa att patienten står på en optimal dos.
Det är absolut nödvändigt att en eventuell omtitrering av något av insatta analgetika endast sker under övervakning av sjukvårdspersonal.
Om adekvat smärtkontroll inte uppnås ska risken för hyperalgesi, tolerans eller progression av den underliggande sjukdomen övervägas (se avsnitt Varningar och försiktighet).
Behandlingslängd och behandlingsmål
Innan behandling med Abstral inleds ska en behandlingsstrategi som omfattar behandlingslängd, behandlingsmål samt en plan för avslutande av behandlingen fastställas i samråd med patienten och i enlighet med riktlinjerna för smärtbehandling. Under behandlingen ska läkare och patient ha frekvent kontakt för bedömning av behovet av fortsatt behandling, övervägande av utsättning och för att dosjustera vid behov. Om tillräcklig smärtkontroll inte uppnås ska eventuell hyperalgesi, tolerans och progression av underliggande sjukdom övervägas (se avsnitt Varningar och försiktighet). Abstral ska inte användas under längre tid än vad som är nödvändigt.
Utsättning av behandlingen:
Abstral ska omedelbart sättas ut om patienten inte längre har episoder av genombrottssmärta. Behandlingen av ihållande bakgrundssmärta ska fortsätta i enlighet med ordinationen.
Om det är nödvändigt att sätta ut all opioidbehandling måste läkaren noga övervaka patienten för att hantera risken för abrupta utsättningseffekter.
Behandling av barn och ungdomar:
Abstral får ej användas till patienter under 18 år beroende på brist på data avseende säkerhet och effekt.
Användning till äldre
Dostitreringen måste ske med särskild omsorg och patienterna observeras noga med avseende på tecken på fentanyltoxicitet (se avsnitt Varningar och försiktighet).
Användning till patienter med nedsatt njur- eller leverfunktion
Patienter med nedsatt njur- eller leverfunktion skall observeras noga med avseende på tecken på fentanyltoxicitet under Abstral-titreringsfasen (se avsnitt Varningar och försiktighet).
Varningar och försiktighet
På grund av de risker, däribland dödsfall, som är förknippade med oavsiktlig exponering, felaktig användning och missbruk, måste patienter och deras vårdgivare uppmanas att förvara Abstral på ett säkert ställe, som inte är tillgängligt för andra.
Patienter och deras vårdgivare måste informeras om att Abstral innehåller en aktiv substans i en mängd som kan vara dödlig för ett barn och att tabletterna därför alltid måste förvaras utom syn och räckhåll för barn.
På grund av de potentiellt allvarliga biverkningar som kan uppträda vid behandling med opioider som Abstral måste patienter och deras vårdgivare vara fullt medvetna om vikten av att ta Abstral på korrekt sätt och vilka åtgärder som skall vidtas om symptom på överdosering skulle uppträda.
Innan behandling med Abstral påbörjas är det viktigt att den behandling med långverkande opioid som patienten får för att kontrollera den ihållande smärtan har stabiliserats.
Tolerans och opioidbrukssyndrom (missbruk och beroende)
Tolerans och fysiskt och/eller psykologiskt beroende kan utvecklas vid upprepad administrering av opioider som fentanyl.
Upprepad användning av Abstral kan leda till opioidbrukssyndrom. Högre dos och längre behandlingstid med opioider kan öka risken för att utveckla opioidbrukssyndrom. Missbruk eller avsiktlig felanvändning av Abstral kan resultera i överdos och/eller dödsfall. Risken för att utveckla opioidbrukssyndrom är förhöjd hos patienter med en personlig anamnes eller en familjeanamnes (föräldrar eller syskon) på drogberoende (inklusive alkoholberoende), hos patienter som använder tobak eller hos patienter med andra psykiska sjukdomar i anamnesen (t.ex. egentlig depression, ångest och personlighetsstörning).
Innan behandling med Abstral inleds och under behandlingen ska behandlingsmål och utsättningsplan fastställas i samråd med patienten (se avsnitt Dosering). Före och under behandlingen ska patienten också informeras om riskerna för och tecknen på opioidbrukssyndrom. Patienterna ska uppmanas att kontakta läkare om sådana tecken skulle uppträda.
Patienterna ska övervakas för tecken på drogsökande beteende (t.ex. för tidiga önskemål om påfyllning). Detta inkluderar en genomgång av opioider och psykoaktiva läkemedel (såsom bensodiazepiner) som används samtidigt. Hos patienter med tecken och symtom på opioidbrukssyndrom ska konsultation med en beroendespecialist övervägas.
Respiratorisk depression
Som med alla opioider finns det risk för kliniskt signifikant andningsdepression vid användning av Abstral. Särskild försiktighet bör iakttas under dostitrering av Abstral hos patienter med kronisk obstruktiv lungsjukdom eller andra medicinska tillstånd som predisponerar för andningsdepression (t.ex. myastenia gravis). Detta till följd av risken för ytterligare andningsdepression, som skulle kunna leda till andningssvikt.
Ökat intrakraniellt tryck
Abstral skall endast administreras med yttersta försiktighet till patienter som kan vara särskilt utsatta för intrakraniella effekter av hyperkapni, såsom patienter som uppvisar tecken på ett förhöjt intrakraniellt tryck, sänkt medvetande, koma eller hjärntumörer. Hos patienter med skallskador kan det kliniska förloppet maskeras vid användning av opioider. I sådana fall bör opioider endast användas om det är absolut nödvändigt.
Hyperalgesi
Liksom med andra opioider ska risken för opioidinducerad hyperalgesi övervägas om patienten inte uppnår tillräcklig smärtkontroll trots ökad dos fentanyl. I sådana fall kan en sänkning av fentanyldosen eller utsättning av fentanylbehandlingen vara indicerad.
Hjärtsjukdom
Fentanyl kan ge upphov till bradykardi. Fentanyl bör användas med försiktighet till patienter med tidigare eller befintliga bradyarytmier.
Äldre, kakektiska eller patienter med nedsatt allmäntillstånd
Data från studier med intravenöst administrerat fentanyl antyder att äldre patienter kan ha ett nedsatt clearance, en förlängd halveringstid och att de kan vara känsligare för den aktiva substansen än yngre patienter. Äldre, kakektiska eller patienter med nedsatt allmäntillstånd skall observeras noga med avseende på tecken på fentanyltoxicitet och dosen skall vid behov reduceras.
Nedsatt lever- eller njurfunktion
Abstral skall administreras med försiktighet till patienter med nedsatt lever- eller njurfunktion, speciellt under titreringsfasen. Användning av Abstral till patienter med nedsatt lever- eller njurfunktion kan öka biotillgängligheten för fentanyl och minska dess systemiska clearance, vilket skulle kunna medföra en ackumulering och ökade och förlängda opioideffekter.
Hypovolemi och hypotoni
Försiktighet bör iakttas vid behandling av patienter med hypovolemi och hypotension.
Användning till patienter med munsår eller mukosit
Abstral har inte studerats hos patienter med munsår eller mukosit. Det kan föreligga en risk för förhöjd systemisk läkemedelsexponering och extra försiktighet rekommenderas därför vid dostitrering.
Utsättande av Abstral
Det bör inte uppstå några märkbara symtom vid utsättande av Abstral, men möjliga utsättningssymtom innefattar ångest, tremor, svettningar, blekhet, illamående och kräkningar.
Serotonergt syndrom
Försiktighet bör iakttas när Abstral administreras samtidigt med läkemedel som påverkar det serotonerga signalsubstanssystemet.
Ett eventuellt livshotande serotonergt syndrom kan uppkomma vid samtidig användning av serotonerga läkemedel som selektiva serotoninåterupptagshämmare (SSRI) och selektiva serotonin-noradrenalinåterupptagshämmare (SNRI), och med läkemedel som påverkar metabolismen av serotonin (t.ex. monoaminoxidashämmare [MAO-hämmare]). Detta kan uppkomma med den rekommenderade dosen.
Serotonergt syndrom kan omfatta förändringar av mental status (t.ex. agitation, hallucinationer, koma), autonom instabilitet (t.ex. takykardi, instabilt blodtryck, hypertermi), neuromuskulära avvikelser (t.ex. hyperreflexi, inkoordination, stelhet) och/eller gastrointestinala symtom (t.ex. illamående, kräkningar, diarré).
Vid misstanke om serotonergt syndrom ska behandlingen med Abstral sättas ut.
Sömnrelaterade andningsstörningar
Opioider kan orsaka sömnrelaterade andningsstörningar, såsom central sömnapné och sömnrelaterad hypoxemi. Risken för central sömnapné ökar med dosen. Överväg att minska den totala dosen opioider till patienter med central sömnapné.
Risk vid samtidig användning av sedativa läkemedel såsom bensodiazepiner eller relaterade läkemedel
Samtidig användning av Abstral och sedativa läkemedel såsom bensodiazepiner eller relaterade läkemedel kan resultera i sedering, respiratorisk depression, koma och död. På grund av dessa risker ska samtidig förskrivning av sedativa läkemedel reserveras till patienter för vilka andra behandlingsalternativ inte är möjliga. Om det beslutas att Abstral ska förskrivas samtidigt med sedativa läkemedel, ska lägsta dosen användas och behandlingstiden hållas så kort som möjligt.
Patienterna ska följas noga för tecken och symtom på respiratorisk depression och sedering. I detta avseende rekommenderas starkt att patienter och deras vårdgivare informeras om att vara uppmärksamma på dessa symtom (se avsnitt Interaktioner).
Abstral innehåller natrium
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per tablett, d.v.s. är näst intill “natriumfritt”.
Interaktioner
Samtidig användning av läkemedel som innehåller natriumoxibat och fentanyl är kontraindicerad (se avsnitt Kontraindikationer). Behandling med natriumoxibat ska avbrytas före behandlingsstart med Abstral.
Fentanyl metaboliseras av CYP3A4. Läkemedel som hämmar CYP3A4-aktivitet, som makrolidantibiotika (t.ex. erytromycin), antimykotika av azoltyp (t.ex. ketokonazol, itrakonazol) eller vissa proteashämmare (t.ex. ritonavir) kan öka biotillgängligheten för fentanyl genom att minska dess systemiska clearance, och därigenom potentiellt förstärka eller förlänga opioideffekterna. Det är även känt att grapefruktjuice hämmar CYP3A4.
Samtidig administrering med medel som inducerar CYP3A4‑aktivitet såsom medel mot mykobakterier (t.ex. rifampicin, rifabutin), antikonvulsiva medel (t.ex. karbamazepim, fenytoin och fenobarbital) och naturläkemedel (t.ex. johannesört, Hypericum perforatum) kan minska effekten av fentanyl. CYP3A4‑inducerare utövar sin effekt på ett tidsberoende sätt och det kan ta minst 2 veckor innan de får maximal effekt efter insättning. Omvänt kan det vid utsättning ta minst 2 veckor innan CYP34A-induktionen klingar av. Patienter som får fentanyl och som avbryter behandlingen med, eller minskar dosen av CYP3A4‑inducerare kan löpa risk för ökad aktivitet eller toxicitet av fentanyl. Fentanyl bör därför ges med försiktighet om det administreras samtidigt med CYP3A4-hämmare och/eller CYP3A4‑inducerare
Samtidig användning av andra CNS-depressiva medel, såsom andra morfinderivat (analgetika och hostdämpande), narkosmedel, gabapentinoider (gabapentin och pregabalin), skelettmuskelrelaxerande medel, sederande antidepressiva, sederande H1-antihistaminer, barbiturater, anxiolytika (d.v.s. bensodiazepiner), hypnotika, antipsykotika, klonidin och närbesläktade substanser kan framkalla en ökning av de CNS-deprimerande effekterna, ökad risk för sedering, respiratorisk depression, hypotoni, koma och död till följd av den förstärkta CNS‑deprimerande effekten. Dos och duration för samtidig användning ska begränsas (se avsnitt Varningar och försiktighet).
Alkohol potentierar den sederande effekten hos morfinbaserade analgetika; därför rekommenderas inte samtidig administrering av alkoholhaltiga drycker eller läkemedel och Abstral.
Användning av Abstral rekommenderas inte till patienter som fått monoaminoxidashämmare (MAOhämmare) de senaste 14 dagarna eftersom allvarlig och oförutsägbar potentiering av MAO-hämmare har rapporterats med opioidanalgetika.
Samtidig användning av partiella opioidagonister/antagonister (t.ex. buprenorfin, nalbufin och pentazocin) rekommenderas inte. De har en hög affinitet till opioidreceptorer med relativt låg egen aktivitet och motverkar därför delvis den analgetiska effekten hos fentanyl och kan inducera utsättningssymptom hos opioidberoende patienter.
Serotonerga läkemedel
Samtidig administrering av fentanyl med ett serotonergt preparat, t.ex. en selektiv serotoninåterupptagshämmare (SSRI), en selektiv serotonin-noradrenalinåterupptagshämmare (SNRI) eller en monoaminoxidashämmare (MAO-hämmare), kan öka risken för serotonergt syndrom, ett eventuellt livshotande tillstånd.
Graviditet
Säkerheten hos fentanyl vid användning under graviditet har ej fastställts. Djurstudier har visat reproduktionstoxikologiska effekter med nedsatt fertilitet hos råtta (se avsnitt Prekliniska uppgifter). Risken för människor är okänd. Fentanyl skall endast användas under graviditet i de fall det är absolut nödvändigt.
Vid långtidsbehandling under graviditet kan fentanyl orsaka utsättningssymtom hos det nyfödda barnet.
Fentanyl bör ej användas under värkarbete och förlossning (inklusive kejsarsnitt), eftersom fentanyl passerar över placenta och kan orsaka andningsdepression hos fostret eller det nyfödda barnet.
Amning
Fentanyl passerar över i bröstmjölk och kan orsaka sedering och andningsdepression hos det ammade barnet. Fentanyl ska inte användas av ammande kvinnor och amning får återupptas tidigast 5 dagar passerat efter den sista administreringen av fentanyl.
Trafik
Inga studier beträffande effekterna på förmågan att framföra fordon eller använda maskiner har utförts med Abstral.
Opioidanalgetika är dock kända för att försämra den mentala eller fysiska förmågan att utföra potentiellt farliga uppgifter som att framföra fordon eller använda maskiner. Patienter bör avrådas från att framföra fordon eller använda maskiner om de drabbas av yrsel eller dåsighet eller upplever dubbelseende eller dimsyn medan de tar Abstral.
Biverkningar
De biverkningar som är typiska för opioider kan förväntas med Abstral; de tenderar att minska i intensitet med fortsatt användning. De allvarligaste potentiella biverkningarna förenade med användning av opioider är andningsdepression (som kan leda till andningsstillestånd), hypotension och chock.
De kliniska prövningarna med Abstral var utformade för att utvärdera säkerhet och effekt vid behandling av genombrottssmärta hos cancerpatienter; alla patienter tog samtidigt opioider, såsom depotmorfin, depotoxikodon eller transdermalt fentanyl, för ihållande smärta. Det är därför inte möjligt att definitivt separera effekterna av enbart Abstral.
De vanligaste observerade biverkningarna av Abstral omfattar opioidbiverkningar, såsom illamående, förstoppning, somnolens och huvudvärk.
Sammanfattningstabell över biverkningar med Abstral och/eller andra föreningar som innehåller fentanyl:
Följande biverkningar har rapporterats med Abstral och/eller andra föreningar som innehåller fentanyl under kliniska studier och efter godkännandet för försäljning.
De är listade nedan, ordnade efter organsystemklass och frekvens (mycket vanliga ≥ 1/10; vanliga ≥ 1/100 till < 1/10; mindre vanliga ≥ 1/1 000, <1/100; ingen känd frekvens (kan inte beräknas från tillgängliga data)). Biverkningarna presenteras inom varje frekvensområde efter fallande allvarlighetsgrad.
|
Organsystemklass |
Biverkningar efter frekvens |
|||
|---|---|---|---|---|
|
Mycket vanliga ≥1/10 |
Vanliga ≥1/100, <1/10 |
Mindre vanliga ≥1/1 000, <1/100 |
Ingen känd frekvens (kan inte beräknas från tillgängliga data) |
|
|
Immunsystemet |
Överkänslighet | |||
|
Metabolism och nutrition |
Anorexi Minskad aptit | |||
|
Psykiska störningar |
Depression Paranoia Förvirringstillstånd Desorientering Förändringar i mental status Ångest Euforisk sinnesstämning Dysfori Känslomässig labilitet Koncentrationssvårigheter Insomnia |
Hallucinationer Läkemedelsberoende Läkemedelsmissbruk Delirium |
||
|
Centrala och perifera nervsystemet |
Yrsel Huvudvärk Somnolens |
Amnesi Parosmi Dysgeusi Tremor Letargi Hypestesi Sömnrubbning |
Kramp Nedsatt medvetandegrad Medvetslöshet |
|
|
Ögon |
Dimsyn | |||
|
Hjärtat |
Takykardi Bradykardi | |||
|
Blodkärl |
Hypotoni | |||
|
Andningsvägar, bröstkorg och mediastinum |
Dyspné |
Orofaryngeal smärta Trånghetskänsla i strupen |
Andningsdepression |
|
|
Magtarmkanalen |
Illamående |
Stomatit Kräkningar Förstoppning Muntorrhet |
Sår i munnen Sår i tandköttet Sår på läpparna Försämrad magsäckstömning Buksmärta Dyspepsi Magbesvär Tungförändringar Aftös stomatit |
Svullen tunga Diarré |
|
Hud och subkutan vävnad |
Hyperhidros |
Hudlesion Utslag Allergisk pruritus Pruritus Nattliga svettningar Ökad tendens att få blåmärken |
Urtikaria |
|
|
Muskuloskeletala systemet och bindväv |
Artralgi Muskuloskeletal stelhet Ledstelhet | |||
|
Reproduktions-organ och bröstkörtel |
Erektil dysfunktion | |||
|
Allmänna symtom och/eller symtom vid administrerings-stället |
Trötthet |
*Abstinenssymtom Asteni Allmän sjukdomskänsla |
Rodnad och värmevallningar Perifert ödem Pyrexi Neonatalt abstinenssyndrom Läkemedelstolerans |
|
|
Skada, förgiftning och behandlings-komplikationer |
Oavsiktlig överdos |
Fall |
||
* symtom på opiatabstinens såsom illamående, kräkning, diarré, ångest, frossa, tremor och svettning har setts vid transmukosalt fentanyl
Beskrivning av utvalda biverkningar
Tolerans
Tolerans kan utvecklas vid upprepad användning.
Läkemedelsberoende
Upprepad användning av Abstral kan leda till läkemedelsberoende, även vid terapeutiska doser. Risken för läkemedelsberoende kan variera beroende på en patients individuella riskfaktorer, dosering och opioidbehandlingens längd (se avsnitt Varningar och försiktighet).
Överdosering
Symtom och tecken
Symtomen vid en överdosering av fentanyl innebär en förstärkning av de farmakologiska effekterna och den allvarligaste effekten utgörs av en andningsdepression, som kan leda till andningsstillestånd.
Det är också känt att koma förekommer.
Fall av Cheynes-Stokes andning har observerats vid överdosering av fentanyl, särskilt hos patienter med hjärtsvikt i anamnesen.
Toxisk leukoencefalopati har också observerats vid överdosering av fentanyl.
Behandling
Den omedelbara behandlingen vid en överdosering innefattar borttagande av eventuella kvarvarande Abstral subliguala resoribletter ur munnen, fysisk och verbal stimulering av patienten och bedömning av medvetandegraden. Etablera och upprätthåll en öppen luftväg. Vid behov skall en svalg- eller trakealtub sättas på plats, syre administreras och mekanisk ventilation påbörjas. Upprätthåll adekvat kroppstemperatur och vid behov parenteral vätsketillförsel.
Vid behandling av oavsiktlig överdos hos opioidnaiva personer skall naloxon eller andra opioidantagonister användas där detta är kliniskt indicerat och i enlighet med produktresuméerna för dessa läkemedel. Upprepad administrering av opioidantagonist kan erfordras om andningsdepressionen är långvarig.
Försiktighet måste iakttas vid användning av naloxon och andra opioidantagonister för behandling av överdos hos patienter som står på opioidbehandling, eftersom det finns en risk för akut utsättningssyndrom.
Om svår eller ihållande hypotension uppträder, bör man överväga möjligheten av hypovolemi, och tillståndet bör hanteras med lämplig parenteral vätskebehandling.
Muskelstelhet som påverkar andningen har rapporterats med fentanyl och andra opioider. Om detta inträffar kan endotrakeal intubation, assisterad ventilation och administrering av såväl opioidantagonister som muskelrelaxantia erfordras.
Farmakodynamik
Fentanyl är ett potent µ-opioidanalgetikum med snabbt insättande smärtlindring och kortvarig effekt. Fentanyl är ett ungefär 100 gånger mer potent analgetikum än morfin. De sekundära effekterna av fentanyl på centrala nervsystemet (CNS), och på respiratorisk och gastrointestinal funktion är de typiska för opioidanalgetika och betraktas som klasseffekter. Dessa kan inkludera andningsdepression, bradykardi, hypotermi, förstoppning, mios, fysiskt beroende och eufori.
Opioider kan påverka hypotalamus-hypofys-binjure- eller -gonadaxlarna. Några av de förändringar som kan ses är förhöjt serumprolaktin och lägre nivåer av kortisol och testosteron i plasma, vilket kan ge upphov till kliniska tecken och symtom.
De analgetiska effekterna av fentanyl är relaterade till blodkoncentrationen av den aktiva substansen; hos opioidnaiva patienter ligger de lägsta serumkoncentrationerna med analgetisk effekt i området 0,3–1,2 ng/ml, medan blodkoncentrationer på 10–20 ng/ml ger kirurgisk anestesi och djup andningsdepression.
Hos patienter med kronisk cancersmärta som står på stabila underhållsdoser av opioider, sågs statistiskt signifikant förbättring med avseende på skillnad i smärtintensitet för Abstral jämfört med placebo med början 10 minuter efter administration och framåt (se figur 1 nedan) med ett signifikant lägre behov av annan anfallskuperande behandling.
Figur 1 Genomsnittlig skillnad i smärtintensitet från baslinjen (± SE) för Abstral jämfört med placebo (mätt med en 0–10-gradig Likert-skala)
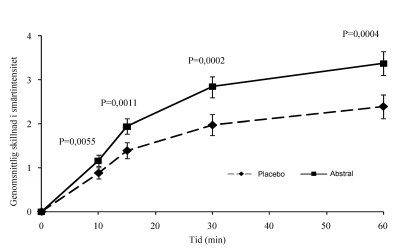
Abstrals säkerhet och effekt har utvärderats hos patienter som tagit läkemedlet i början av en episod med genombrottssmärta. Profylaktisk användning av Abstral inför förutsägbara smärtepisoder undersöktes inte vid de kliniska prövningarna.
Fentanyl ger, liksom alla µ-opioidreceptoragonister, en dosberoende andningsdepression. Denna risk är högre hos opioidnaiva patienter än hos patienter som lider av svår smärta eller står på kronisk opioidbehandling. Långtidsbehandling med opioider leder vanligen till utveckling av tolerans mot de sekundära effekterna.
Även om opioider generellt ökar tonus hos den glatta muskulaturen i urinvägarna, tenderar nettoeffekten att variera, så att man i vissa fall får urinträngningar, i andra fall svårighet att urinera.
Opioider ökar tonus och minskar de propulsiva kontraktionerna hos den glatta muskulaturen i magtarmkanalen. Detta leder till en förlängd passagetid genom magtarmkanalen, vilket kan vara orsaken till den obstiperande effekten hos fentanyl.
Farmakokinetik
Fentanyl är en starkt lipofil läkemedelssubstans som absorberas mycket snabbt genom munslemhinnan och långsammare genom magtarmkanalen. Peroralt administrerat fentanyl har en markant hepatisk och intestinal första passage-effekt.
Abstral är en snabblöslig resoriblettberedning. Abstral absorberas snabbt under cirka 30 minuter efter administrering. Den absoluta biotillgängligheten för Abstral har beräknats till 54 %. Den genomsnittliga maximala plasmakoncentrationen av fentanyl ligger i intervallet från 0,2 till 1,3 ng/ml (efter administrering av 100 till 800 µg Abstral) och uppnås efter 22,5 till 240 minuter.
Cirka 80–85 % av fentanylet är bundet till plasmaproteiner, främst α1-glykoprotein och i lägre grad albumin och lipoprotein. Distributionsvolymen för fentanyl vid steady state är cirka 3–6 l/kg.
Fentanyl metaboliseras främst via CYP3A4 till ett antal farmakologiskt inaktiva metaboliter, inklusive norfentanyl. Inom 72 timmar efter en intravenös fentanyladministrering utsöndras cirka 75 % av dosen i urinen, främst som metaboliter, och mindre än 10 % av dosen som oförändrad läkemedelssubstans. Cirka 9 % av dosen återfinns i faeces, främst som metaboliter. Totalt plasmaclearance för fentanyl är cirka 0,5 l/h/kg.
Efter administrering av Abstral är den huvudsakliga eliminationshalveringstiden för fentanyl cirka 7 timmar (intervall 3–12,5 timmar) och den terminala halveringstiden cirka 20 timmar (intervall 11,5–25 timmar).
Farmakokinetiken för Abstral har visats vara dosproportionell inom dosområdet 100–800 µg.
Farmakokinetiska studier har visat att flera tabletter är bioekvivalenta med enstaka tabletter i motsvarande dos.
Nedsatt njur/leverfunktion
Nedsatt lever- eller njurfunktion kan leda till förhöjda serumkoncentrationer. Äldre, kakektiska eller patienter med nedsatt allmäntillstånd kan ha en lägre fentanylclearance, vilket kan leda till en förlängd terminal halveringstid för substansen (se avsnitt Dosering och Varningar och försiktighet).
Prekliniska uppgifter
Data för säkerhetsfarmakologi och toxicitet vid upprepad dosering visar inte några särskilda risker för människa, som inte redan täcks av andra avsnitt i denna produktresumé. Djurstudier har visat nedsatt fertilitet och ökad dödlighet hos råttfoster. Inga teratogena effekter har dock påvisats.
Mutagenicitetstestning på bakterier och på gnagare gav negativa resultat. Liksom andra opioider uppvisade fentanyl mutagena effekter in vitro på däggdjursceller. En mutagen risk förefaller osannolik vid terapeutisk användning, eftersom effekterna endast inducerades av mycket höga koncentrationer.
Karcinogenicitetsstudier (26 veckor, dermal, ”alternative bioassay” på Tg.AC transgena möss; 2 års subkutan karcinogenicitetsstudie på råttor) med fentanyl visade inga fynd med onkogen potential.
Bedömning av bilder av hjärnan från karcinogenicitetsstudien på råttor visade hjärnlesioner på djur som fått höga doser av fentanylcitrat. Relevansen av dessa fynd för människor är okänd.
Innehåll
Kvalitativ och kvantitativ sammansättning
En sublingual resoriblett innehåller:
100 mikrogram fentanyl (som citrat)
200 mikrogram fentanyl (som citrat)
300 mikrogram fentanyl (som citrat)
400 mikrogram fentanyl (som citrat)
600 mikrogram fentanyl (som citrat)
800 mikrogram fentanyl (som citrat)
Förteckning över hjälpämnen
Mannitol (E421)
Silicifierad mikrokristallin cellulosa
Kroskarmellosnatrium
Magnesiumstearat
Blandbarhet
Ej relevant
Hållbarhet, förvaring och hantering
Hållbarhet
2 år
Särskilda förvaringsanvisningar
Förvaras vid högst 25 °C.
Förvaras i blistret i originalförpackningen. Fuktkänsligt.
Särskilda anvisningar för destruktion
Avfall skall kasseras på ett säkert sätt. Patienter/vårdgivare skall uppmanas att lämna tillbaka eventuellt oanvänt läkemedel till apoteket, där det skall kasseras i enlighet med nationella och lokala regelverk.
Egenskaper hos läkemedelsformen
Sublingual resoriblett
100 mikrogram sublingual resoriblett är en vit rund tablett
200 mikrogram sublingual resoriblett är en vit oval tablett
300 mikrogram sublingual resoriblett är en vit triangulär tablett
400 mikrogram sublingual resoriblett är en vit rombformad tablett
600 mikrogram sublingual resoriblett är en vit ”D”-formad tablett
800 mikrogram sublingual resoriblett är en vit kapselformad tablett
Förpackningsinformation
Resoriblett, sublingual 100 mikrog
Vit, rund tablett.
10 tablett(er) blister, 543:-, F
30 tablett(er) blister, 1737:13, F
Resoriblett, sublingual 200 mikrog
Vit, oval tablett.
10 tablett(er) blister, 539:93, F
30 tablett(er) blister, 1596:19, F
Resoriblett, sublingual 300 mikrog
Vit, triangulär tablett.
30 tablett(er) blister, 1594:65, F
Resoriblett, sublingual 400 mikrog
Vit, rombformad tablett.
30 tablett(er) blister, 1594:65, F
Resoriblett, sublingual 600 mikrog
Vit, "D"-formad tablett.
30 tablett(er) blister, 1595:68, F
Resoriblett, sublingual 800 mikrog
Vit, kapselformad tablett.
30 tablett(er) blister, 1596:09, F





