1. Det veterinärmedicinska läkemedlets namn
Canizol vet 200 mg och 400 mg tablett för hund
2. Sammansättning
200 mg tabletter:
Varje tablett innehåller:
Aktiv substans: Ketokonazol 200 mg
400 mg tabletter:
Varje tablett innehåller:
Aktiv substans: Ketokonazol 400 mg
Bruna knottriga, runda smaksatta tabletter som kan delas i halvor och fjärdedelar.
3. Djurslag
Hund
4. Användningsområden
Behandling av svampinfektioner i huden orsakade av:
-
Microsporum canis,
-
Microsporum gypseum,
-
Trichophyton mentagrophytes.
5. Kontraindikationer
Använd inte till djur med leversvikt.
Använd inte vid överkänslighet mot den aktiva substansen eller mot något av hjälpämnena.
6. Särskilda varningar
Särskilda varningar:
I sällsynta fall kan upprepad användning av ketokonazol orsaka resistens mot andra azoler.
Särskilda försiktighetsåtgärder för säker användning hos det avsedda djurslaget:
Användning av läkemedlet ska baseras på identifiering och resistensbestämning av målpatogen(er). Om detta inte är möjligt ska behandlingen baseras på epidemiologisk information och kunskap om känslighet hos målpatogenerna på gårdsnivå eller på lokal/regional nivå.
Användning av läkemedlet ska ske i enlighet med officiella, nationella och regionala antimikrobiella riktlinjer.
Behandling med ketokonazol hämmar koncentrationen av testosteron och ökar koncentrationen av progesteron och kan påverka avelsförmågan hos hanhundar under och några veckor efter behandling.
Behandling av hudsvampsinfektioner ska inte begränsas till behandling av infekterade djur. Det ska även omfatta desinfektion av omgivningen, eftersom sporer kan överleva i omgivningen under lång tid. Andra åtgärder som frekvent dammsugning, desinfektion av pälsvårdsutrustning och avlägsnande av allt potentiellt smittat material som inte kan desinfekteras minimerar risken för återfall eller spridning av infektionen.
En kombination av lokal behandling och behandling som påverkar hela kroppen rekommenderas.
Vid långvarig behandling ska leverfunktionen kontrolleras noggrant. Om symtom på nedsatt leverfunktion utvecklas ska behandlingen avbrytas omedelbart. Eftersom tabletterna är smaksatta ska de förvaras på en säker plats utom räckhåll för djur.
Särskilda försiktighetsåtgärder för personer som ger läkemedlet till djur:
Förvara blisterförpackningen i ytterkartongen för att förhindra åtkomst för barn. Delar (halvor/fjärdedelar) av tabletter ska förvaras i blisterförpackningen och användas för nästa dostillfälle.
Vid oavsiktligt intag, uppsök genast läkare och visa bipacksedeln eller etiketten.
Personer med känd överkänslighet mot ketokonazol bör undvika kontakt med läkemedlet. Tvätta händerna efter användning.
Andra försiktighetsåtgärder:
De hudsvampsinfektioner som anges i användningsområdet kan eventuellt överföras till människa. Iaktta god personlig hygien (tvätta händerna efter hantering av djuret och undvik direktkontakt med djur). Vid tecken på hudskador, kontakta läkare.
Dräktighet och digivning:
Studier på laboratoriedjur har visat belägg för fosterskadande effekter.
Säkerheten för detta läkemedel har inte fastställts hos dräktiga eller digivande tikar.
Användning rekommenderas inte under dräktighet.
Interaktioner med andra läkemedel och övriga interaktioner:
Ge inte tillsammans med syraneutraliserande medel och/eller H2-receptorantagonister (cimetidin/ranitidin) eller protonpumpshämmare (t.ex. omeprazol) som används mot sur mage, eftersom absorptionen av ketokonazol kan påverkas (absorption kräver en sur miljö).
Ketokonazol är en stark hämmare av cytokrom P450 3A4 (CYP3A4). Det kan minska utsöndringen av läkemedel som bryts ner av CYP3A4, och därmed ändra läkemedlens koncentration i blodplasma. Detta kan leda till ökad koncentration i blodplasma av t.ex. ciklosporin, makrocykliska laktoner (ivermektin, selamektin, milbemycin), midazolam, cisaprid, kalciumkanalblockerare, fentanyl, digoxin, makrolider, metylprednisolon eller kumarinantikoagulantia. Den ökade nivån i blodplasma av
de läkemedel som anges ovan kan förlänga effekternas och biverkningarnas varaktighet.
Å andra sidan kan förstärkare av cytokrom P450 öka hastigheten på ketokonazolnedbrytningen, t.ex. barbiturater eller fenytoin kan öka hastigheten på ketokonazolnedbrytningen och leda till minskad biotillgänglighet och således minskad effekt.
Ketokonazol kan minska koncentrationen av teofyllin i blodserum.
Ketokonazol hämmar omvandlingen av kolesterol till kortisol och kan därmed påverka doseringen av trilostan/mitotan hos hundar som samtidigt behandlas för hyperadrenokorticism (tillstånd där binjurarna producerar för mycket hormoner).
Det är inte känt i vilken omfattning denna påverkan av eller på andra läkemedel är relevant för hundar och katter, men vid avsaknad av data ska samtidig administrering av läkemedlet och dessa läkemedel undvikas.
Ge inga andra läkemedel till din hund utan att först rådfråga din veterinär.
Överdosering:
Vid överdosering kan följande effekter förekomma: anorexi (allvarlig brist på aptit), kräkningar, pruritus (klåda), alopeci (hårförlust) och ökning av vissa leverenzymer (ALAT och ALP).
7. Biverkningar
Hund:
|
Sällsynta (1 till 10 av 10 000 behandlade djur): |
Neurologiska teckena (t.ex. ataxi [bristande koordination], tremor [muskeldarrningar]) Apatia, anorexi (minskad aptit)a Hepatisk toxicitet (leverskada)a Kräkningara, diarréa |
|
Mycket sällsynta (färre än 1 av 10 000 behandlade djur, enstaka rapporterade händelser inkluderade): |
Störningar i endokrina systemet (antiandrogena effekterb, c, antiglukokortikoida effekterb) |
a Kan observeras vid standarddoser.
b Övergående. Ketokonazol hämmar omvandlingen av kolesterol till steroidhormoner som testosteron och kortisol på ett dosberoende och tidsberoende sätt.
c Se även avsnittet Särskilda försiktighetsåtgärder för säker användning hos det avsedda djurslaget för effekter på hanhundar för avel.
Det är viktigt att rapportera biverkningar. Det möjliggör fortlöpande säkerhetsövervakning av ett läkemedel. Om du observerar biverkningar, även sådana som inte nämns i denna bipacksedel, eller om du tror att läkemedlet inte har fungerat, meddela i första hand din veterinär. Du kan också rapportera eventuella biverkningar till innehavaren av godkännande för försäljning eller den lokala företrädaren för innehavaren av godkännandet för försäljning genom att använda kontaktuppgifterna i slutet av denna bipacksedel, eller via ditt nationella rapporteringssystem:
Läkemedelsverket
Box 26
751 03 Uppsala
Webbplats: www.lakemedelsverket.se
8. Dosering för varje djurslag, administreringssätt och administreringsväg(ar)
Ges via munnen.
200 mg tabletter:
10 mg ketokonazol per kg kroppsvikt per dag, som ges via munnen. Detta motsvarar 1 tablett per 20 kg kroppsvikt per dag.
400 mg tabletter:
10 mg ketokonazol per kg kroppsvikt per dag, som ges via munnen. Detta motsvarar 1 tablett per 40 kg kroppsvikt per dag.
Det rekommenderas att prov tas på djuret en gång i månaden under behandlingen och att den svampbekämpande behandlingen avbryts efter två negativa odlingar. När uppföljning genom provtagning inte är möjlig ska behandlingen fortsätta under en lämplig tidsperiod för att säkerställa att svampen är borta. Vid bestående hudförändringar efter 8 veckors behandling ska läkemedlet utvärderas på nytt av ansvarig veterinär.
För att säkerställa att rätt dos ges bör kroppsvikten fastställas så noggrant som möjligt.
Det rekommenderas att prov tas på djuret en gång i månaden under behandlingen och att den svampbekämpande behandlingen avbryts efter två negativa odlingar. När uppföljning genom provtagning inte är möjlig ska behandlingen fortsätta under en lämplig tidsperiod för att säkerställa att svampen är borta. Vid bestående hudförändringar efter 8 veckors behandling ska läkemedlet utvärderas på nytt av ansvarig veterinär.
9. Råd om korrekt administrering
Ges företrädelsevis tillsammans med mat, för maximal absorption.
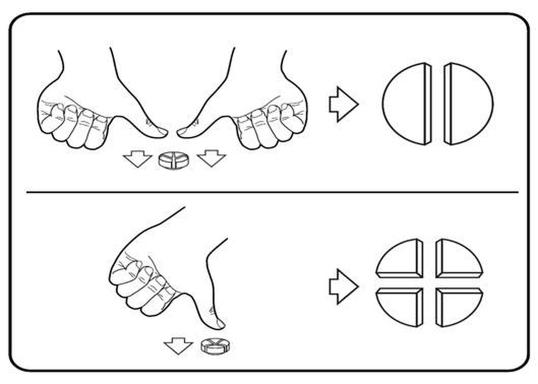
Tabletterna kan delas i halvor eller fjärdedelar för att säkerställa korrekt dosering. Lägg tabletten på ett plant underlag med den skårade sidan uppåt och den konvexa (rundade) sidan mot underlaget.
Dela i halvor: Applicera ett lätt tryck uppifrån med tummarnas toppar på båda sidor av tabletten för att bryta den i halvor.
Dela i fjärdedelar: Applicera ett lätt tryck uppifrån med ena tummens topp mitt på tabletten för att bryta den i fjärdedelar.
10. Karenstider
Ej relevant.
11. Särskilda förvaringsanvisningar
Förvaras utom syn- och räckhåll för barn.
Inga särskilda förvaringsanvisningar.
Använd inte detta läkemedel efter utgångsdatumet på kartongen efter Exp. Utgångsdatumet är den sista dagen i angiven månad.
Hållbarhet för delade tabletter: 3 dagar
12. Särskilda anvisningar för destruktion
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall.
Använd retursystem för kassering av ej använt läkemedel eller avfall från läkemedelsanvändningen i enlighet med lokala bestämmelser. Dessa åtgärder är till för att skydda miljön.
Fråga veterinär eller apotekspersonal hur man gör med läkemedel som inte längre används.
13. Klassificering av det veterinärmedicinska läkemedlet
Receptbelagt läkemedel.
14. Nummer på godkännande för försäljning och förpackningsstorlekar
Nummer på godkännande för försäljning:
200 mg: 49997
400 mg: 49998
Aluminium – PVC/PE/PVDC-blisterförpackning.
Kartong med 1, 2, 3, 4, 5, 6, 7, 8, 9 eller 10 blisterförpackningar, som innehåller 10 tabletter vardera.
Eventuellt kommer inte alla förpackningsstorlekar att marknadsföras.
15. Datum då bipacksedeln senast ändrades
2025-01-29
16. Kontaktuppgifter
Innehavare av godkännande för försäljning:
Dechra Regulatory B.V.
Handelsweg 25
5531 AE Bladel
Nederländerna
Tillverkare ansvarig för frisläppande av tillverkningssats:
Lelypharma B.V.
Zuiveringweg 42
8243 PZ Lelystad
Nederländerna
Genera d.d.
Svetonedeljska cesta 2
Kalinovica
10436 Rakov Potok
Kroatien
Lokal företrädare och kontaktuppgifter för att rapportera misstänkta biverkningar:
Dechra Veterinary Products Ab
Rotebergsvägen 9
192 78 Sollentuna
Sverige
Tel: +46 (0)8325355
För ytterligare upplysningar om detta läkemedel, kontakta den lokala företrädaren för innehavaren av godkännandet för försäljning.
Utförlig information om detta läkemedel finns i unionens produktdatabas (https://medicines.health.europa.eu/veterinary).



