Indikationer
Underhåll (barn och vuxna) av inhalationsanestesi med spontan eller kontrollerad ventilation. Desfluran är indicerat för inandning som induktion och/eller som underhåll av anestesi för patienter i slutenvården och för poliklinisk kirurgi hos vuxna och som underhåll av anestesi i slutenvård och öppen barnkirurgi. Desfluran rekommenderas inte för induktion av anestesi hos barn.
Kontraindikationer
Desfluran är kontraindicerat hos patienter med: Känd överkänslighet för halogenerade inhalationsanestetika, verifierad eller misstänkt genetisk benägenhet för malign hypertermi eller en sjukdomshistoria med bekräftad hepatit orsakad av halogenerade anestetika för inhalation eller måttlig till svår oförklarlig leverdysfunktion (t ex gulsot med feber och/eller eosinofili) efter anestesi med halogenerade inhalationsanestetika. Desfluran är kontraindicerat för induktion av anestesi hos pediatriska patienter på grund av frekvent förekomst av hosta, andningsuppehåll, apné, laryngospasm och ökad sekretion.
Dosering
Desfluran kan kombineras med övriga medel som normalt används vid anestesi. Premedicinering ges efter patientens behov, en ökad salivsekretion kan motivera användningen av ett antikolinergikum. Opioider eller bensodiazepiner minskar mängden desfluran som krävs för att ge anestesi. Samtidig tillförsel av lustgas reducerar behovet av desfluran, se tabell 1 nedan.
Underhållsdos
Dosen justeras efter patientens svar på behandlingen och är beroende av patientens allmäntillstånd, tillförsel av övriga farmaka inklusive lustgas samt den kirurgiska stimuleringen.
Dosering
Den minimala alveolära koncentrationen (MAC) av desfluran minskar med stigande patientålder. Desflurandosen ska justeras därefter. MAC har fastställts enligt tabell 1.
|
Ålder |
100% O2 |
60% N2O/40% O2 |
|
2 veckor |
9,2 ± 0,0 |
- |
|
10 veckor |
9,4 ± 0,4 |
- |
|
9 månader |
10,0 ± 0,7 |
7,5 ± 0,8 |
|
2 år |
9,1 ± 0,6 |
- |
|
3 år |
- |
6,4 ± 0,4 |
|
4 år |
8,6 ± 0,6 |
- |
|
7 år |
8,1 ± 0,6 |
- |
|
25 år |
7,3 ± 0,0 |
4,0 ± 0,3 |
|
45 år |
6,0 ± 0,3 |
2,8 ± 0,6 |
|
70 år |
5,2 ± 0,6 |
1,7 |
Den låga lösligheten medger snabba variationer i anestesidjup som lätt kan anpassas till den kirurgiska stimuleringen. Vid höga koncentrationer ger desfluran ökad hjärtfrekvens. Systoliskt blodtryck minskar gradvis med ökat anestesidjup.
Underhållsanestesi hos vuxna
2,5 - 8,5 % desfluran kan krävas vid administrering med syrgas eller syreberikad luft. Hos vuxna kan kirurgiskt anestesidjup bibehållas med en reducerad koncentration av desfluran när lustgas används samtidigt. Högre koncentrationer av desfluran kan vara indicerade. Man bör dock beakta risken för hypoxi och justera lustgas/syrgastillförsel. Underhållsdosen bör justeras gradvis i förhållande till den kliniska effekten.
Underhållsanestesi hos barn
Desfluran är indicerat för underhållsanestesi till spädbarn och barn. Kirurgiskt anestesidjup kan bibehållas hos barn med endtidala koncentrationer på 5,2 till 10 % desfluran med eller utan samtidig användning av lustgas. Om höga koncentrationer används tillsammans med lustgas är det ändå viktigt att säkerställa att den inhalerade blandningen innehåller minst 25 % syrgas.
Blodtryck och hjärtfrekvens vid underhållsanestesi
Blodtryck och hjärtfrekvens ska övervakas noggrant vid underhållsanestesi som del av kontrollen av anestesidjup (se avsnitt Varningar och försiktighet).
Dosering vid nedsatt njur- och leverfunktion
Desflurankoncentrationer på 1 - 4% i lustgas/syrgas har använts till patienter med kronisk njur- eller leverfunktionsnedsättning och under njurtransplantationskirurgi.
Behov av dosjustering till patienter med nedsatt njur- eller leverfunktion är inte att vänta då eliminationen via lever och njurar är minimal (se avsnitt Farmakokinetik).
Varningar och försiktighet
Hypovolemi bör korrigeras före anestesiinduktion.
Desfluran kan höja det intrakraniella trycket hos patienter med utrymmeskrävande lesioner och kan därför inte rekommenderas för neuroanestesi hos denna specifika patientkategori.
Malign hypertermi
Hos predisponerade individer kan inhalation av potenta anestesimedel utlösa ett hypermetaboliskt tillstånd i skelettmuskulaturen vilket kan leda till förhöjt syrgasbehov och ett kliniskt syndrom benämnt malign hypertermi. Desfluran har visats vara en potentiell utlösare av malign hypertermi. Tillståndet signaleras av hyperkapni och kan inkludera symtom som muskelrigiditet, takykardi, takypné, cyanos, arytmier och/eller labilt blodtryck. Vissa av dessa ospecifika symtom kan också uppträda vid lätt anestesi: akut hypoxi, hyperkapni och hypovolemi. Behandling av malign hypertermi innefattar utsättande av de utlösande substanserna, intravenös tillförsel av dantrolennatrium samt symtomatisk behandling. Njursvikt kan uppträda senare, och därför ska urinflödet övervakas och upprätthållas om möjligt. Desfluran ska inte ges till individer som man vet har en benägenhet att utveckla malign hypertermi. Malign hypertermi med fatal utgång har rapporterats med desfluran.
Perioperativ hyperkalemi
Ett samband har setts mellan användning av inhalationsanestetika, inklusive desfluran, och sällsynta ökningar av kaliumnivåerna i serum, vilket har resulterat i hjärtarytmier, vissa fatala, hos patienter postoperativt.
Patienter med latent såväl som pågående muskeldystrofi, särskilt Duchennes muskeldystrofi, förefaller vara mest känsliga. Samtidig användning av succinylkolin har förknippats med de flesta, men inte alla dessa fall. Dessa patienter hade också signifikanta förhöjningar av serumkreatininkinasnivåer och, i vissa fall, förändringar i urin i överensstämmelse med myoglobinuri. Trots liknande symtombild som malign hypertermi visade inga av dessa patienter tecken eller symtom på muskelrigiditet eller hypermetaboliskt tillstånd. Tidig och aggressiv insättning av behandling av hyperkalemi och resistenta arytmier rekommenderas, liksom fortsatt utredning av latent neuromuskulär sjukdom.
Anestesiinledning hos barn
Desfluran bör inte användas för anestesiinledning hos barn på grund av hög förekomst av hosta, andningsuppehåll, apné, laryngospasm och ökad sekretion.
Användning hos barn med bronkial hyperreaktivitet
Desfluran ska användas med försiktighet hos barn med astma eller som nyligen haft en infektion i de övre luftvägarna, på grund av risken för luftvägsförträngning och ökad lufvägsresistans.
Underhållsanestesi hos barn
På grund av den begränsade mängd data som finns hos icke-intuberade barn är desfluran inte godkänt för underhållsanestesi hos icke-intuberade barn. Användning av desfluran som underhållsanestesi via ansiktsmask eller larynxmask (LMA), medför hos barn en ökad risk för medelsvåra till svåra respiratoriska biverkningar, såsom hosta och laryngospasm (se avsnitt Biverkningar). Försiktighet skall därför vidtas om desfluran används som underhållsanestesi hos icke intuberade barn, särskilt hos barn som är 6 år gamla eller yngre. Då Suprane används vid pediatrisk anestesi är intubation att föredra. Laryngospasm och hosta är särskilt vanligt förekommande hos yngre barn och även efter avlägsnande av LMA-mask efter djup anestesi. Därför rekommenderas att larynxmasken skall avlägsnas först då barnet är fullt vaken.
Obstetrik
På grund av begränsad erfarenhet bör desfluran för närvarande ej användas i samband med obstetrisk kirurgisk anestesi. Ökad blodförlust efter livmoderskrapning har observerats i samband med inhalationsanestesi. Desfluran verkar relaxerande på uterus och reducerar blodflödet mellan uterus och placentan (se avsnitt Graviditet).
QT-förlängning
QT-förlängning, som i mycket sällsynta fall associerats med torsade de pointes, har rapporterats (se avsnitt Biverkningar). Försiktighet bör iakttas vid administrering av desfluran till patienter med medfödd eller förvärvad QT förlängning, hypokalemi eller samtidig användning av läkemedel som likaledes kan orsaka QT förlängning.
Försiktighet
Leverpåverkan, ikterus och levernekros med dödlig utgång har rapporterats efter narkos med halogenerade anestetika. Sådana reaktioner tycks representera en överkänslighetsreaktion mot dessa anestetika. Desfluran kan orsaka immunmedierad hepatit hos patienter som blivit sensibilisreade genom tidigare inhalation av halogenerade anestetika. Cirros, viral hepatit eller andra förekommande leversjukdomar kan vara skäl till att välja andra anestetika än halogenerande anestetika.
Hos patienter med kranskärlssjukdom är upprätthållande av normal hemodynamik viktigt för att undvika myokardiell ischemi. Markanta ökningar i puls, medelartärtryck samt av nivåerna av epinefrin och norepinefrin är förknippade med en snabb ökning av desflurankoncentrationerna. Desfluran ska inte användas som enda läkemedel för anestesiinduktion till patienter med risk för kranskärlssjukdom eller till patienter där ökad hjärtfrekvens eller förhöjt blodtryck inte är önskvärt. Det ska användas med annan behandling, företrädesvis intravenösa opioider och hypnotika.
Vid underhållsanestesi behöver ökning i hjärtfrekvens och blodtryck som inträffar efter snabba, stegvisa ökningar i endtidal koncentration av desfluran inte tyda på otillräcklig anestesi. Förändringar på grund av sympatisk aktivering försvinner inom cirka 4 minuter. Ökning i hjärtfrekvens och blodtryck som inträffar innan eller i frånvaro av en snabb ökning av desflurankoncentrationen kan tolkas som ytlig anestesi.
Hypotension och andningsdepression ökar när anestesin djupnar.
Liksom med andra snabbverkande anestetika ska det snabba uppvaknandet vid användning av desfluran tas i beaktande i fall där postanestetisk smärta kan förväntas.
Det ska säkerställas att tillräcklig analgesi har administrerats till patienten i slutet av behandlingen eller tidigt i det efterföljande omhändertagandet.
Hos barn kan uppvaknande ur anestesi framkalla ett kort tillstånd av agitation som kan försvåra samarbetet.
Liksom med alla halogenerade anestetika ska upprepad anestesi under en kort tidsperiod utföras med försiktighet.
Resurser och utrustning för upprätthållande av öppna luftvägar, artificiell ventilation, tillägg av syrgas och cirkulatorisk återupplivningsutrustning måste finnas omedelbart tillgängligt.
Observerade reaktioner hos andra än patienten, som oavsiktlig exponerats av desfluran, är yrsel, migrän, takyarytmi, palpitationer, brännskador i ögonen, övergående blindhet, encefalopati, ulcerativ keratit, okulär hyperemi, reducerad visuell synskärpa, ögonirritation, ögonsmärta, trötthet och brännande känsla i huden.
Interaktioner
Samtidig inhalation av N20 (lustgas) ökar effekten av desfluran (se tabell 1 i avsnitt Dosering). Desfluran förstärker effekten av både depolariserande och icke-depolariserande muskelrelaxantia varför dosen av dessa preparat skall justeras vid samtidig administrering av desfluran. Förslag på dosering för vanligen använda muskelrelaxantia ges i tabellen nedan.
|
Desflurankoncentration |
Pankuron |
Atrakurium |
Suxameton |
Vekuron |
|---|---|---|---|---|
|
0,65 MAC 60 % N2O/O2 |
0,026 |
0,133 |
data saknas* |
data saknas* |
|
1,25 MAC 60 % N2O/O2 |
0,018 |
0,119 |
data saknas* |
data saknas* |
|
1,25 MAC 100 % O2 |
0,022 |
0,120 |
0,360 |
0,019 |
*data saknas - inga data finns tillgängliga
Sedativa läkemedel
Tillförsel av fentanyl och midazolam minskar behovet av anestetika och reducerar MAC värdet för desfluran i enlighet med tabellen nedan. Det är möjligt att det kommer att finnas en liknande inverkan på MAC med andra opioider och sedativa läkemedel.
|
Läkemedel |
*MAC (%) |
% MAC-reduktion |
|---|---|---|
|
Inget fentanyl |
6,33 - 6,35 |
- |
|
Fentanyl (3 mikrogram/kg) |
3,12 - 3,46 |
46 - 51 |
|
Fentanyl (6 mikrogram/kg) |
2,25 - 2,97 |
53 - 64 |
|
Inget midazolam |
5,85 - 6,86 |
- |
|
Midazolam (25 mikrogram/kg) |
4,93 |
15,7 |
|
Midazolam (50 mikrogram/kg) |
4,88 |
16,6 |
* Inkluderar värden för åldersgruppen 18 – 65 år.
Kombinationen inhalationsanestetika och kalciumblockerare, såsom verapamil, ger en additativ negativ inotrop effekt. Kombinationen inhalationsanestetika och beta-receptorblockerande medel, såsom propranolol, kan orsaka blodtrycksfall.
Graviditet
Det finns ingen eller begränsad mängd data från användning av desfluran till gravida kvinnor. Desfluran har en relaxerande effekt på uterus och reducerar blodflödet mellan uterus och placenta. Djurstudier har visat reproduktionstoxikologiska effekter (se avsnitt Prekliniska uppgifter). SUPRANE är inte rekommenderat att användas under graviditet.
Amning
Det är okänt om desfluran utsöndras i humanmjölk. Det rekommenderas inte att använda SUPRANE under amning.
Trafik
Desfluran har stor påverkan på förmågan att framföra fordon och använda maskiner. Patienter bör informeras om att förmågan att framföra fordon och använda maskiner kan påverkas efter narkos.
Biverkningar
Som alla potenta inhalationsanestetika kan desfluran orsaka dosberoende kardio-respiratorisk depression. De flesta andra biverkningarna är milda och övergående. Illamående och kräkningar har observerats postoperativt, vilket är en vanlig följd av kirurgi och anestesi, och som kan bero på inhalationsanestetika, andra läkemedel som administrerats i samband med det kirurgiska ingreppet eller postoperativt eller på patientens svar på den kirurgiska behandlingen.
Andra dosberoende biverkningar inkluderar en ökad cerebral cirkulation som kan resultera i ökat cerebraltryck. Hos patienter med kranskärlssjukdom, är upprätthållande av normal hemodynamik viktigt för att undvika myokardischemi. Vid inhalations induktion har en hög incidens av respiratoriska biverkningar såsom hosta, ökad sekretion och laryngospasm rapporterats.
Biverkningsfrekvensen anges enligt följande: Mycket vanliga (≥1/10); vanliga (≥1/100 till <1/10); mindre vanliga (≥1/1000 till <1/100), sällsynta (≥1/10 000 till <1/1000; mycket sällsynta (<1/10 000, ingen känd frekvens (biverkningar rapporterade efter marknadsintroduktion).
|
Biverkning |
||
|---|---|---|
|
Organsystemklassystem |
MedDRA-term |
Frekvens |
|
Infektioner och infestationer |
Faryngit |
Vanliga |
|
Blodet och lymfsystemet |
Koagulopati |
Ingen känd frekvens |
|
Metabolism och nutrition |
Hyperkalemi Hypokalemi Metabolisk acidos |
Ingen känd frekvens |
|
Psykiska störningar |
Agitation Delirium |
Mindre vanliga Ingen känd frekvens |
|
Centrala och perifera nervsystemet |
Huvudvärk Yrsel Kramper |
Vanliga Mindre vanliga Ingen känd frekvens |
|
Ögon |
Konjunktivit |
Vanliga |
|
Hjärtat |
QT förlängning Nodulär arytmi Bradykardi Takykardi Hypertension Myokardinfarkt Myokardiell ischemi Arytmi Hjärtstillestånd Torsade de pointes Ventrikulär svikt Ventrikulär hypokinesi Förmaksflimmer |
Vanliga Vanliga Vanliga Vanliga Vanliga Mindre vanliga Mindre vanliga Mindre vanliga Ingen känd frekvens |
|
Blodkärl |
Vasodilatation Malign hypertension Blödning Hypotension Chock |
Mindre vanliga Ingen känd frekvens |
|
Andningsvägar, bröstkorg och mediastinum |
Apné+ Hosta+ Laryngospasm* Hypoxi+ Andningssvikt Andnöd Bronkospasm |
Vanliga Vanliga Vanliga Mindre vanliga Ingen känd frekvens |
|
Magtarmkanalen |
Kräkningar+ Illamående+ Hypersekretion av saliv+ Akut pankreatit Buksmärta |
Mycket vanliga Mycket vanliga Vanliga Ingen känd frekvens |
|
Lever och gallvägar |
Leversvikt Hepatisk nekros Hepatit Cytolytisk hepatit Kolestas Gulsot Onormal leverfunktion Leverrubbning |
Ingen känd frekvens |
|
Hud och subkutan vävnad |
Urtikaria Erytem |
Ingen känd frekvens |
|
Muskuloskeletala systemet och bindväv |
Myalgi Rhabdomyolys |
Mindre vanliga Ingen känd frekvens |
|
Allmänna symtom och/eller symtom vid administreringsstället |
Malign hypertermi Asteni Sjukdomskänsla |
Ingen känd frekvens |
|
Undersökningar |
Ökat kreatininfosfokinas ST-T-förändring i EKG T-vågsinversion i EKG Ökat alaninaminotransferas Ökat aspartataminotransferas Förhöjt blodbilirubin Onormalt koagulationstest Ammoniumökning |
Vanliga Ingen känd frekvens |
|
Skador och förgiftningar och behandlingskomplikationer |
Postoperativ agitation |
Ingen känd frekvens |
*rapporterat under induktion med desfluran
+rapporterat under induktion och upprätthållande med desfluran
Glukosförhöjning
Liksom för andra halogenerade anestesimedel har desfluran associerats med en viss glukoshöjning under operation.
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till Läkemedelsverket, men alla kan rapportera misstänkta biverkningar till Läkemedelsverket, www.lakemedelsverket.se. Postadress
Läkemedelsverket
Box 26
751 03 Uppsala
Överdosering
Symtom på överdosering av desfluran kan yttra sig som fördjupad anestesi, kardiell och/eller respiratorisk depression hos patienter med spontanandning, och kardiell depression hos ventilerade patienter hos vilka hyperkapni och hypoxi kan inträffa först i ett sent skede. Vid fall av överdosering, eller vad som förefaller vara överdosering, ska följande åtgärder vidtas:
1. Avbryt eller minimera exponeringen för desfluran.
2. Upprätta en fri luftväg och initiera assisterad eller kontrollerad ventilation med 100 % syrgas.
3. Stöd och upprätthåll adekvat hemodynamik.
Farmakodynamik
Desfluran är ett anestesimedel för inhalationsanestesi. Kemiskt är desfluran en halogenerad metyletyleter. Desfluran är inte eldfarligt eller explosivt i kliniskt använda koncentrationer. Desfluran är en färglös, flyktig vätska med en kokpunkt på 22,8°C. Desfluran är kemiskt stabil. Desfluran reagerar inte kemiskt eller fysikaliskt med rostfritt stål. Desfluran har en god anestetisk effekt. Induktionstiden är kort och uppvaknandet sker snabbt. Uppvaknandet förlängs av samtidigt tillförda anestesimedel med sedativ-hypnotisk verkan som bensodiazepiner, opioider etc. Desfluran ger en dosberoende reduktion av blodtryck och andning. Desfluran ger ej upphov till epileptogen EEG-aktivitet. Desfluran kan användas tillsammans med vasokonstriktorer och inotropa droger och syns inte öka förekomsten av extrasystolier.
Farmakokinetik
Undersökningar har visat att endast 0,02% av upptaget desfluran metaboliseras. Endast marginella ökningar av oorganisk fluorid kan ses i serum och urin.
Prekliniska uppgifter
I djurförsök har en möjlig anestesirelaterad fetotoxisk effekt visats efter ca 40 timmars kumulativ exposition (MAC-timmar). Inga effekter har observerats vid 10 timmars kumulativ exposition till råtta eller kanin.
Publicerade djurstudier (inklusive primater) vid doser som resulterat i lätt till måttlig anestesi visar att användningen av anestesiläkemedel under hjärnans snabba tillväxtperiod eller synaptogenes resulterar i cellförlust hos den utvecklande hjärnan som kan associeras till långvariga kognitiva brister. Den kliniska betydelsen av dessa prekliniska fynd är okänd.
Innehåll
En flaska innehåller 240 ml desfluran.
Blandbarhet
Ej tillämpligt.
Miljöpåverkan
Desfluran
Miljörisk:
Användning av desfluran har bedömts medföra försumbar risk för miljöpåverkan.
Nedbrytning:
Desfluran är potentiellt persistent.
Bioackumulering:
Desfluran har låg potential att bioackumuleras.
Läs mer
Detaljerad miljöinformation
Detailed background information
Due to the prescribed application regime of the medicine and its physical-chemical properties, the parent compound desflurane (CAS 57041-67-5) is mainly emitted to the air compartment. Indeed, a minor amount of desflurane and its metabolites fluoride and trifluoroacetic acid (TFA) are maybe emitted down-the-drain. Only the latter releases, parent and metabolite, have been examined in the following risk classification. Thus, only the potential risk to the aquatic compartment is addressed here.
Environmental Risk Classification
Predicted Environmental Concentration (PEC): parent compound
PEC is calculated according to the following formula:
PEC (μg/L) = (A*109*(100-R))/(365*P*V*D*100) = 1.5*10-6*A(100-R)
PEC = 0.000045 μg/L
Where:
A = 1466.9 kg * 0.02% (total sold amount API in Sweden year 2017, data from IQVIA (2018); reduced by fraction excreted). The 0.02% represents a worst-case assumption; Justification on reduction sees metabolism data below.
R = removal rate (due to loss by adsorption to sludge particles, by volatilization, hydrolysis or biodegradation) = 0 %. This value represents a worst-case assumption due to volatilisation; Justification sees data below.
P = number of inhabitants in Sweden = 9 *106
V (L/day) = volume of wastewater per capita and day = 200 (ECHA default) (ECHA, 2016)
D = factor for dilution of waste water by surface water flow = 10 (ECHA default) (ECHA, 2016)
Predicted No Effect Concentration (PNEC): parent compound
Ecotoxicological studies
For desflurane information on aquatic toxicity is not available.
Algae:
Not available
Crustacean:
Acute toxicity
Not available
Chronic toxicity
Not available
Fish:
Acute toxicity
Not available
Chronic toxicity
Not available
Environmental risk classification (PEC/PNEC ratio): parent compound
Based on the fact that for desflurane information on aquatic toxicity is not available, the phrase “Risk of environmental impact of desflurane cannot be excluded, since no ecotoxicity data are available” has to be chosen.
However, according to the European Medicines Agency guideline on environmental risk assessment of medicinal products (EMA/CHMP/SWP/4447/00), use of desflurane is unlikely to represent a risk for the environment, because the predicted environmental concentration (PEC) is below the action limit 0.01 μg/L.
Moreover, the available information for the metabolite TFA (see below), justifies the phrase "Use of desflurane has been considered to result in insignificant risk."
Therefore, the use of desflurane under the prescribed application regime is unlikely to represent a risk for the environment, although, due to the missing of experimentally determined ecotoxicity data for the parent compound, an environmental impact of desflurane cannot be completely ruled out.
Overall, the distinct difference to the action limit for the parent compound as well as the low risk characterization ratio for the metabolite justifies the phrase "Use of desflurane has been considered to result in insignificant risk."
Predicted Environmental Concentration (PEC): metabolite TFA
PEC is calculated according to the following formula:
PEC (μg/L) = (A*109*(100-R))/(365*P*V*D*100) = 1.5*10-6*A(100-R)
PEC = 0.000030 μg/L
Where:
A = 1466.9 kg * 114.02 g/mol / 168.04 g/mol * 0.02% (total sold amount API in Sweden year 2017, data from IQVIA (2018); reduced by fraction excreted). The 0.02% represents a worst-case assumption; Justification on reduction sees metabolism data below.
R = removal rate (due to loss by adsorption to sludge particles, by volatilization, hydrolysis or biodegradation) = 0 %
P = number of inhabitants in Sweden = 9 *106
V (L/day) = volume of wastewater per capita and day = 200 (ECHA default) (ECHA, 2016)
D = factor for dilution of waste water by surface water flow = 10 (ECHA default) (ECHA, 2016)
Predicted No Effect Concentration (PNEC): metabolite TFA
Ecotoxicological studies
Review of effects of TFA on environmental organisms is published by Solomon et al. (2016), which cites effect values based on biomass given by Berends et al (1999). A registration dossier under REACh is available on the ECHA website (ECHA, 2018) describing several aquatic toxicity studies with TFA (studies performed with sodium trifluoroacetate; concentrations re-calculated for TFA). It should be noted that the original study reports could not be evaluated. Instead, only information publicly disseminated on the ECHA website served as basis of this assessment. Therefore, definitive quality and reliability cannot be assessed from this limited information.
However, the registrants regarded the studies as reliable.
Algae:
Green alga (Pseudokirchneriella subcapita (synonym Raphidocelis subcapitata) formerly known as Selenastrum capricornutum) (OECD 201, GLP, including analytical monitoring) (ECHA, 2018)
EC50 72 h (growth rate) =237 mg/L
EC10 72 h (growth rate) = 5.6 mg/L
Marine alga (Phaeodactylum tricornutum) (OECD 201, GLP, no analytical monitoring, effect values based on nominal concentrations) (ECHA, 2018)
EC50 96 h (growth rate) > 97 mg/L
NOEC 96 h (growth rate) = 97 mg/L
Blue green alga (Anabaena flos-aquae) (US-EPA 540/09-82-020, GLP, including analytical monitoring, effect values based on nominal concentrations) (Smyth et al., 1994)
EC50 120 h (growth rate) > 1997 mg/L
NOEC 120 h (growth rate) = 499 mg/L
Crustacean (Daphnia magna):
Acute toxicity
EC50 48 h (immobility) > 999 mg/L (nominal concentration, OECD 202, GLP, limit test with 1200 mg/L sodium trifluoroacetate, including analytical monitoring)
Chronic toxicity
NOEC 21 days (reproduction rate, survival of adults) > 25 mg/L (nominal concentration, OECD 211, GLP, including analytical monitoring, no effect observed at highest concentration tested)
Fish:
Acute toxicity
Zebra fish (Danio rerio) LC50 96 h > 999 mg/L (nominal concentration, OECD 203, GLP, limit test with 1200 mg/L sodium trifluoroacetate, including analytical monitoring)
Chronic toxicity
No experimental results available
According to REACh Technical Guidance Document, Chapter R.10 (ECHA, 2008) an assessment factor of 50 applies to the lowest of two long term results (e.g. EC10 or NOECs) representing two trophic levels when such results have been generated covering that level showing the lowest L(E)C50 in the short-term tests. NOEC of the most recent study with the green alga Raphidocelis subcapitata has been used for this calculation since it is the most sensitive of the three tested species and the most reliable study. This PNEC is regarded a worst case estimate. For comparison, the REACh dossier derives a PNEC of 0.56 mg/L based on the EC10 of 5.6 mg/L and using an AF of 10.
PNECsurface water = lowest NOEC/50 = 112 µg/L
Environmental risk classification (PEC/PNEC ratio): metabolite TFA
According to the European Medicines Agency guideline on environmental risk assessment of medicinal products (EMA/CHMP/SWP/4447/00), TFA as a relevant metabolite from the use of desflurane is unlikely to represent a risk for the environment, because the predicted environmental concentration (PEC) is below the action limit 0.01 μg/L.
Moreover, based on the available information for the metabolite TFA,
PEC/PNEC = 0.000030/112 = 0.00000027, i.e. PEC/PNEC ≤ 0.1 which justifies the phrase "Use of desflurane has been considered to result in insignificant risk."
Degradation
Biotic degradation
Ready degradability:
For desflurane studies on ready biodegradability are not available.
For the metabolite TFA biodegradation studies are presented in the REACh dossier (ECHA, 2012):
Test result: 0 % degradation within 28 days (OECD 301D).
These results indicate that desflurane as well as TFA can be regarded as not readily biodegradable.
Inherent degradability:
Information on inherent biodegradability of desflurane is not available.
For the metabolite TFA a modified SCAS Test is presented in the REACh dossier (ECHA, 2012) indicating that TFA is not biodegraded.
Simulation studies:
STP simulation studies and test results in water, sediment and total system are not available.
TFA was shown to be persistent in water compartments since it was not biodegraded during a year-long study using laboratory aquatic microcosms and ecosystem sediment-water systems (Ellis et al., 2001).
Abiotic degradation
Hydrolysis:
Information on hydrolysis is not available.
Photolysis:
Information on photolysis in water is not available.
Justification if R not equal to 0, e.g. modelling results using SimpleTreat:
As desflurane is not readily biodegradable, and simulation studies are not available, the default value was used for removal rate R = 0. However, this is considered to represent a worst-case approach for desflurane, as modelling results using SimpleTreat suggest that within STP about 93.2% is emitted to air, 0.9% to sludge, and only 5.9% to water.
As the metabolite TFA is not readily biodegradable, simulation studies are not available, and microcosms/field studies suggest persistence in the environment, the default value was used for removal rate R = 0. Modelling results using SimpleTreat suggest that within STP about 0.01% is emitted to air, 0.238% to sludge, and 99.8% to water.
Justification of chosen degradation phrase:
Based on the information that desflurane as well as its metabolite TFA are not readily biodegradable, and reliable simulation studies are not available, the phrase "desflurane is potentially persistent" is thus chosen.
Photodegradation:
In the atmosphere desflurane could be removed by chemical reaction with radicals, by photolysis and by wet or dry deposition. The degradation time is assumed to be limited by the reaction with the hydroxyl radical (OH). The following rate coefficients kOH are described:
EpiSuite (estimation): 6E-15 cm3/molecule-sec at 298 K
Langbein et al. (1999): 4.4E-15 cm3/molecule-sec at 298 K
Sulbaek Andersen et al. (2010) 3.55E-15 cm3/molecule-sec at 272 K
Sulbaek Andersen et al. (2012) 3.7E-15 cm3/molecule-sec at 296 K
The life-times given in the literature are between 5.8 and 21.4 years depending on the rate constant, OH radical concentration, and temperature.
For TFA the estimated rate coefficient kOH is 0.52E-012 cm3/molecule-sec at 298 K corresponding to a half-life of 31 d (EpiSuite, AOPWIN). The major elimination pathway of TFA in air is rainout.
Adsorption and desorption to soil
The soil adsorption coefficient (Koc) of desflurane was calculated by ACD/Labs to be 251 L/kg. Estimations via EpiSuite show Koc values of 97.54 L/kg (MCI method) and 31.5 L/kg. (Kow method with a logKow of 1.2). Using the logPow and the recommended QSAR of the TGD for non-hydrophobics, results in a Koc of 90.4 L/kg. Thus, adsorption of desflurane to soil and sediment is assumed to be low.
For TFA the soil adsorption coefficient (Koc) was estimated via EpiSuite. This estimation results in values of 3.231 L/kg (MCI method) and 2.706 L/kg. (Kow method with a logKow of 0.5). Using the logPow and the recommended QSAR of the TGD for non-hydrophobics, results in a Koc of 19.1 L/kg. However, the logPow and the Koc of this structure may be sensitive to pH, and thus may vary significantly. In a screening test presented in the REACh dossier (ECHA, 2012), no adsorption to three different standard soils was observed. In addition, in soil retention studies on a total of 54 soil samples the Kd were ranged between 0.17 to 20 L/kg for all soil location (Richey et al., 1997). The results indicate that retention of TFA by soil surfaces is dependent upon pH, soil organic matter and mineral surfaces and the presence of other anions in soil solution. Overall, TFA can be considered as a mobile organic compound in the majority of soils.
Volatilisation
Distribution of desflurane between air and water (Henry’s law constant) was estimated from the ratio of the vapour pressure to the water solubility. The calculated value of 7630 Pa m3/mole at 25 °C, resulting in an air-water partitioning coefficient of 1.54 at 12°C, indicates a rapid and significant volatilization from water.
For the metabolite TFA experimental Henrys law constants are presented in the REACh dossier (ECHA, 2018): the values ranges from 5800 mol/dm3/atm (Kutsuna and Hori, 2008) and 8950 mol/dm3/atm (Bowden et al., 1996) corresponding to a value of 0.00713 and 0.0112 Pa m3/mol at 25 °C, respectively. This indicates a very low the volatility potential of the metabolite.
Bioaccumulation
Bioconcentration factor (BCF):
An experimental bioconcentration study for desflurane is not available.
As well, an experimental bioconcentration study for the metabolite TFA is not available, that would enable the derivation of a reliable BCF. However, results on the incorporation of TFA into freshwater sediment organisms as well as estimation data (EpiSuite/BCFBAF) indicate only an insignificant potential for bioconcentration in aquatic species.
Partitioning coefficient:
An experimental study according to OECD 107 on the logPow of desflurane determined a logPow > 1.8 (Baxter, 2012). With the analytical method performed in this study it was not possible to detect desflurane in the water phase, thus no exact value could be determined. However, this experimentally determined lower limit of the logPow is similar to the calculated values of 1.88 at 25°C (ACD/Labs) and 1.2 (EpiSuite/KOWWIN v1.67).
Desflurane: estimated Log Dow = 1.88 at pH 7
For TFA estimated values for logPow of 0.5 (EpiSuite/KOWWIN v1.68) and 1.35 ± 0.38 (ACD/Labs) could be calculated. However, the partitioning is pH dependent as TFA dissociates in water and is expected to exist almost entirely in the anion form (dissociation constant pKa = 0.52); pH-dependence could be calculated using ACD/Labs.
TFA: estimated Log Dow = - 2.4 at pH 7
Justification of chosen bioaccumulation phrase:
Since log Dow < 4 at pH 7, desflurane has a low potential for bioaccumulation. Moreover, toxicokinetic data from humans show that desflurane does not remain in human bodies but is released back into the air.
Since log Dow < 4 at pH 7, TFA has a low potential for bioaccumulation.
Excretion (metabolism)
Desflurane predominantly leaves the human body via pulmonary exhalation and reaches the atmosphere as the main target compartment. Scientific literature demonstrates that the administered desflurane is mainly emitted unchanged into the atmosphere. Only a minor fraction of fluranes is excreted unchanged in urine (Saber and Sorig Hougaard, 2009).
The metabolism of desflurane has been comprehensively reviewed (Koblin, 1992; Kenna and van Pelt, 1994). Desflurane is metabolized to fluoride and trifluoroacetic acid (TFA), which is excreted via urine. The extent of desflurane metabolism has been estimated to be one-tenth that of isoflurane (Sutton et al., 1991), corresponding to approximately 0.02 – 0.2% (Kharasch, 1996), which is in alignment to SPC Sweden.
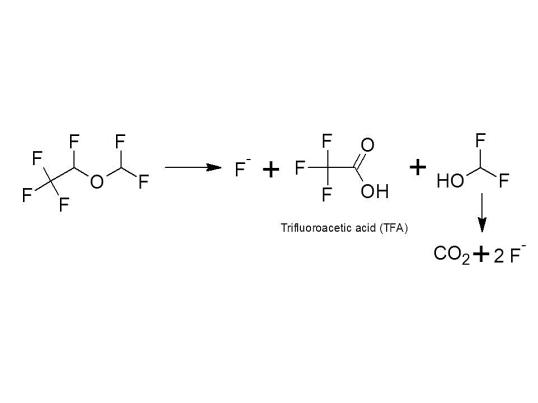
The portion of urinary organic fluorine is factor 5 below that of isoflurane (Sutton et al, 1991); for isoflurane the portion of organic fluorine is < 0.1% (Holaday and Fiserova-Bergerova, 1979). Thus, into wastewater, desflurane is excreted assuming all organic fluorine is unchanged parent or TFA – as a worst-case assumption - to < 0.02% as parent compound or as metabolite trifluoroacetic acid (TFA). The pharmacological activity of the metabolite is not known.
A reduction of A (total sold amount API in Sweden 2017) in the PEC calculation is justified based on excretion/metabolism as follows:
Desflurane (Parent):
A = 1466.9 kg * 0.02%
TFA (Metabolite):
A = 1466.9 kg * MW(metabolite)/MW(parent) * M
= 1466.9 kg * 114.02 g/mol / 168.04 g/mol * 0.02%
PBT/vPvB assessment
As both Desflurane and its metabolite TFA have low potential for bioaccumulation, they do not fulfil the criteria for PBT and/or vBvP substances and thus should not be flagged.
According to the established EU criteria, the medicine should not be regarded as a PBT/vPvB substance.
References
Baxter, 2012. Experimental study report: Desflurane, Partition Coefficient n-Octanol/Water (OECD 107), Shake Flask Method. Performed by Siemens AG, Prozess-Sicherheit, Industriepark Höchst, B 596 & B 598, 65926 Frankfurt am Main, Germany.
Berends AG, Boutonnet JC, De Rooij CG, and Thompson RS, 1999. Toxicity of trifluoroacetate to aquatic organisms. Environmental Toxicology and Chemistry. 18:1053–1059
Bowden DJ, Clegg SL and Brimblecombe P, 1996. The Henry's law constant of trifluoroacetic acid and its partitioning into liquid water in the atmosphere. Chemosphere, 32, 405-420
ECHA, European Chemicals Agency, 2008. Guidance on information requirements and chemical safety assessment. https://echa.europa.eu/documents/10162/13632/information_requirements_r10_en.pdf/bb902be7-a503-4ab7-9036-d866b8ddce69
ECHA, European Chemicals Agency, 2016. Guidance on information requirements and chemical safety assessment chapter R.16: Environmental exposure assessment version 3.0 February 2016. https://echa.europa.eu/documents/10162/13632/information_requirements_r16_en.pdf/b9f0f406-ff5f-4315-908e-e5f83115d6af
ECHA, European Chemicals Agency, 2018. REACH-Registrationdossier trifluoroacetic acid (CAS 76-05-1), last modified 2018-11-14. European Chemicals Agency, Helsinki, Finland. Publicly available under: https://www.echa.europa.eu/web/guest/registration-dossier/-/registered-dossier/5203
Ellis DA, Hanson ML, Sibley PK, Shahid T, Fineberg NA, Solomon KR, Muir DC and Mabury SA, 2001. The fate and persistence of trifluoroacetic and chloroacetic acids in pond waters. Chemosphere, 42, 309-318.
Holaday DA, Fiserova-Bergerova V, 1979. "Fate of fluorinated metabolites of inhalation anesthetics in man." Drug Metab Rev 9(1): 61-78.
IQVIA, 2018. Consumption assessment in kg for input to enviromental classification - updated 2018 (data 2017), Project 1048212
Kenna JG and van Pelt FNAM, 1994. The metabolism and toxicity of inhaled anaesthetic agents. Anaesthetic Pharmacology Review, 2, 29-42
Kharasch ED, 1996. Metabolism and toxicity of the new anesthetic agents. Acta Anaesthesiologica Belgica, 47, 7-14.
Koblin DD, 1992. Characteristics and implications of desflurane metabolism and toxicity. Anesth Analg, 75, S10-16
Kutsuna S and Hori H, 2008. Experimental determination of Henry's law constants of trifluoroacetic acid at 278–298 K. Atmospheric Environment, 42, 1399-1412
Langbein T, Sonntag H, Trapp D, Hoffmann A, Malms W, Roth EP, Mors V and Zellner R, 1999. Volatile anaesthetics and the atmosphere: atmospheric lifetimes and atmospheric effects of halothane, enflurane, isoflurane, desflurane and sevoflurane. British Journal of Anaesthesia, 82, 66-73
Richey DG, Driscoll CT and Likens GE, 1997. Soil Retention of Trifluoroacetate. Environ Sci Technol, 31, 1723-1727
Saber AT and Sorig Hougaard K, 2009. 141. Isoflurane, sevoflurane and desflurane. Arbete och Hälsa, 43
Smyth DV, Thompson R S, E Gillings1994. Sodium Trifluoroacetate: Toxicity to the Blue-green Alga, Anabaena Flos-aquae, and to the Freshwater Diatom, Navicula Pelliculosa, with Cover Letter dated 06/27/94. Brixham Environmental Lab., NTIS report: OTS0557458.
Solomon KR, Velders GJM, Wilson SR, Madronich S, Longstreth J, Aucamp PJ, Bornman JF. 2016. Sources, fates, toxicity, and risks of trifluoroacetic acid and its salts: Relevance to substances regulated under the montreal and kyoto protocols. Journal of Toxicology and Environmental Health - Part B: Critical Reviews. 19(7):289-304
Sulbaek Andersen MP, Nielsen OJ, Karpichev B, Wallington TJ and Sander SP, 2012. Atmospheric Chemistry of Isoflurane, Desflurane, and Sevoflurane: Kinetics and Mechanisms of Reactions with Chlorine Atoms and OH Radicals and Global Warming Potentials. J Phys Chem A. 116(24):5806-5820
Sulbaek Andersen MP, Sander SP, Nielsen OJ, Wagner DS, Sanford TJ, Jr. and Wallington TJ, 2010. Inhalation anaesthetics and climate change. British Journal of Anaesthesia, 105, 760-766.
Sutton TS, Koblin DD, Gruenke LD, Weiskopf RB, Rampil IJ, Waskell L and Eger EI, 2nd, 1991. Fluoride metabolites after prolonged exposure of volunteers and patients to desflurane. Anesth Analg, 73, 180-185
Hållbarhet, förvaring och hantering
Förvaras stående med locket väl tillslutet. Desfluran ska endast tillföras via specialförgasare avsedd för desfluran.
SUPRANE, liksom andra halogenerade inhalationsanestetika, har rapporterats interagera med torr soda i koldioxidabsorbern och bilda kolmonoxid. Detta kan i ett återandningssystem medföra ökad risk för förhöjda karboxyhemoglobinvärden. Färsk (fuktig) soda i koldioxidabsorbern ska därför användas. Fallrapporter har visat att bariumhydroxidlime och sodalime uttorkas när färska gaser passerar genom CO2-behållaren vid högt flöde över många timmar eller dagar.





