Indikationer
Icke-småcellig lungcancer (Non-Small Cell Lung Cancer, NSCLC)
Tarceva är indicerat som första linjens behandling av patienter med lokalt avancerad eller metastaserad icke-småcellig lungcancer (NSCLC) med EGFR-aktiverande mutationer.
Tarceva är också indicerat för underhållsbehandling hos patienter med lokalt avancerad eller metastaserande NSCLC med EGFR-aktiverande mutationer och stabil sjukdom efter första linjens kemoterapi.
Tarceva är också indicerat för behandling av patienter med lokalt avancerad eller metastaserad NSCLC som har sviktat på minst en tidigare kemoterapibehandling. Hos patienter med tumörer utan EGFR-aktiverande mutationer är Tarceva indicerat när andra behandlingsalternativ inte anses lämpliga.
När Tarceva förskrivs bör hänsyn tas till faktorer som är förknippade med förlängd överlevnad.
Någon överlevnadsfördel eller andra kliniskt relevanta effekter av behandlingen har inte påvisats hos patienter med epidermal tillväxtfaktorreceptor (EGFR)-IHC-negativa tumörer (se avsnitt Farmakodynamik).
Pankreascancer
Tarceva i kombination med gemcitabin är indicerat för behandling av patienter med metastaserad pankreascancer.
När Tarceva förskrivs bör hänsyn tas till faktorer som är förknippade med förlängd överlevnad (se avsnitt Dosering och Farmakodynamik).
Ingen överlevnadsfördel kunde visas för patienter med lokalt avancerad sjukdom.
Kontraindikationer
Överkänslighet mot erlotinib eller mot något hjälpämne som anges i avsnitt Innehåll.
Dosering
Behandling med Tarceva bör ske under överinseende av en läkare med erfarenhet av cancerbehandling.
Patienter med icke-småcellig lungcancer
Test för EGFR-mutation bör genomföras i enlighet med de godkända indikationerna (se avsnitt Indikationer).
Den rekommenderade dagliga dosen av Tarceva är 150 mg som tas minst en timma före eller två timmar efter födointag.
Patienter med pankreascancer
Den rekommenderade dagliga dosen av Tarceva är 100 mg som tas minst en timma före eller två timmar efter födointag, i kombination med gemcitabin (se gemcitabins produktresumé för indikationen pankreascancer).
Hos patienter som inte utvecklar hudutslag (rash) inom de första 4-8 veckornas behandling ska fortsatt behandling med Tarceva utvärderas på nytt (se avsnitt Farmakodynamik).
Om dosjustering krävs ska dosen minskas stegvis med 50 mg i taget (se avsnitt Varningar och försiktighet).
Tarceva finns tillgängligt i styrkorna 25 mg, 100 mg och 150 mg.
Samtidig användning av substrat och modulatorer för CYP3A4 kan kräva dosjustering (se avsnitt Interaktioner).
Nedsatt leverfunktion
Erlotinib elimineras genom levermetabolism och utsöndring via gallan. Även om exponering av erlotinib var likadan hos patienter med måttligt nedsatt leverfunktion (Child-Pugh score 7-9) jämfört med patienter med adekvat leverfunktion, ska försiktighet iakttas när Tarceva administreras till patienter med nedsatt leverfunktion. Dosreduktion eller avbrytande av behandling med Tarceva ska övervägas om allvarliga biverkningar förekommer. Säkerhet och effekt av erlotinib har inte studerats hos patienter med gravt nedsatt leverfunktion (ASAT/SGOT och ALAT/SGPT >5 x ULN. Användning av Tarceva hos patienter med gravt nedsatt leverfunktion rekommenderas inte (se avsnitt Farmakokinetik).
Nedsatt njurfunktion
Säkerhet och effekt av erlotinib har inte studerats hos patienter med nedsatt njurfunktion (serumkreatininkoncentration >1,5 gånger den övre normalgränsen). Baserat på farmakokinetiska data tycks inte dosjusteringar vara nödvändiga för patienter med mild eller måttligt nedsatt njurfunktion (se avsnitt Farmakokinetik). Användning av Tarceva hos patienter med gravt nedsatt njurfunktion rekommenderas inte.
Pediatrisk population
Säkerhet och effekt för erlotinib i de godkända indikationerna har inte fastställts för patienter under 18 år. Användning av Tarceva hos barn rekommenderas inte.
Rökare
Cigarettrökning har visats minska exponeringen av erlotinib med 50-60 %. Den maximala tolererade dosen av Tarceva var 300 mg hos patienter med icke-småcellig lungcancer som rökte cigaretter. 300 mg-dosen visade ingen förbättrad effekt i andra linjens behandling efter svikt på kemoterapi jämfört med den rekommenderade dosen på 150 mg hos patienter som fortsätter att röka cigaretter. Säkerhetsdata var jämförbara mellan doserna på 300 mg och 150 mg. Det förekom emellertid en numerisk ökning i incidensen av hudutslag, interstitiell lungsjukdom och diarré hos patienter som fick den högre dosen av erlotinib. Nuvarande rökare ska rådas att sluta röka (se avsnitt Varningar och försiktighet, Interaktioner, Farmakodynamik och Farmakokinetik).
Varningar och försiktighet
Bedömning av EGFR-mutationsstatus
När användning av Tarceva som första linjens behandling eller underhållsbehandling övervägs för lokalt avancerad eller metastaserad NSCLC är det viktigt att EGFR‑mutationsstatus hos patienten bestäms.
Ett validerat, robust, tillförlitligt och känsligt test med ett förspecificerat tröskelvärde för positivitet och som visats fungera för bestämning av EGFR-mutationsstatus, antingen med tumör-DNA från ett vävnadsprov eller cirkulerande fritt DNA (cfDNA) från blodprov (plasma), ska genomföras enligt lokal medicinsk praxis.
Om ett plasmabaserat cfDNA-test används och resultatet är negativt för aktiverande mutationer ska, där så är möjligt, ett vävnadstest tas på grund av risken för falskt negativa resultat från ett plasmabaserat test.
Rökare
Rökare bör rådas att sluta röka eftersom plasmakoncentrationer av erlotinib hos rökare är lägre jämfört med icke-rökare. Minskningen är troligen av klinisk betydelse (se avsnitt Dosering, Interaktioner, Farmakodynamik och Farmakokinetik).
Interstitiell lungsjukdom
Sällsynta fall liknande interstitiell lungsjukdom (ILS), inkluderande dödsfall, har rapporterats hos patienter som behandlats med Tarceva för icke‑småcellig lungcancer, pankreascancer eller andra avancerade solida tumörer. I den pivotala studien BR.21 var förekomsten av ILS (0,8 %) densamma för både placebo‑ och Tarcevagruppen hos patienter med icke‑småcellig lungcancer. I en metaanalys av randomiserade kontrollerade kliniska prövningar (exkluderande fas I och enarmade fas II studier på grund av avsaknad av kontrollgrupper) på icke-småcellig lungcancer var incidensen av ILS-liknande händelser 0,9 % med Tarceva jämfört med 0,4% hos patienter i kontrollarmarna. I pankreascancerstudien i kombination med gemcitabin, var förekomsten av biverkningar liknande ILS 2,5 % i gruppen som fick Tarceva plus gemcitabin jämfört med 0,4 % i behandlingsgruppen med placebo plus gemcitabin. De diagnoser som rapporterades hos patienter som misstänktes ha biverkningar liknande ILS omfattade pneumonit, strålningspneumonit, överkänslighetspneumonit, interstitiell pneumoni, interstitiell lungsjukdom, obliterativ bronkiolit, lungfibros, akut svår andningsinsufficiens (ARDS), alveolit och lunginfiltration. Symtom startade från ett par dagar till flera månader efter att Tarcevabehandling inletts. Det var vanligt med komplicerande eller bidragande faktorer såsom samtidig eller tidigare kemoterapi, tidigare strålning, etablerad parenkymal lungsjukdom, metastaserad lungsjukdom eller lunginfektioner. En högre förekomst av ILS (cirka 5 % med en dödlighet på 1,5 %) ses hos patienter i studier genomförda i Japan.
Hos patienter som plötsligt utvecklar nya och/eller progressiva och oförklarliga lungsymtom såsom andnöd, hosta och feber, ska behandling med Tarceva avbrytas under diagnostisk utredning. Patienter som samtidigt behandlas med erlotinib och gemcitabin ska noggrant kontrolleras avseende utveckling av biverkningar liknande ILS. Om ILS diagnosticeras, ska Tarceva sättas ut och lämplig behandling påbörjas (se avsnitt Biverkningar).
Diarré, dehydrering, elektrolytrubbningar och njursvikt
Diarré (inklusive mycket sällsynta fall med dödlig utgång) har uppträtt hos ca 50 % av patienter som behandlats med Tarceva, och måttlig eller svår diarré ska behandlas med t ex loperamid. I vissa fall kan en dosreduktion vara nödvändig. I de kliniska studierna minskades doserna stegvis med 50 mg i taget. Dosreduktioner med 25 mg i taget har inte studerats. Vid svår eller långvarig diarré, illamående, anorexi eller kräkningar förknippade med dehydrering ska behandling med Tarceva avbrytas och lämpliga åtgärder vidtas för att behandla dehydreringen (se avsnitt Biverkningar). Sällsynta fall av hypokalemi och njursvikt (inklusive dödsfall) har rapporterats. Vissa fall var sekundära effekter av svår dehydrering pga diarré, kräkningar och/eller anorexi, medan andra komplicerades av samtidig kemoterapibehandling. För svåra eller ihållande fall av diarré, eller för tillstånd som leder till dehydrering, framförallt hos grupper av patienter med försvårande riskfaktorer (särskilt samtidig kemoterapi eller andra behandlingar, symtom eller sjukdomar eller andra predisponerande omständigheter inklusive hög ålder), bör behandling med Tarceva tillfälligt avbrytas och erforderliga åtgärder vidtas för att intensivt rehydrera patienterna intravenöst. Dessutom bör njurfunktion och serumelektrolyter, inklusive kalium, kontrolleras hos patienter med risk för dehydrering.
Hepatotoxicitet
Allvarliga fall av läkemedelsinducerad leverskada (DILI) inklusive hepatit, akut hepatit och leversvikt (inklusive dödsfall) har rapporterats under behandling med Tarceva. Riskfaktorer kan inkludera leversjukdom i anamnesen eller samtidig behandling med levertoxiska läkemedel. Periodisk uppföljning av leverfunktionen rekommenderas under behandling med Tarceva. Frekvensen för kontroll av leverfunktionen bör ökas hos patienter som redan har nedsatt leverfunktion eller biliär obstruktion. Snabb klinisk utvärdering och kontroll av leverfunktionsprover bör göras hos patienter som rapporterar symtom som kan tyda på leverskada. Behandling med Tarceva ska avbrytas vid allvarliga förändringar av leverfunktionen (se avsnitt Biverkningar). Användning av Tarceva hos patienter med gravt nedsatt leverfunktion rekommenderas inte.
Gastrointestinal perforation
Patienter som behandlas med Tarceva har en ökad risk att utveckla gastrointestinal perforation, vilket observerades som mindre vanligt förekommande (inklusive vissa fall med dödlig utgång). Patienter som samtidigt behandlas med angiogeneshämmare, kortikosteroider, NSAIDs och/eller taxanbaserad kemoterapi eller som tidigare har haft peptiskt ulcus eller divertikulär sjukdom har en ökad risk. Tarceva-behandling ska avbrytas permanent hos patienter som utvecklar gastrointestinal perforation (se avsnitt Biverkningar).
Bullösa och exfoliativa hudsjukdomar
Bullösa, vesikulära och exfoliativa hudtillstånd har rapporterats, inkluderande mycket sällsynta fall liknande Stevens-Johnsons syndrom/toxisk epidermal nekrolys, som i vissa fall var fatala (se avsnitt Biverkningar). Tarceva-behandling ska avbrytas tillfälligt eller avslutas om patienter utvecklar allvarliga bullösa, vesikulära eller exfoliativa tillstånd. Patienter med bullösa och exfoliativa hudsjukdomar bör testas för hudinfektion och behandlas enligt lokala behandlingsriktlinjer.
Ögonsjukdomar
Patienter som uppvisar tecken och symptom på keratit så som akut eller försämrad; ögoninflammation, tårflöde, ljuskänslighet, dimsyn, ögonsmärta och/eller rött öga ska remitteras omgående till en oftalmologispecialist. Om diagnosen ulcerös keratit bekräftas, ska behandling med Tarceva avbrytas eller avslutas. Om keratit diagnosticeras ska fördelar och risker med fortsatt behandling noga övervägas. Tarceva ska användas med försiktighet hos patienter med tidigare keratit, ulcerativ keratit eller svårt torra ögon. Kontaktlinsanvändning är också en riskfaktor för keratit och ulceration. Mycket sällsynta fall av sår på, eller perforation av hornhinnan har rapporterats vid användning av Tarceva (se avsnitt Biverkningar).
Interaktioner med andra läkemedel
Potenta inducerare av CYP3A4 kan minska effekten av erlotinib medan potenta hämmare av CYP3A4 kan leda till ökad toxicitet. Samtidig behandling med dessa typer av läkemedel ska undvikas (se avsnitt Interaktioner).
Andra former av interaktioner
Erlotinib karakteriseras av en minskad löslighet vid pH över 5. Läkemedel som förändrar pH i övre delen av magtarmkanalen, såsom protonpumpshämmare, H2‑antagonister och antacida, kan ändra erlotinibs löslighet och därmed dess biotillgänglighet. Det är inte troligt att denna minskade exponering kan kompenseras genom att öka dosen av Tarceva vid samtidig administrering med sådana läkemedel. Kombination av erlotinib med protonpumpshämmare ska undvikas. Effekterna av samtidig administrering av erlotinib med H2-antagonister och antacida är okända; dock är en minskad biotillgänglighet trolig. Samtidig administrering av sådana kombinationer ska därför undvikas (se avsnitt Interaktioner). Om användning av antacida bedöms vara nödvändig under behandling med Tarceva ska dessa intas minst 4 timmar före eller 2 timmar efter den dagliga dosen av Tarceva.
Hjälpämnen med känd effekt
Tabletterna innehåller laktos. Patienter med sällsynta ärftliga problem med galaktosintolerans, total laktasbrist eller malabsorption av glukos‑galaktos, ska inte ta detta läkemedel.
Detta läkemedel innehåller mindre än 1 mmol (23 mg) natrium per tablett, d.v.s. är näst intill ”natriumfritt”.
Interaktioner
Interaktionsstudier har endast utförts på vuxna.
Erlotinib och andra CYP-substrat
Erlotinib är en potent hämmare av CYP1A1, och en måttlig hämmare av CYP3A4 och CYP2C8, samt en stark hämmare av glukuronidering med UGT1A1 in vitro.
Den fysiologiska betydelsen av den starka CYP1A1-hämningen är inte känd då CYP1A1 uttrycks i mycket begränsad omfattning i human vävnad.
När erlotinib gavs tillsammans med ciprofloxacin, en måttlig hämmare av CYP1A2, ökade erlotinibs exponering [AUC] signifikant med 39 %, medan det inte var någon statistiskt signifikant förändring av Cmax. På liknande sätt ökade exponeringen (AUC) för den aktiva metaboliten med 60 % och Cmax med 48 %. Den kliniska betydelsen av denna ökning har inte fastställts. Försiktighet bör iakttas när ciprofloxacin eller potenta CYP1A2 hämmare (t ex fluvoxamin) kombineras med erlotinib. Om biverkningar som förknippas med erlotinib observeras kan erlotinibdosen reduceras.
Tidigare behandling eller samtidig behandling med Tarceva förändrade inte clearance av de prototypa CYP3A4-substraten midazolam och erytromycin, men verkade minska den orala biotillgängligheten av midazolam med upp till 24 %. En annan klinisk studie visade att erlotinib inte påverkade farmakokinetiken av CYP3A4/2C8 substratet paklitaxel vid samtidig administrering. Betydelsefulla interaktioner med avseende på clearance av andra CYP3A4-substrat är därför inte troliga.
Hämning av glukuronidering kan orsaka interaktioner med läkemedel som är substrat till UGT1A1 och som enbart elimineras på detta sätt. Patienter med låga nivåer av UGT1A1 eller som har genetiska rubbningar av glukuronideringen (t ex Gilberts sjukdom) kan uppvisa ökade serumkoncentrationer av bilirubin och måste behandlas med försiktighet.
Hos människa metaboliseras erlotinib i levern av levercytokromer, framförallt av CYP3A4 och i mindre utsträckning av CYP1A2. Extrahepatisk metabolisering av CYP3A4 i tarm, CYP1A1 i lunga och CYP1B1 i tumörvävnad kan också potentiellt bidra till den metaboliska eliminationen av erlotinib. Interaktioner kan uppträda med aktiva substanser som metaboliseras av, eller som är hämmare eller inducerare av, dessa enzymer.
Potenta hämmare av CYP3A4-aktiviteten minskar metabolismen av erlotinib och ökar erlotinibs plasmakoncentrationer. I en klinisk studie resulterade samtidig administrering av erlotinib och ketokonazol (200 mg peroralt två gånger dagligen i 5 dagar), en potent CYP3A4-hämmare, i en ökning av erlotinibs exponering (86 % av AUC och 69 % av Cmax). Försiktighet ska därför iakttas när erlotinib kombineras med en potent CYP3A4-hämmare, t ex antimykotika av azoltyp (såsom ketokonazol, itrakonazol, vorikonazol), proteashämmare, erytromycin eller klaritromycin. Om nödvändigt bör erlotinibdosen reduceras, framförallt om besvärande biverkningar observeras.
Potenta inducerare av CYP3A4 aktiviteten ökar metabolismen av erlotinib och minskar signifikant erlotinibs plasmakoncentrationer. I en klinisk studie medförde samtidig administrering av erlotinib och rifampicin (600 mg peroralt fyra gånger dagligen i 7 dagar), en potent inducerare av CYP3A4, en minskning av medianvärdet för erlotinibs AUC med 69 %. Samtidig administrering av rifampicin med Tarceva i en singeldos om 450 mg resulterade i en medelexponering av erlotinib (AUC) på 57,5 % av den som fås efter en oral singeldos om 150 mg Tarceva utan rifampicin. Samtidig behandling av Tarceva med inducerare av CYP3A4 bör därför undvikas. För patienter som behöver samtidig behandling med Tarceva och en potent inducerare av CYP3A4, såsom rifampicin, bör en dosökning till 300 mg övervägas under noggrann säkerhetsövervakning (som inkluderar njur- och leverfunktion samt serumelektrolyter). Om denna dosering tolereras väl under mer än 2 veckor kan en ytterligare dosökning till 450 mg övervägas under noggrann säkerhetsövervakning. Minskad exponering kan också uppträda med andra inducerare t ex fenytoin, karbamazepin, barbiturater eller johannesört (hypericum perforatum). Försiktighet ska iakttas när dessa aktiva substanser kombineras med erlotinib. Om möjligt ska alternativa behandlingar som saknar potent CYP3A4 inducerande aktivitet övervägas.
Erlotinib och kumarinderiverade antikoagulantia
Interaktion med kumarinderiverade antikoagulantia, inklusive warfarin, som leder till ökad internationell normaliserad kvot (International Normalised Ratio, INR) och blödningshändelser, i vissa fall med dödlig utgång, har rapporterats hos patienter som får Tarceva. Patienter som behandlas med kumarinderiverade antikoagulantia ska regelbundet kontrolleras avseende några förändringar i protrombintid eller INR.
Erlotinib och statiner
Kombinationen av Tarceva och en statin kan öka risken för statin-inducerad myopati, inklusive rabdomyolys, vilket observerats i sällsynta fall.
Erlotinib och rökare
Resultat från en farmakokinetisk interaktionsstudie indikerade en signifikant 2,8-, 1,5‑ respektive 9-faldig minskning av AUCinf, Cmax respektive plasmakoncentration 24 timmar efter administrering av Tarceva till rökare jämfört med icke-rökare. Patienter som fortfarande röker ska därför uppmuntras att sluta röka så tidigt som möjligt innan behandling med Tarceva inleds eftersom plasmakoncentrationer av erlotinib annars blir lägre. Baserat på data från CURRENTS‑studien sågs inga bevis på någon fördel med en högre erlotinibdos på 300 mg när det jämfördes med den rekommenderade dosen på 150 mg hos aktiva rökare. Säkerhetsdata var jämförbara mellan doserna på 300 mg och 150 mg. Det förekom emellertid en numerisk ökning i incidensen av hudutslag, interstitiell lungsjukdom och diarré hos patienter som fick den högre dosen av erlotinib (se avsnitt Dosering, Varningar och försiktighet, Farmakodynamik och Farmakokinetik).
Erlotinib och P-glykoproteinhämmare
Erlotinib är ett substrat för P-glykoprotein, som är en transportör av aktiv substans. Samtidig administrering av hämmare av P-glykoprotein, t ex ciklosporin och verapamil, kan leda till förändrad distribution och/eller förändrad elimination av erlotinib. Effekterna av denna interaktion på t ex CNS-toxicitet har inte fastställts. Försiktighet bör iakttas i sådana situationer.
Erlotinib och läkemedel som förändrar pH
Erlotinib karakteriseras av en minskad löslighet vid pH över 5. Läkemedel som förändrar pH i den övre delen av magtarmkanalen kan därför ändra erlotinibs löslighet och därmed dess biotillgänglighet. Vid samtidig administrering av erlotinib med omeprazol, en protonpumpshämmare, minskade erlotinibs exponering [AUC] med 46 % och den maximala koncentrationen [Cmax] med 61 %. Tmax eller halveringstid förändrades inte. Samtidig administrering av Tarceva med 300 mg ranitidin, en H2-receptorantagonist, minskade erlotinibs exponering [AUC] med 33 % och den maximala koncentrationen [Cmax] med 54 %. Det är inte troligt att denna minskade exponering kan kompenseras genom att öka dosen av Tarceva vid samtidig administrering med sådana läkemedel. När Tarceva doserades separat 2 timmar före eller 10 timmar efter 150 mg ranitidin 2 gånger dagligen minskade däremot erlotinibs exponering [AUC] endast med 15 % och den maximala koncentrationen [Cmax] endast med 17 %. Effekten av antacida på erlotinibs absorption har inte studerats, men absorptionen kan försämras och därmed ge lägre plasmanivåer. Sammanfattningsvis ska kombination av erlotinib med protonpumpshämmare undvikas. Om användning av antacida bedöms vara nödvändig under behandling med Tarceva ska dessa intas minst 4 timmar före eller 2 timmar efter den dagliga dosen av Tarceva. Om användning av ranitidin övervägs ska det användas på ett separat sätt, dvs Tarceva måste tas minst 2 timmar innan eller 10 timmar efter ranitidin.
Erlotinib och gemcitabin
I en fas Ib-studie hade gemcitabin inga signifikanta effekter på erlotinibs farmakokinetik och erlotinib hade heller inga signifikanta effekter på gemcitabins farmakokinetik.
Erlotinib och karboplatin/paklitaxel
Erlotinib ökar koncentrationerna av platina. I en klinisk studie ledde samtidig användning av erlotinib med karboplatin och paklitaxel till en ökning av totalt AUC 0‑48 för platina med 10,6 %. Även om ökningen var statistiskt signifikant bedöms inte storleken av denna skillnad som kliniskt betydelsefull. I klinisk praxis kan det finnas andra medverkande faktorer, såsom nedsatt njurfunktion, som kan leda till ökad exponering av karboplatin. Karboplatin och paklitaxel hade inga signifikanta effekter på erlotinibs farmakokinetik.
Erlotinib och kapecitabin
Kapecitabin kan öka koncentrationerna av erlotinib. När erlotinib gavs i kombination med kapecitabin erhölls en statistiskt signifikant ökning av erlotinibs AUC och en marginell ökning av Cmax jämfört med värden som observerades i en annan studie där erlotinib gavs ensamt. Erlotinib hade inga signifikanta effekter på farmakokinetiken av kapecitabin.
Erlotinib och proteasomhämmare
På grund av verkningsmekanismen kan proteasomhämmare inklusive bortezomib förväntas påverka effekten av EGFR-hämmare inklusive erlotinib. En sådan påverkan stöds av begränsade kliniska data och prekliniska studier som visar nedbrytning av EGFR genom proteasomen.
Graviditet
Graviditet
Det finns inga adekvata data från användning av erlotinib i gravida kvinnor. Djurstudier har inte visat några tecken på teratogenicitet eller onormalt födande. Däremot kan negativa effekter avseende graviditet inte uteslutas då studier på råtta och kanin har visat en ökad embryonal/fetal dödlighet, (se avsnitt Prekliniska uppgifter). Den potentiella risken för människa är inte känd.
Fertila kvinnor
Fertila kvinnor måste rådas att undvika att bli gravida när de behandlas med Tarceva. Tillförlitliga preventivmetoder ska användas under behandling och under minst 2 veckor efter avslutad behandling. Behandling av gravida kvinnor ska endast fortsätta om den potentiella nyttan för modern överväger risken för fostret.
Amning
Det är inte känt om erlotinib utsöndras i bröstmjölk. Inga studier har genomförts för att bedöma Tarcevas inverkan på mjölkproduktionen eller om det utsöndras i bröstmjölk. Eftersom den potentiella risken för skada på det ammande barnet är okänd ska mödrar rådas att undvika amning under behandling med Tarceva och i minst 2 veckor efter den sista dosen.
Fertilitet
Djurstudier har inte visat några tecken på försämrad fertilitet. Däremot kan negativa effekter avseende fertilitet inte uteslutas då djurstudier har visat effekter på reproduktionsparametrar (se avsnitt Prekliniska uppgifter). Den potentiella risken för människa är inte känd.
Trafik
Inga studier har utförts. Erlotinib är dock inte förknippad med påverkan på den mentala förmågan.
Biverkningar
Sammanfattning av säkerhetsprofilen
Säkerhetsutvärderingen av Tarceva baseras på data från fler än 1500 patienter som behandlades med minst en 150 mg-dos av Tarceva i monoterapi samt fler än 300 patienter som fick Tarceva 100 mg eller 150 mg i kombination med gemcitabin.
Icke-småcellig lungcancer (Tarceva administrerad som monoterapi)
Första linjens behandling av patienter med EGFR-mutationer
I en öppen, randomiserad fas III studie, ML20650, genomförd på 154 patienter utvärderades säkerheten av Tarceva vid första linjens behandling av NSCLC‑patienter med EGFR-aktiverande mutationer hos 75 patienter.
De vanligaste biverkningarna som sågs hos patienter som behandlats med Tarceva i studie ML20650 var hudutslag och diarré, de flesta var grad 1-2 i allvarlighetsgrad och hanterbara utan medicinsk åtgärd. Fullständig information om gradering och incidens av hudutslag och diarré i alla kliniska studier finns i avsnittet ”Beskrivning av utvalda biverkningar” nedan.
Underhållsbehandling
I två andra dubbelblinda, randomiserade placebokontrollerade fas III-studier, BO18192 (SATURN) och BO25460 (IUNO), gavs Tarceva som underhållsbehandling efter första linjens kemoterapi. I dessa studier ingick totalt 1532 patienter med avancerad, recidiverande eller metastaserande NSCLC efter första linjens platinabaserad standard-kemoterapi.
De vanligaste biverkningarna som rapporterades hos patienter som behandlades med Tarceva i studierna BO18192 och BO25460 var hudutslag och diarré.
Andra och senare linjens behandling
I en randomiserad dubbelblind studie (BR.21; Tarceva gavs som andra linjens behandling), var hudutslag och diarré de vanligaste rapporterade biverkningarna. De flesta var av svårighetsgrad 1‑2 och hanterbara utan medicinsk åtgärd. Mediantiden till att hudutslag uppträdde var 8 dagar, och mediantiden till att diarré uppträdde var 12 dagar.
Pankreascancer (Tarceva administrerad tillsammans med gemcitabin)
De vanligaste rapporterade biverkningarna i den pivotala studien PA.3 med pankreascancerpatienter som fick Tarceva 100 mg plus gemcitabin var trötthet, hudutslag och diarré. Mediantiden till att hudutslag och diarré uppträdde var 10 dagar respektive 15 dagar.
Sammanfattning av biverkningar i tabellform
Incidensen av biverkningar som rapporterats från kliniska prövningar och efter godkännandet för försäljning, med Tarceva ensamt eller i kombination med kemoterapi sammanfattas i tabell 1. Biverkningar är listade enligt MedDRA organsystem. Motsvarade frekvenskategorier för varje biverkning är baserad på följande konvention: mycket vanliga (≥10), vanliga (≥1/100, <1/10), mindre vanliga (≥1/1000, <1/100), sällsynta (≥1/10 000, <1/1000), mycket sällsynta (<1/10 000), ingen känd frekvens (kan inte beräknas från tillgängliga data).
Inom varje frekvensgrupp anges biverkningarna med minskande allvarlighetsgrad.
Tabell 1: Sammanfattning av biverkningar från kliniska prövningar och efter godkännandet för försäljning per frekvenskategori:
|
Infektioner och infestationer |
|
|
Mycket vanliga |
infektion* |
|
Metabolism och nutrition |
|
|
Mycket vanliga |
anorexi, viktnedgång |
|
Psykiska störningar |
|
|
Mycket vanliga |
depression |
|
Centrala och perifera nervsystemet |
|
|
Mycket vanliga |
neuropati, huvudvärk |
|
Ögon |
|
|
Mycket vanliga |
keratokonjunktivit sicca |
|
Vanliga |
keratit, konjunktivit |
|
Mindre vanliga |
förändringar av ögonfransar* |
|
Mycket sällsynta |
perforation på hornhinnan, sår på hornhinnan, uveit |
|
Andningsvägar, bröstkorg och mediastinum |
|
|
Mycket vanliga |
dyspné, hosta |
|
Vanliga |
epistaxis |
|
Mindre vanliga |
interstitiell lungsjukdom* |
|
Magtarmkanalen |
|
|
Mycket vanliga |
diarré*, illamående, kräkning, stomatit, buksmärta, dyspepsi, flatulens |
|
Vanliga |
gastrointestinal blödning* |
|
Mindre vanliga |
gastrointestinala perforationer* |
|
Sällsynta |
pneumatosis intestinalis |
|
Lever och gallvägar |
|
|
Mycket vanliga |
onormalt leverfunktionstest* |
|
Sällsynta |
leversvikt*, hepatit |
|
Ingen känd frekvens (kan inte beräknas från tillgängliga data) |
akut hepatit |
|
Hud och subkutan vävnad |
|
|
Mycket vanliga |
hudutslag*, klåda |
|
Vanliga |
alopeci, torr hud, paronyki, follikulit, akne/akneiform dermatit, hudfissurer |
|
Mindre vanliga |
hirsutism, förändringar av ögonbryn, sköra och lösa naglar, milda hudreaktioner såsom hyperpigmentering |
|
Sällsynta |
hand-fot-syndromet (palmar-plantar erytrodysestesi) |
|
Mycket sällsynta |
Stevens-Johnson syndrom/toxisk epidermal nekrolys* |
|
Njurar och urinvägar |
|
|
Vanliga |
njurinsufficiens |
|
Mindre vanliga |
nefrit, proteinuri |
|
Allmänna symtom och/eller symtom vid administreringsstället |
|
|
Mycket vanliga |
trötthet, feber, frossbrytning |
*För ytterligare detaljer, se avsnitt ”Beskrivning av utvalda biverkningar” nedan.
Beskrivning av utvalda biverkningar
Hudutslag
Hudutslag inkluderar aknieform dermatit. I allmänhet uppträder hudutslagen som milda till måttliga erytematösa och papulopustulära utslag vilka kan uppkomma eller förvärras på solexponerade områden. Patienter som exponeras för sol bör rådas att använda skyddande kläder och/eller solskyddsmedel (t.ex. mineralinnehållande).
Diarré
Diarré kan leda till dehydrering, hypokalemi och njursvikt. Det inkluderar dödsfall (se avsnitt Varningar och försiktighet).
Tabell 2: Sammanfattning av incidens och grader av hudutslag och diarré som observerats i respektive kliniska studie
|
Studie |
Indikation |
Hudutslag (%) |
Diarré (%) |
||||||||
|
Grad |
Vidtagen åtgärd |
Grad |
Vidtagen åtgärd |
||||||||
|
Alla |
3 |
4 |
Avslut1 |
Mod2 |
Alla |
3 |
4 |
Avslut1 |
Mod2 |
||
|
ML20650 |
NSCLC |
80 |
9 |
0 |
1 |
11 |
57 |
4 |
0 |
1 |
7 |
|
BO18192 |
NSCLC |
49,2 |
6,0 |
0 |
1 |
8,3 |
20,3 |
1,8 |
0 |
<1 |
3 |
|
BO25460 |
NSCLC |
39,4 |
5,0 |
0 |
0 |
5,6 |
24,2 |
2,5 |
0 |
0 |
2,8 |
|
BR.21 |
NSCLC |
75 |
9 |
1 |
6 |
54 |
6 |
1 |
1 |
||
|
PA.3 |
Pankreas-cancer |
- |
5 |
1 |
2 |
- |
5 |
1 |
2 |
||
1 Avslutad behandling
2 Modifierad dos
Infektion
Detta kan vara svåra infektioner med eller utan neutropeni, inkluderande pneumoni, sepsis och cellulit.
Förändringar av ögonfransar
Förändringar inkluderar inåtväxande ögonfransar, ökad tillväxt och förtjockning av ögonfransarna.
Interstitiell lungsjukdom (ILS)
ILS inkluderar dödsfall hos patienter som får Tarceva för behandling av icke-småcellig lungcancer eller andra avancerade solida tumörer (se avsnitt Varningar och försiktighet). En högre incidens har observerats hos patienter i Japan (se avsnitt Varningar och försiktighet).
Gastrointestinal (GI) blödning
GI blödning inkluderar dödsfall (se avsnitt Varningar och försiktighet). I kliniska studier har vissa fall förknippats med samtidig användning av warfarin och i vissa fall med samtidig användning av NSAID (se avsnitt Interaktioner). Gastrointestinala perforationer inkluderar även dödsfall (se avsnitt Varningar och försiktighet).
Onormalt leverfunktionstest
Onormalt leverfunktionstest inkluderar förhöjda nivåer av alaninaminotransferas (ALAT), aspartasaminotansferas (ASAT) och bilirubin. Fallen var övervägande milda till måttliga i svårighetsgrad, övergående till sin natur eller förknippade med levermetastaser.
Leversvikt
Inkluderar dödsfall. Riskfaktorer kan inkludera leversjukdom i anamnesen eller samtidig behandling med levertoxiska läkemedel (se avsnitt Varningar och försiktighet).
Stevens-Johnson syndrom/toxisk epidermal nekrolys
Inkluderar dödsfall (se avsnitt Varningar och försiktighet).
Rapportering av misstänkta biverkningar
Det är viktigt att rapportera misstänkta biverkningar efter att läkemedlet godkänts. Det gör det möjligt att kontinuerligt övervaka läkemedlets nytta-riskförhållande. Hälso- och sjukvårdspersonal uppmanas att rapportera varje misstänkt biverkning till Läkemedelsverket, men alla kan rapportera misstänkta biverkningar till Läkemedelsverket, www.lakemedelsverket.se. Postadress
Läkemedelsverket
Box 26
751 03 Uppsala
Överdosering
Symtom
Enstaka orala doser av Tarceva upp till 1000 mg erlotinib hos friska försökspersoner, och upp till 1600 mg hos cancerpatienter, har tolererats. Upprepad dosering två gånger dagligen med 200 mg hos friska försökspersoner tolererades dåligt efter bara några få dagars dosering. Baserat på data från dessa studier, kan allvarliga biverkningar såsom diarré, hudutslag och möjligen ökad aktivitet av levertransaminaser uppträda vid doser över den rekommenderade dosen.
Behandling
Vid misstänkt överdosering ska behandling med Tarceva avbrytas och symtomatisk behandling påbörjas.
Farmakodynamik
Verkningsmekanism
Erlotinib är en epidermal tillväxtfaktorreceptor/human epidermal tillväxtfaktorreceptor typ 1 (EGFR är även känt som HER1) tyrosinkinashämmare. Erlotinib är en potent hämmare av den intracellulära fosforyleringen av EGFR. EGFR uttrycks på cellytan av normala celler och cancerceller. I prekliniska modeller resulterar hämning av EGFR fosfotyrosin i cellstas och/eller celldöd.
EGFR-mutationer kan leda till att signalsystemvägar för anti-apoptotos och proliferation aktiveras konstitutivt. Erlotinibs kraftfulla effekt som blockerare av EGFR-medierad signalering hos dessa EGFR-mutationspositiva tumörer beror på den starka bindningen av erlotinib till ATP-bindningsstället på den muterade kinasdomänen av EGFR. På grund av att nedströmssignaleringen blockeras, stoppas proliferation i cellerna och celldöd induceras genom cellens inneboende apoptosväg. Tumörregression har observerats i musmodeller vid förstärkt uttryck av dessa EGFR‑aktiverande mutationer.
Klinisk effekt
Första linjens behandling av icke-småcellig lungcancer (NSCLC) för patienter med EGFR-aktiverande mutationer (Tarceva administrerat som monoterapi)
Effekten av Tarceva vid första linjens behandling av patienter med EGFR‑aktiverande mutationer vid icke-småcellig lungcancer visades i en randomiserad öppen fas III studie (ML20650, EURTAC). Denna studie genomfördes på kaukasiska patienter med metastaserande eller lokalt avancerad icke-småcellig lungcancer (stadium IIIB och IV) som inte tidigare fått kemoterapi eller någon annan systemisk antitumörbehandling för sin avancerade sjukdom och som visade mutationer i tyrosinkinas-domänen av EGFR (exon 19 deletion eller exon 21 mutation). Patienterna randomiserades 1:1 att få Tarceva 150 mg eller platinabaserad kombinationskemoterapi.
Den primära effektvariabeln var prövarbedömd PFS. Effektresultaten sammanfattas i tabell 3.
Figur 1: Kaplan-Meier kurva för prövarbedömd PFS i studie ML20650 (EURTAC) (sista datum för datainsamling april 2012)
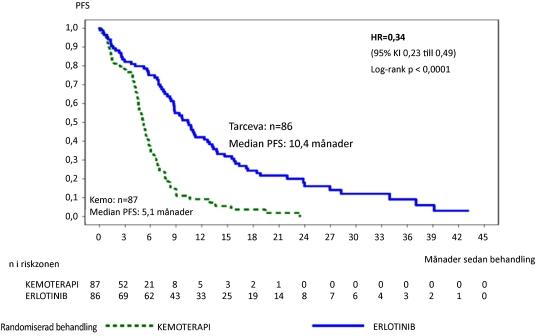
Tabell 3: Effektresultat för Tarceva jämfört med kemoterapi i studie ML20650 (EURTAC)
|
Tarceva |
Kemoterapi |
Hazard Ratio (95% KI) |
p-värde |
||
|---|---|---|---|---|---|
|
Förhandsplanerad interimsanalys (35% mognad av överlevnadsdata) (n = 153) Sista datum för datainsamling: aug 2010 |
n=77 |
n=76 | |||
|
Primär effektvariabel: Progressionsfri överlevnad (PFS, median i månader)* | |||||
|
Prövarbedömd** |
9,4 |
5,2 |
0,42 [0,27-0,64] |
p<0,0001 |
|
|
Oberoende bedömning** |
10,4 |
5,4 |
0,47 [0,27-0,78] |
p=0,003 |
|
|
Bästa responsfrekvens (CR/PR) |
54,5% |
10,5% |
p<0,0001 |
||
|
Överlevnad (månader) |
22,9 |
18,8 |
0,80 [0,47-1,37] |
p=0,4170 |
|
|
Explorativ analys (40% mognad av överlevnadsdata) (n=173) Sista datum för datainsamling: jan 2011 |
n=86 |
n=87 | |||
|
PFS (median i månader) Prövarbedömd |
9,7 |
5,2 |
0,37 [0,27-0,54] |
p<0,0001 |
|
|
Bästa responsfrekvens (CR/PR) |
58,1% |
14,9% |
p<0,0001 |
||
|
Överlevnad (månader) |
19,3 |
19,5 |
1,04 [0,65-1,68] |
p=0,8702 |
|
|
Uppdaterad analys (62% mognad av överlevnadsdata) (n=173) Sista datum för datainsamling: april 2012 |
n=86 |
n=87 | |||
|
PFS (median i månader) |
10,4 |
5,1 |
0,34 [0,23-0,49] |
p<0,0001 |
|
|
Överlevnad*** (månader) |
22,9 |
20,8 |
0,93 [0,64-1,36] |
p=0,7149 |
CR=komplett respons; PR=partiell respons
*En 58% riskreduktion av sjukdomsprogression eller död observerades
**Övergripande konkordans mellan bedömning av prövare och oberoende kommitté var 70%
***En hög andel crossover observerades med 82% av patienterna i kemoterapigruppen som fick efterföljande behandling med en EGFR tyrosinkinashämmare och alla förutom 2 av dessa patienter fick efterföljande Tarceva.
Underhållsbehandling av NSCLC efter första linjens kemoterapi (Tarceva administrerat som monoterapi)
Effekt och säkerhet för Tarceva som underhållsbehandling efter första linjens kemoterapi vid NSCLC undersöktes i en randomiserad, dubbelblind, placebokontrollerad studie (BO18192, SATURN). Denna studie utfördes med 889 patienter med lokalt avancerad eller metastaserande NSCLC som inte progredierat efter 4 cykler med platinabaserad kombinationskemoterapi. Patienterna randomiserades 1:1 för att få Tarceva 150 mg eller placebo peroralt en gång dagligen till sjukdomsprogression. Den primära effektvariabeln inkluderade progressionsfri överlevnad hos alla patienter. Demografiska data och sjukdomskaraktäristik före behandlingsstart var välbalanserat mellan de två behandlingsgrupperna. Patienter med ECOG PS>1, signifikanta co-morbiditeter i lever eller njure inkluderades inte i studien.
I denna studie visade den totala populationen en fördel för den primära effektvariabeln PFS (HR=0,71 p<0,0001) och den sekundära effektvariabeln OS (HR=0,81 p=0,0088). Den största fördelen observerades emellertid i en fördefinierad explorativ analys hos patienter med EGFR-aktiverande mutationer (n=49) som visade en betydande fördel för PFS (HR=0,10, 95% KI, 0,04 till 0,25; p<0,0001) och en HR för överlevnad på 0,83 (95% KI, 0,34 till 2,02). 67% av patienterna som fick placebo i den EGFR-mutationspositiva subgruppen erhöll en EGFR-TKI i andra eller senare linjens behandling.
Studien BO25460 (IUNO) utfördes på 643 patienter med avancerad NSCLC vars tumörer inte hade en EGFR-aktiverande mutation (exon 19 deletion eller exon 21 L858R mutation) och som inte fått sjukdomsprogression efter fyra cykler med platinabaserad kemoterapi.
Syftet med studien var att jämföra överlevnad vid första linjens underhållsbehandling med erlotinib jämfört med erlotinib administrerat vid tiden för sjukdomsprogression. Studien uppfyllde inte den primära effektvariabeln. Överlevnad med Tarceva i första linjens underhållsbehandling var inte bättre än Tarceva som andra linjes behandling hos patienter vars tumör inte hade en EGFR-aktiverande mutation (HR=1,02, 95% KI, 0,85 till 1,22, p=0,82). Den sekundära effektvariabeln PFS visade ingen skillnad mellan Tarceva och placebo vid underhållsbehandling (HR=0,94, 95% KI, 0,80 till 1,11; p=0,48).
Baserat på data från studien BO25460 (IUNO) rekommenderas inte Tarceva som första linjens underhållsbehandling hos patienter utan en EGFR-aktiverande mutation.
Behandling av NSCLC efter svikt på minst en tidigare kemoterapiregim (Tarceva administrerat som monoterapi)
Effekten och säkerheten av Tarceva som andra/tredje linjens behandling visades i en randomiserad, dubbelblind, placebokontrollerad studie (BR.21) med 731 patienter med lokalt avancerad eller metastaserad icke-småcellig lungcancer som sviktat på minst en kemoterapibehandling. Patienterna randomiserades 2:1 till behandling med Tarceva 150 mg eller placebo oralt en gång dagligen. Studiens effektmått inkluderade överlevnad, progressionsfri överlevnad (PFS), responsfrekvens, responsduration, tid till försämring av lungcancerrelaterade symtom (hosta, dyspné och smärta) och säkerhet. Det primära effektmåttet var överlevnad.
Demografiska karakteristika var väl balanserade mellan de två behandlingsgrupperna. Ungefär två tredjedelar av patienterna var män och ca en tredjedel hade ett värde på ECOG performance status (PS) på 2 vid inklusion i studien och 9 % hade ett ECOG PS på 3 vid inklusion. Nittiotre procent och 92 % av alla patienter i Tarceva- respektive placebogruppen hade tidigare erhållit platinainnehållande behandling och 36 % respektive 37 % av patienterna hade tidigare erhållit taxanbehandling.
Det justerade hazard ratio (HR) för död i Tarcevagruppen jämfört med placebogruppen var 0,73 (95 % konfidensintervall [KI], 0,60 till 0,87) (p = 0,001). Andelen patienter som levde vid 12 månader var 31,2 % för Tarcevagruppen respektive 21,5 % för placebogruppen. Medianöverlevnaden var 6,7 månader i Tarcevagruppen (95 % KI, 5,5 till 7,8 månader) jämfört med 4,7 månader i placebogruppen (95 % KI, 4,1 till 6,3 månader).
Effekten på överlevnad undersöktes för olika patientundergrupper. Tarcevas effekt på överlevnad var jämförbar hos patienter med ett performance status (ECOG) vid studiestart på 2-3 (HR = 0,77, 95% KI 0,6-1,0) eller 0-1 (HR = 0,73, 95 % KI 0,6-0,9), hos manliga patienter (HR = 0,76, 95 % KI 0,6-0,9) eller kvinnliga patienter (HR = 0,80, 95 % KI 0,6-1,1), hos patienter yngre än 65 år (HR = 0,75, 95 % KI 0,6‑0,9) eller äldre patienter (HR = 0,79, 95 % KI 0,6‑1,0), hos patienter med en tidigare behandling (HR = 0,76, 95 % KI 0,6‑1,0) eller fler än en tidigare behandling (HR = 0,75, 95 % KI 0,6‑1,0), hos kaukasiska patienter (HR = 0,79, 95 % KI 0,6‑1,0) eller asiatiska patienter (HR = 0,61, 95 % KI 0,4‑1,0), hos patienter med adenokarcinom (HR = 0,71, 95 % KI 0,6‑0,9) eller skivepitelcancer (HR = 0,67, 95 % KI 0,5‑0,9), men inte hos patienter med andra histologier (HR = 1,04, 95 % KI 0,7‑1,5), patienter med sjukdom av stadium IV vid diagnos (HR = 0,92, 95 % KI 0,7‑1,2) eller sjukdom lägre än stadium IV vid diagnos (HR = 0,65, 95 % KI 0,5‑0,8). Patienter som aldrig hade rökt hade en avsevärt större fördel av erlotinib (HR för överlevnad = 0,42, 95 % KI 0,28‑0,64) jämfört med nuvarande eller tidigare rökare (HR = 0,87, 95 % KI 0,71‑1,05).
Hos de 45 % av patienterna vars EGFR‑uttryck var känt var hazard ratio 0,68 (95 % KI 0,49‑0,94) för patienter med EGFR-positiva tumörer och 0,93 (95 % KI 0,63‑1,36) för patienter med EGFR-negativa tumörer (bestämt med en standardiserad immunhistokemisk metod [EGFR pharmDx] som definierade EGFR‑negativitet som färgning av mindre än 10 % av tumörcellerna). Hos de återstående 55 % av patienterna med okänt EGFR‑uttryck var hazard ratio 0,77 (95 % KI 0,61‑0,98).
Medianvärdet för PFS var 9,7 veckor i Tarcevagruppen (95 % KI, 8,4 till 12,4 veckor) jämfört med 8,0 veckor i placebogruppen (95 % KI, 7,9 till 8,1 veckor).
Objektiv responsfrekvens med RECIST var 8,9 % (95 % KI, 6,4 till 12,0) i Tarcevagruppen. De första 330 patienterna utvärderades centralt (responsfrekvens 6,2 %); 401 patienter utvärderades av prövaren (responsfrekvens 11,2 %).
Medianvärdet för responsduration var 34,3 veckor, och varierade mellan 9,7 till 57,6+ veckor. Andelen patienter som upplevde komplett respons, partiell respons eller stabil sjukdom var 44,0 % för Tarcevagruppen respektive 25,7 % för placebogruppen (p = 0,004).
En överlevnadsfördel av Tarceva observerades också hos patienter som inte fick något objektivt tumörsvar (med RECIST). Detta verifierades med ett hazard ratio för död på 0,82 (95 % KI, 0,68 till 0,99) för de patienter vars bästa respons var stabil sjukdom eller progredierande sjukdom.
Tarceva medförde symtomförbättringar genom att signifikant förlänga tid till försämring av hosta, dyspné och smärta jämfört med placebo.
I en dubbelblind, randomiserad fas III studie (MO22162, CURRENTS) som jämförde två doser av Tarceva (300 mg jämfört med 150 mg) hos rökare (i medel 38 förpackningar per år) med lokalt avancerad eller metastaserande NSCLC i andra linjen efter svikt på kemoterapi, visade 300 mg-dosen av Tarceva ingen fördel gällande progressionsfri överlevnad jämfört med den rekommenderade dosen (7,00 veckor jämfört med 6,86 veckor).
Alla sekundära effektmått överensstämde med det primära effektmåttet och ingen skillnad i överlevnad upptäcktes mellan patienter som behandlats med erlotinib 300 mg och 150 mg dagligen (HR 1,03, 95% KI 0,80 till 1.32). Säkerhetsdata var jämförbara mellan doserna på 300 mg och 150 mg. Det förekom emellertid en numerisk ökning i incidensen av hudutslag, interstitiell lungsjukdom och diarré hos patienter som fick den högre dosen av erlotinib. Baserat på data från CURRENTS‑studien sågs inga bevis på någon fördel med en högre erlotinibdos än 300 mg när det jämfördes med den rekommenderade dosen på 150 mg hos aktiva rökare.
Patienterna i denna studie valdes inte baserat på EGFR-mutationsstatus. Se avsnitt Dosering, Varningar och försiktighet, Interaktioner och Farmakokinetik.
Pankreascancer (Tarceva administrerad tillsammans med gemcitabin i studie PA.3)
Effekt och säkerhet av Tarceva i kombination med gemcitabin som första linjens behandling utvärderades i en randomiserad, dubbelblind, placebokontrollerad studie hos patienter med lokalt avancerad, icke-resecerbar eller metastaserad pankreascancer. Patienter randomiserades till Tarceva eller placebo en gång dagligen enligt ett kontinuerligt schema plus gemcitabin intravenöst (1000 mg/m2, behandlingscykel 1 – dag 1, 8, 15, 22, 29, 36 och 43 i en 8-veckorscykel; behandlingscykel 2 och efterföljande cykler – dag 1, 8 och 15 i en 4-veckorscykel [godkänd dosering och doseringsschema vid pankreascancer, se gemcitabins produktresumé]). Tarceva eller placebo intogs oralt en gång dagligen till sjukdomsprogress eller oacceptabel toxicitet. Primärt effektmått var överlevnad.
Demografi och sjukdomskarakteristika för patienterna var vid studiestart likvärdiga mellan de två behandlingsgrupperna, 100 mg Tarceva plus gemcitabin eller placebo plus gemcitabin, förutom en något större andel kvinnor i gruppen erlotinib/gemcitabin jämfört med placebo/gemcitabin:
|
Vid studiestart |
Tarceva |
Placebo |
|---|---|---|
|
Kvinnor |
51 % |
44 % |
|
ECOG performance status (PS) = 0 vid studiestart |
31 % |
32 % |
|
ECOG performance status (PS) = 1 vid studiestart |
51 % |
51 % |
|
ECOG performance status (PS) = 2 vid studiestart |
17 % |
17 % |
|
Metastaserad sjukdom vid studiestart |
77 % |
76 % |
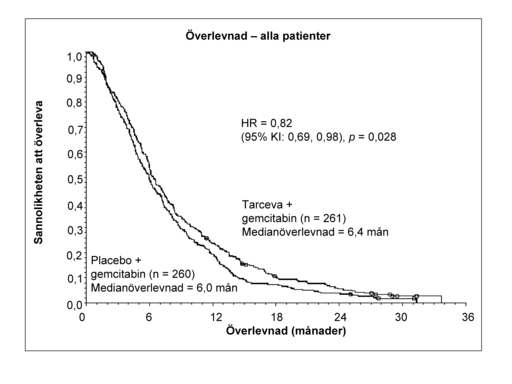
Överlevnad utvärderades i ”intent-to-treat”-populationen baserad på uppföljande överlevnadsdata. Resultaten presenteras i tabellen nedan (resultaten för patientgrupperna med metastaserad och lokalt avancerad sjukdom är erhållna från en explorativ subgruppsanalys).
|
Utfall |
Tarceva (mån) |
Placebo (mån) |
Δ (mån) |
KI av Δ |
HR |
KI av HR |
P- värde |
|---|---|---|---|---|---|---|---|
|
Totala patientpopulationen |
|||||||
|
Median-överlevnad |
6,4 |
6,0 |
0,41 |
-0,54-1,64 |
0,82 |
0,69-0,98 |
0,028 |
|
Medel-överlevnad |
8,8 |
7,6 |
1,16 |
-0,05-2,34 |
|||
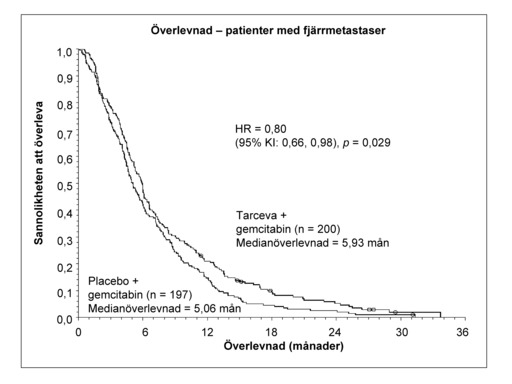
|
Patientpopulation med metastaserad sjukdom |
|||||||
|
Median-överlevnad |
5,9 |
5,1 |
0,87 |
-0,26-1,56 |
0,80 |
0,66-0,98 |
0,029 |
|
Medel-överlevnad |
8,1 |
6,7 |
1,43 |
0,17-2,66 |
|||
|
Patientpopulation med lokalt avancerad sjukdom |
|||||||
|
Median-överlevnad |
8,5 |
8,2 |
0,36 |
-2,43-2,96 |
0,93 |
0,65-1,35 |
0,713 |
|
Medel-överlevnad |
10,7 |
10,5 |
0,19 |
-2,43-2,69 |
|||
I en ”post-hoc”-analys kan patienter med god klinisk status vid studiestart (låg smärtintensitet, god livskvalitet (QoL) och bra PS) erhålla större fördel av Tarceva. Fördelen påverkas framförallt av låga smärtintensitetspoäng.
I en ”post-hoc”-analys hade patienter som utvecklade hudutslag en längre överlevnad jämfört med patienter som inte utvecklade hudutslag (medelöverlevnad 7,2 månader jämfört med 5 månader, HR:0,61). 90% av patienterna som behandlades med Tarceva utvecklade hudutslag inom de första 44 dagarna. Mediantid för utveckling av hudutslag var 10 dagar.
Pediatrisk population
Europeiska läkemedelsmyndigheten har tagit bort kravet att skicka in studieresultat med Tarceva för alla undergrupper av den pediatriska populationen inom icke småcelling lungcancer och pankreascancer, (se avsnitt Dosering för information om pediatrisk användning).
Farmakokinetik
Absorption
Vid oral administrering uppnås maximala plasmakoncentrationer av erlotinib efter ca 4 timmar. En studie på normala friska frivilliga försökspersoner gav en uppskattning av den absoluta biotillgängligheten till 59 %. Exponeringen efter en oral dos kan ökas av föda.
Distribution
Medelvärdet för den skenbara distributionsvolymen av erlotinib är 232 l och hos människa distribueras erlotinib in i tumörvävnad. I en studie på 4 patienter (3 med icke-småcellig lungcancer och 1 med larynxcancer) som fick dagliga orala doser av 150 mg Tarceva, visade tumörprover från kirurgiska snitt tagna på dag 9 av behandlingen att erlotinibkoncentrationerna i tumör i genomsnitt var 1,185 ng/g av vävnaden. Detta motsvarar ett totalt genomsnitt på 63 % (intervall 5-161 %) av observerade maximala plasmakoncentrationer vid steady-state. De primära aktiva metaboliterna fanns i tumör med genomsnittliga koncentrationer av 160 ng/g vävnad, vilket motsvarade ett totalt genomsnitt på 113 % (intervall 88-130 %) av de observerade maximala plasmakoncentrationerna vid steady-state. Plasmaproteinbindningen är ca 95 %. Erlotinib binds till serumalbumin och alfa‑1‑syra glykoprotein (AAG).
Metabolism
Hos människa metaboliseras erlotinib i levern av levercytokromer, framförallt av CYP3A4 och i mindre utsträckning av CYP1A2. Extrahepatisk metabolism av CYP3A4 i tarm, CYP1A1 i lunga och 1B1 i tumörvävnad bidrar potentiellt till den metaboliska eliminationen av erlotinib.
Det finns tre huvudsakliga metaboliseringsvägar identifierade: 1) O-demetylering av någon av sidokedjorna eller båda, följt av oxidering till karboxylsyror; 2) oxidering av acetylendelen följt av hydrolys till arylkarboxylsyra; och 3) aromatisk hydroxylering av fenyl-acetylendelen. De primära metaboliterna OSI-420 och OSI-413 av erlotinib, vilka produceras genom O-demetylering av någon av sidokedjorna, har jämförbar aktivitet med erlotinib i prekliniska in vitro analyser och in vivo tumörmodeller. I plasma är deras nivåer <10 % av erlotinibs och uppvisar en likvärdig farmakokinetik som erlotinib.
Eliminering
Erlotinib elimineras huvudsakligen som metaboliter via faeces (>90 %) och elimination via njuren svarar endast för en liten mängd (ca 9 %) av en oral dos. Mindre än 2 % av den oralt givna dosen utsöndras som modersubstans. En populationsfarmakokinetisk analys på 591 patienter som enbart fick Tarceva visar ett medelvärde på skenbart clearance på 4,47 l/timme med ett medianvärde för halveringstiden på 36,2 timmar. Tiden för att uppnå plasmakoncentrationer vid steady-state förväntas därför vara ca 7-8 dagar.
Farmakokinetik för särskilda patientgrupper
Baserat på populationsfarmakokinetisk analys observerades inget kliniskt signifikant samband mellan skenbart clearance och patientens ålder, kroppsvikt, kön eller etnicitet. Patientfaktorer som korrelerade med erlotinibs farmakokinetik var totalt serumbilirubin, AAG och rökning. Förhöjda serumkoncentrationer av totalt bilirubin och AAG förknippades med ett reducerat clearance av erlotinib. Den kliniska relevansen av dessa skillnader är oklar. Rökare hade dock ett förhöjt clearance av erlotinib. Detta bekräftades i en farmakokinetisk studie där friska försökspersoner som var icke-rökare respektive cigarettrökare fick en oral singeldos av 150 mg erlotinib. Det geometriska medelvärdet för Cmax var 1056 ng/ml hos icke‑rökarna och 689 ng/ml hos rökarna och kvoten mellan icke-rökare och rökare var i medeltal 65,2 % (95 % KI: 44,3 till 95,9, p=0,031). Det geometriska medelvärdet för AUC0‑inf var 18726 ng•h/ml för icke-rökarna och 6718 ng•h/ml för rökarna och kvoten var i medeltal 35,9 % (95 % KI: 23,7 till 54,3, p<0,0001). Det geometriska medelvärdet för C24tim var 288 ng/ml för icke-rökarna och 34,8 ng/ml för rökarna och kvoten var i medeltal 12,1 % (95 % KI: 4,82 till 30,2, p=0,0001).
I den pivotala fas III-studien på icke-småcellig lungcancer uppnådde nuvarande rökare ett dalvärde i plasmakoncentration vid steady state på 0,65 µg/ml (n=16) vilket var ungefär hälften så mycket som hos tidigare rökare eller patienter som aldrig rökt (1,28 µg/ml, n=108). Denna effekt åtföljdes av en 24 %-ig ökning av skenbar plasmaclearance för erlotinib. I en dos-eskaleringsstudie i fas I hos nuvarande rökande patienter med icke-småcellig lungcancer, visade farmakokinetiska analyser en ökning av erlotinibexponeringen vid steady state som var proportionell mot given dos av Tarceva från 150 mg till den maximalt tolererade dosen 300 mg. Dalvärdet i plasmakoncentration vid steady state var 1,22 µg/ml (n=17) vid dosen 300 mg hos nuvarande rökare i denna studie. Se avsnitt Dosering, Varningar och försiktighet, Interaktioner och Farmakodynamik.
Baserat på resultaten från farmakokinetiska studier bör rökare rådas att sluta röka under behandling med Tarceva eftersom plasmakoncentrationerna annars kan reduceras.
Baserat på populationsfarmakokinetisk analys föreföll närvaro av opoider medföra en ökning av exponeringen med ca 11 %.
En andra populationsfarmakokinetisk analys utfördes och omfattade erlotinibdata från 204 patienter med pankreascancer som erhöll erlotinib plus gemcitabin. Denna analys visade att de kovariater som påverkade erlotinibs clearance hos patienter från pankreascancerstudien var mycket lika de som sågs i den tidigare farmakokinetiska analysen där erlotinib gavs som monoterapi. Inga nya kovariateffekter identifierades. Samtidig behandling med gemcitabin hade ingen effekt på erlotinibs plasmaclearance.
Pediatrisk population
Det finns inga särskilda studier på pediatriska patienter.
Äldre population
Det finns inga särskilda studier på äldre patienter.
Nedsatt leverfunktion
Erlotinib elimineras till största delen via levern. Hos patienter med solida tumörer och med måttligt nedsatt leverfunktion (Child-Pugh score 7-9) var det geometriska medelvärdet för erlotinib AUC0-t och Cmax 27000 ng•h/ml respektive 805 ng/ml jämfört med 29300 ng•h/ml respektive 1090 ng/ml hos patienter med adekvat leverfunktion inklusive patienter med primär levercancer eller levermetastaser. Även om Cmax var statistiskt signifikant lägre hos patienter med måttligt nedsatt leverfunktion anses denna skillnad inte kliniskt relevant. Det finns inga tillgängliga data på hur gravt nedsatt leverfunktion påverkar erlotinibs farmakokinetik. I populationsfarmakokinetisk analys förknippades förhöjda nivåer av totalt bilirubin med ett långsammare clearance av erlotinib.
Nedsatt njurfunktion
Erlotinib och dess metaboliter utsöndras inte till någon större del via njuren, eftersom mindre än 9 % av en singeldos utsöndras i urinen. I populationsfarmakokinetisk analys observerades inget kliniskt signifikant samband mellan clearance av erlotinib och kreatininclearance, men det finns inga data tillgängliga för patienter med kreatininclearance <15 ml/min.
Prekliniska uppgifter
De effekter av upprepad dosering som observerades i minst ett djurslag eller studie inkluderade effekter på hornhinnan (atrofi, ulceration), hud (follikulär degeneration och inflammation, rodnad och alopeci), äggstockar (atrofi), lever (levernekros), njure (renal papillär nekros och tubulär utvidgning) och magtarmkanalen (fördröjd magtömning och diarré). Antalet röda blodkroppar var sänkt och antalet vita blodkroppar, framförallt neutrofiler, var förhöjt. Behandlingsrelaterade stegringar av ALAT, ASAT och bilirubin sågs. Dessa fynd observerades vid exponeringar som väl understeg kliniskt relevanta exponeringar.
Baserat på verkningsmekanismen kan erlotinib vara teratogent. Data från reproduktionstoxikologiska tester på råtta och kanin vid doser nära den maximalt tolerabla dosen och/eller maternellt toxiska doser visade reproduktionstoxikologiska effekter (embryotoxicitet på råtta, embryoresorption och fostertoxicitet på kanin) och utvecklingstoxikologiska effekter (minskning av tillväxt och överlevnad hos råtta), men var inte teratogent och påverkade inte fertiliteten. Dessa fynd observerades vid kliniskt relevanta exponeringar.
Erlotinib uppvisade negativa resultat i konventionella genotoxicitetsstudier. Karcinogenicitetsstudier med erlotinib under två år med råtta och mus var negativa upp till exponeringar överstigande human terapeutisk exponering (upp till 2-faldigt respektive 10-faldigt högre, baserat på Cmax och /eller AUC.
En lindrig fototoxisk hudreaktion observerades hos råtta efter UV-strålning.
Innehåll
Kvalitativ och kvantitativ sammansättning
Tarceva 25 mg filmdragerade tabletter
Varje filmdragerad tablett innehåller 25 mg erlotinib (som erlotinibhydroklorid).
Tarceva 100 mg filmdragerade tabletter
Varje filmdragerad tablett innehåller 100 mg erlotinib (som erlotinibhydroklorid).
Tarceva 150 mg filmdragerade tabletter
Varje filmdragerad tablett innehåller 150 mg erlotinib (som erlotinibhydroklorid).
Hjälpämne med känd effekt
Tarceva 25 mg filmdragerade tabletter
Varje 25 mg filmdragerad tablett innehåller 27,43 mg laktosmonohydrat.
Tarceva 100 mg filmdragerade tabletter
Varje 100 mg filmdragerad tablett innehåller 69,21 mg laktosmonohydrat.
Tarceva 150 mg filmdragerade tabletter
Varje 150 mg filmdragerad tablett innehåller 103,82 mg laktosmonohydrat.
Förteckning över hjälpämnen
Tablettkärna
Laktosmonohydrat
Mikrokristallin cellulosa (E460)
Natriumstärkelseglykolat Typ A
Natriumlaurylsulfat
Magnesiumstearat (E470b)
Tabletthölje
Hydroxipropylcellulosa (E463)
Titandioxid (E171)
Makrogol
Hypromellos (E464)
Blandbarhet
Ej relevant.
Hållbarhet, förvaring och hantering
Hållbarhet
4 år.
Särskilda förvaringsanvisningar
Inga särskilda förvaringsanvisningar.
Särskilda anvisningar för destruktion
Inga särskilda anvisningar för destruktion.
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.
Förpackningsinformation
Filmdragerad tablett 25 mg
Vit till gulaktig, rund, bikonvex filmdragerad tablett med "T 25" ingraverat på ena sidan.
30 styck blister (fri prissättning), tillhandahålls ej
Filmdragerad tablett 100 mg
Vit till gulaktig, rund, bikonvex filmdragerad tablett med "T 100" ingraverat på ena sidan
30 styck blister (fri prissättning), tillhandahålls ej
Filmdragerad tablett 150 mg
Vit till gulaktig, rund, bikonvex, filmdragerad tablett med "T 150" ingraverat på ena sidan
30 styck blister (fri prissättning), tillhandahålls ej
Följande produkter har även parallelldistribuerade förpackningar:
Filmdragerad tablett 100 mg
Filmdragerad tablett 150 mg




