Transiderm-Nitro
Glyceryltrinitrat
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel.
-
Spara denna information, du kan behöva läsa den igen.
-
Om du har ytterligare frågor vänd dig till läkare eller apotekspersonal.
-
Detta läkemedel har ordinerats åt dig. Ge det inte till andra. Det kan skada dem, även om de uppvisar symtom som liknar dina.
-
Om några biverkningar blir värre eller om du märker några biverkningar som inte nämns i denna information, kontakta läkare eller apotekspersonal.
I denna bipacksedel finner du information om:
1. VAD TRANSIDERM-NITRO ÄR OCH VAD DET ANVÄNDS FÖR
2. INNAN DU ANVÄNDER TRANSIDERM-NITRO
3. HUR DU ANVÄNDER TRANSIDERM-NITRO
4. EVENTUELLA BIVERKNINGAR
5. HUR TRANSIDERM-NITRO SKA FÖRVARAS
6. ÖVRIGA UPPLYSNINGAR
1. VAD TRANSIDERM-NITRO ÄR OCH VAD DET ANVÄNDS FÖR
Transiderm-Nitro vidgar blodkärlen och underlättar på så sätt hjärtats arbete.
Transiderm-Nitro är ett plåster avsett för tillförsel av nitroglycerin genom huden och ut i blodet. Det verksamma ämnet finns upplagrat i plåstret och frisätts med en jämn och låg takt under minst ett dygn.
Transiderm-Nitro används för att förhindra att kärlkramp i hjärtat uppstår (angina pectoris).
2. INNAN DU ANVÄNDER TRANSIDERM-NITRO
Använd inte Transiderm-Nitro
-
om du är allergisk (överkänslig) mot glycerylnitrat, andra nitrater eller mot något av övriga innehållsämnen i Transiderm-Nitro
-
om du samtidigt behandlas med fosfodiesterashämmare typ 5 (PDE5) t.ex. sildenafil mot impotens.
-
om du har påverkad blodcirkulation med mycket lågt blodtryck (chock) eller systoliskt blodtryck under 90 mmHg
-
om du har allvarlig vätskebrist.
-
om du har hjärtmuskelsjukdom på grund av blockering i hjärtat (som vid aorta-/ mitralisstenos)
-
om du har hjärtsäcksinflammation (perikardit) eller vätskeansamlig i hjärtsäcken (perikardiell tamponad)
-
om du har förhöjt tryck i skallen
Var särskilt försiktig med Transiderm-Nitro
Rådgör med läkare innan behandling med Transiderm-Nitro påbörjas om du:
-
har blodbrist (anemi)
-
har bristande syresättning av blodet (hypoxemi)
-
har någon sjukdom som påverkar syresättning och genomströmning av blod (t.ex. hjärtsvikt eller lungsjukdom)
-
nyligen har haft hjärtinfarkt eller akut hjärtsvikt
-
har lågt blodtryck
-
har cerebrovaskulär sjukdom (t.ex. hjärnblödning eller blodpropp i hjärnan)
-
har andra hjärt-kärlsjukdomar
-
har nedsatt sköldkörtelfunktion
Att tänka på under behandlingen:
-
Under perioder utan plåster kan kärlkrampen förvärras, kontakta din läkare om detta händer dig.
-
Om tolerans utvecklas mot plåstret kan effekten av nitroglycerin som används under tungan vid ansträngning minskas.
-
Det är viktigt att du vid ett eventuellt sjukhusbesök informerar sjukvårdspersonal om att du använder Transiderm-Nitro. Plåstret innehåller ett aluminiumskikt och ska avlägsnas innan kroppen utsätts för magnetiska fält eller elkonvertering.
Användning av andra läkemedel
Tala om för läkare eller apotekspersonal om du tar eller nyligen har tagit andra läkemedel, även receptfria sådana.
Läkemedel mot impotens så kallade fosfodiesterashämmare typ 5 (PDE5) t.ex. sildenafil ska inte användas under behandling med Transiderm-Nitro.
Transiderm-Nitro kan påverka eller påverkas av vissa läkemedel som används vid behandling av:
-
depression (tricykliskt antidepressiva läkemedel)
-
psykisk sjukdom (antipsykotiska läkemedel)
-
högt blodtryck till exempel kalciumantagonister, ACE-hämmare, beta-receptorblockerare, vätskedrivande medel (diuretika)
-
cancer (amifostin)
-
smärta, feber och inflammation så kallade NSAID och acetylsalicylsyra
-
migrän (dihydroergotamin)
-
blodproppar (heparin)
Användning av Transiderm-Nitro med mat och dryck
Var försiktig vid samtidig användning av alkohol och Transiderm-Nitro eftersom den blodtryckssänkande effekten av Transiderm-Nitro kan förstärkas vid samtidigt intag av alkohol.
Graviditet och amning
Begränsad erfarenhet av användning av Transiderm-Nitro under graviditet. Rådgör därför med läkare före användning under graviditet.
Okänt om Transiderm-Nitro går över i modersmjölk. Rådgör därför med läkare före användning under amning.
Körförmåga och användning av maskiner
Du bör inte köra bil eller använda verktyg och maskiner om du känner av biverkningar som kan påverka din reaktionsförmåga, såsom yrsel och blodtrycksfall.
Du är själv ansvarig för att bedöma om du är i kondition att framföra motorfordon eller utföra arbete som kräver skärpt uppmärksamhet. En av faktorerna som kan påverka din förmåga i dessa avseenden är användning av läkemedel på grund av deras effekter och/eller biverkningar. Beskrivning av dessa effekter och biverkningar finns i andra avsnitt. Läs därför all information i denna bipacksedel för vägledning. Diskutera med läkare eller apotekspersonal om du är osäker.
3. HUR DU ANVÄNDER TRANSIDERM-NITRO
Dosen bestäms av läkaren, som avpassar den individuellt för Dig. Använd alltid Transiderm-Nitro enligt läkarens anvisningar. Rådfråga läkare eller apotekspersonal om du är osäker.
Vanlig dos är 5-10 mg/24 timmar (ett depotplåster per dygn).
Vid upprepad behandling kan effekten försvagas. För att undvika detta görs ett uppehåll på 8-12 timmar, under den symtomfria delen av dygnet, genom att t ex avlägsna plåstret vid sänggåendet och sätta på ett nytt igen på morgonen.
Bruksanvisning
Varje Transiderm-Nitro finns i en lufttät innerförpackning.
1. Riv (klipp inte) i skåran och tag ut plåstret.
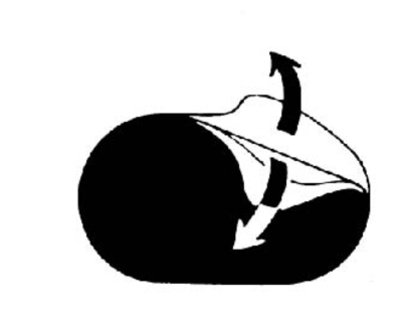
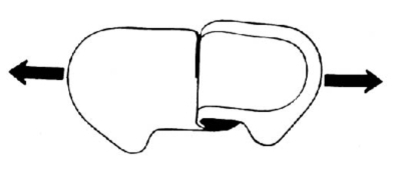
2. Vik ned den lilla fliken och drag långsamt bort hela den vita skyddsplasten (se fig. A-B).
|
A |
B |
| 
|
3. Fäst plåstret på ett torrt, rent och hårfritt ställe på sidan av bröstkorgen genom att pressa det mot huden i minst 10-15 sekunder. Plåstret byts varje dygn och ett nytt plåster fästs då på ett nytt ställe på bröstkorgen. Samma ställe bör inte användas igen förrän efter några dagar för att minska risken för hudbesvär. Hudytan där plåstret fästs bör inte vara röd eller irriterad, eller insmord med hudlotion eller kräm. Om plåstret lossnar, kan man prova att fästa det igen. Går inte det, tag ett nytt och fäst på en ny hudyta så snart som möjligt.
När plåstret avlägsnas, viks det ihop och kasseras så att inte barn kan komma åt det.
Plåstret sitter väl fast och kan behållas på under bad, dusch och fysisk aktivitet men bör tas av vid bastubad.
Om du använt för stor mängd av Transiderm-Nitro
Om Du fått i dig för stor mängd läkemedel eller om t.ex. ett barn fått i sig läkemedlet av misstag kontakta läkare, sjukhus eller Giftinformationscentralen (tel. 112) för bedömning av risken samt rådgivning.
Om du har glömt att använda Transiderm-Nitro
Om du upptäcker att du glömt att byta plåster, byt plåster så snart du kan. Ta sedan av plåstret vid samma tidpunkt som vanligt.
Om du slutar att använda Transiderm-Nitro
Avsluta inte behandlingen utan att rådgöra med behandlande läkare. Alternativ behandling bör påbörjas innan behandlingen med Transiderm-Nitro avslutas.
4. EVENTUELLA BIVERKNINGAR
Liksom alla läkemedel kan Transiderm-Nitro orsaka biverkningar men alla användare behöver inte få dem.
Mycket vanliga (förekommer hos fler än 1 av 10 användare): Illamående, kräkningar.
Vanliga (förekommer hos fler än 1 av 100 användare): Huvudvärk. Ungefär hälften av patienterna får huvudvärk i början av behandlingen. Den försvinner vanligen inom någon vecka.
Mindre vanliga (förekommer hos färre än en av 100 användare): Allergisk hudinflammation efter kontakt med plåstret, rodnad, klåda, sveda, lokal hudirritation.
Sällsynta (förekommer hos färre än 1 av 1000 användare): Hjärtklappning, lågt blodtryck, plötslig värmekänsla, ofta med rodnad.
Mycket sällsynta (förekommer hos färre än 1 av 10 000 användare): Yrsel
Ingen känd frekvens: (kan inte beräknas från tillgängliga data): Hudutslag. Kontakta din läkare om detta påverkar dig allvarligt.
Den lätta rodnaden som kan uppstå vid borttagande av plåstret försvinner vanligtvis inom ett par timmar. För att förebygga hudirritation ska platsen på huden där plåstret fästs varieras.
Om några biverkningar blir värre eller om du märker några biverkningar som inte nämns i denna information, kontakta läkare eller apotekspersonal.
5. HUR TRANSIDERM-NITRO SKA FÖRVARAS
Förvaras utom syn- och räckhåll för barn
Används före utgångsdatum som anges på förpackningen. Utgångsdatumet är den sista dagen i angiven månad.
Använt plåster ska vikas ihop med den klibbiga sidan inåt och kasseras på ett säkert sätt så att barn inte kommer åt plåstret. Om din kommun bränner hushållsavfall går det bra att kasta plåstret tillsammans med hushållssoporna. Annars lämnas använt plåster tillbaka till apotek, helst i originalförpackningen. Oanvänt läkemedel ska inte spolas ner i toaletten eller kastas bland hushållsavfall. Fråga på apoteket hur man gör med läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
6. ÖVRIGA UPPLYSNINGAR
Innehållsdeklaration
-
Den aktiva substansen är glyceryltrinitrat.
1 plåster à 5 mg/24 timmar innehåller: Glyceryltrinitrat 25 mg.
1 plåster à 10 mg/24 tim innehåller: Glyceryltrinitrat 50 mg.
-
Övriga innehållsämnen är laktos, dimetikon (flytande silikon) och aerosil 200 (vattenfri kolloidal kiseldioxid).
-
Övriga ingående komponenter i plåstret: copolymer av etylen-vinylacetat, silikonbaserad häftmassa (medicinskt klister CH15).
Läkemedlets utseende och förpackningsstorlekar
Transiderm-Nitro tillhandahålls i förpackningar om 100 plåster.
Innehavare av godkännande för försäljning
Sandoz A/S
Edvard Thomsens Vej 14
2300 Köpenhamn S
Danmark
Denna bipacksedel godkändes senast den 2023-05-06




