Phoxilium
kalciumkloriddihydrat, magnesiumkloridhexahydrat, natriumklorid, natriumvätekarbonat, kaliumklorid, dinatriumfosfatdihydrat
Läs noga igenom denna bipacksedel innan du börjar använda detta läkemedel. Den innehåller information som är viktig för dig.
-
Spara denna information, du kan behöva läsa den igen.
-
Om du har ytterligare frågor vänd dig till läkare, apotekspersonal eller sjuksköterska.
-
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Se avsnitt 4.
I denna bipacksedel finner du information om:
1. Vad Phoxilium är och vad det används för
2. Vad du behöver veta innan du använder Phoxilium
3. Hur du använder Phoxilium
4. Eventuella biverkningar
5. Hur Phoxilium ska förvaras
6. Förpackningens innehåll och övriga upplysningar
1. Vad Phoxilium är och vad det används för
Phoxilium tillhör gruppen hemofiltrationsvätskor och innehåller kalciumkloriddihydrat, magnesiumkloridhexahydrat, natriumklorid, natriumvätekarbonat, kaliumklorid och dinatriumfosfatdihydrat.
Phoxilium används på sjukhus inom intensivvårdsbehandling för att korrigera kemisk obalans i blodet orsakad av njurskada.
Kontinuerlig njurersättningsbehandling används för att avlägsna avfallsprodukter från blodet som ansamlats när njurarna inte fungerar.
Phoxilium lösning används främst för att behandla kritiskt sjuka patienter med akut njurskada och:
-
normal kaliumhalt i blodet eller
-
normal eller låg fosfathalt (hypofosfatemi) i blodet.
Detta läkemedel kan också användas vid läkemedelsförgiftning eller intoxikation av dialyserbara eller filtrerbara substanser.
2. Vad du behöver veta innan du använder Phoxilium
Använd inte Phoxilium i följande tre fall:
-
hög kaliumhalt i blodet (hyperkalemi)
-
hög bikarbonathalt i blodet (metabolisk alkalos)
-
hög fosfathalt i blodet (hyperfosfatemi).
Använd inte hemodialys eller hemofiltration i något av följande tre fall:
-
om symtom orsakade av hög halt av urinämne i blodet (uremiska symtom) till följd av njurskada med uttalad hyperkatabolism (onormalt hög nedbrytning av vävnader) inte kan korrigeras med hemofiltration
-
om det arteriella trycket i kärlaccessen är otillräckligt
-
om koaguleringsförmågan är minskad (systemisk antikoagulering) och det föreligger hög risk för blödning.
Varningar och försiktighet
Tala med läkare, apotekspersonal eller sjuksköterska innan du använder Phoxilium.
Före och under behandling kommer ditt blodtillstånd att kontrolleras och exempelvis syra/bas-balansen och saltkoncentrationen i blodet (elektrolyter) att övervakas, inklusive all vätsketillförsel (intravenös infusion) och alla vätskeuttag (urinproduktion), även de som inte är direkt relaterade till behandlingen.
Andra läkemedel och Phoxilium
Tala om för läkare eller apotekspersonal om du använder, nyligen har använt eller kan tänkas använda andra läkemedel. Det är viktigt eftersom koncentrationen av andra läkemedel kan påverka behandlingen med Phoxilium. Din läkare beslutar om doseringen av de läkemedel du tar eventuellt måste justeras.
Det är särskilt viktigt att du talar om för läkare om du tar något av följande:
-
Ytterligare fosfatkällor (t.ex. nutritionsvätskor) eftersom de kan öka risken för en hög fosfatkoncentration i blodet (hyperfosfatemi).
-
Vitamin D och läkemedel som innehåller kalciumklorid eller kalciumglukonat eftersom de kan öka risken för hög kalciumkoncentration i blodet (hyperkalcemi).
-
Natriumbikarbonat eftersom det kan öka risken för överskott av bikarbonat i blodet (metabolisk alkalos).
-
När citrat används för att motverka blodkoagulation, eftersom det kan det sänka kalciumkoncentrationen i blodet.
Graviditet, amning och fertilitet
Graviditet och amning:
Det finns inga dokumenterade kliniska data om användning av detta läkemedel under graviditet eller amning. Detta läkemedel ska endast ges till gravida eller ammande kvinnor om det finns ett tydligt behov.
Fertilitet:
Inga effekter på fertiliteten förväntas eftersom kalcium, natrium, kalium, magnesium, klorid, vätefosfat och vätekarbonat är normala beståndsdelar i kroppen.
Körförmåga och användning av maskiner
Phoxilium påverkar inte förmågan att framföra fordon eller använda maskiner.
3. Hur du använder Phoxilium
Phoxilium ska användas på sjukhus och enbart administreras av sjukvårdspersonal. Volymen av Phoxilium, och därmed den dos som används, kommer att bero på ditt tillstånd. Doseringen kommer att avgöras av den läkare som är ansvarig för din behandling.
Phoxilium kan administreras direkt i blodomloppet (intravenöst) genom en CRRT-maskin eller via hemodialys där lösningen flödar på ena sida av ett dialysmembran medan blodet flödar på den andra sidan.
Använd alltid detta läkemedel exakt enligt anvisningar från läkare, apotekspersonal eller sjuksköterska. Rådfråga läkare, apotekspersonal eller sjuksköterska om du är osäker.
Instruktioner för användning hittar du i delen ”Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal”.
Om du använt för stor mängd av Phoxilium
Phoxilium ska användas på sjukhus och endast administreras av sjukvårdspersonal, och din vätskebalans och blodstatus kommer att kontrolleras noga.
Därför är det föga troligt att du kommer att använda för stor mängd av Phoxilium.
Om det osannolika skulle inträffa och du får en överdos kommer din läkare att vidta nödvändiga åtgärder och anpassa din dos.
Överdosering kan resultera i övervätskning, reduktion av bikarbonatkoncentrationen i blodet (metabol acidos) och/eller hög fosfathalt (hyperfosfatemi) om du har njurskada.
Det kan leda till allvarliga konsekvenser, såsom hjärtsvikt eller rubbningar i blodstatus.
Om du har ytterligare frågor om detta läkemedel kontakta läkare eller apotekspersonal.
4. Eventuella biverkningar
Liksom alla läkemedel kan detta läkemedel orsaka biverkningar, men alla användare behöver inte få dem.
Följande tre biverkningar som är relaterade till användning av Phoxilium kan förekomma:
-
onormalt hög eller låg vätskenivå i kroppen (hyper- eller hypovolemi)
-
förändrad saltbalans i blodet (rubbad elektrolytbalans som t.ex. hyperfosfatemi)
-
förhöjd bikarbonathalt i blodet (metabolisk alkalos) eller reduktion av bikarbonathalten i blodet (metabol acidos).
Det finns också vissa biverkningar som kan orsakas av dialysbehandlingar, såsom:
-
illamående, kräkningar, muskelkramp och lågt blodtryck (hypotoni).
Rapportering av biverkningar
Om du får biverkningar, tala med läkare, apotekspersonal eller sjuksköterska. Detta gäller även eventuella biverkningar som inte nämns i denna information. Du kan också rapportera biverkningar direkt till Läkemedelsverket, www.lakemedelsverket.se. Genom att rapportera biverkningar kan du bidra till att öka informationen om läkemedels säkerhet. Postadress
Läkemedelsverket
Box 26
751 03 Uppsala
5. Hur Phoxilium ska förvaras
Förvara detta läkemedel utom syn- och räckhåll för barn.
Används före utgångsdatum som anges på etiketten och på förpackningen. Utgångsdatumet är den sista dagen i angiven månad.
Förvaras mellan +4 °C och +30 °C. Förvaras i skydd mot kyla. Får ej frysas.
För den färdigblandade lösningen har kemisk och fysikalisk stabilitet under användning påvisats upp till 24 timmar vid 22 °C. Om den inte används omedelbart är förvaringstiden och förvaringsvillkoren före administrering användarens ansvar och bör inte överstiga 24 timmar, inklusive behandlingstiden.
Använd inte detta läkemedel om lösningen är grumlig eller om omslaget är skadat. Alla förseglingar måste vara obrutna.
Läkemedel ska inte kastas i avloppet eller bland hushållsavfall. Fråga apotekspersonalen hur man kastar läkemedel som inte längre används. Dessa åtgärder är till för att skydda miljön.
6. Förpackningens innehåll och övriga upplysningar
Innehållsdeklaration
De aktiva substanserna före och efter beredning (blandning) visas nedan.
Aktiva substanser före beredning:
1 000 ml lösning från den lilla kammaren (A) innehåller:
|
Kalciumklorid, 2 H2O |
3,68 g |
|
Magnesiumklorid, 6 H2O |
2,44 g |
1 000 ml lösning från den stora kammaren (B) innehåller:
|
Natriumklorid |
6,44 g |
|
Natriumvätekarbonat |
2,92 g |
|
Kaliumklorid |
0,314 g |
|
Dinatriumfosfat, 2 H2O |
0,225 g |
Aktiva substanser efter beredning:
Lösningarna i kamrarna A (250 ml) och B (4 750 ml) bereds till den färdigblandade lösningen (5 000 ml) vars sammansättning är:
|
mmol/l |
|
|
Kalcium Ca2+ |
1,25 |
|
Magnesium Mg2+ |
0,6 |
|
Natrium, Na+ |
140 |
|
Klorid, Cl- |
115,9 |
|
Vätefosfat, HPO42- |
1,2 |
|
Vätekarbonat, HCO3- |
30 |
|
Kalium, K+ |
4 |
Teoretisk osmolaritet: 293 mOsm/l
Övriga innehållsämnen är:
-
koldioxid (för pH-justering) E 290
-
saltsyra (för pH-justering) E 507
-
vatten för injektionsvätskor.
Läkemedlets utseende och förpackningsstorlekar
Phoxilium är en lösning för hemodialys och hemofiltration och är förpackad i en tvåkammarpåse. Den färdigblandade lösningen erhålles genom att förslutningen bryts och de båda lösningarna blandas. Den färdigblandade lösningen är klar och färglös. Varje påse (A+B) innehåller 5 000 ml lösning för hemodialys och hemofiltration. Påsen är överdragen med en genomskinlig film.
Varje kartong innehåller två påsar och en bipacksedel.
Innehavare av godkännande för försäljning
Baxter Holding B.V.
Kobaltweg 49
3542CE Utrecht
Nederländerna
Tillverkare:
Bieffe Medital S.p.A.
Via Stelvio 94
23035 Sondalo (SO)
ITALIEN
eller
Baxter Healthcare S.A.
Moneen Road, Castlebar
County Mayo, F23 XR63
Irland
Lokal företrädare
Baxter Medical AB
Box 63
164 94 Kista
Denna bipacksedel ändrades senast 2023-12-11
Följande uppgifter är endast avsedda för hälso- och sjukvårdspersonal:
Phoxilium® 1,2 mmol/l fosfat
hemodialysvätska/ hemofiltrationsvätska
Försiktighet
Instruktionerna för användning/hantering av Phoxilium måste följas noggrant.
Lösningarna i de två kamrarna måste blandas före användning.
Användning av en kontaminerad lösning kan orsaka sepsis och chock.
Phoxilium får värmas till 37 °C för att öka patientens komfort. Uppvärmning av vätskan före användning ska utföras före beredning med endast torr värme. Vätskor får inte värmas i vatten eller i en mikrovågsugn. Phoxilium ska kontrolleras visuellt avseende partiklar och missfärgningar före administrering. Administrera inte om vätskan inte är klar eller om förseglingen inte är intakt.
Koncentrationen av oorganiska fosfater bör mätas regelbundet. Tillsats av oorganiska fosfater måste göras i de fall låga fosfatvärden i blodet föreligger.
Ytterligare tillsats av natriumbikarbonat kan öka risken för metabolisk alkalos.
Vid vätskeobalans måste det kliniska tillståndet noga övervakas och vätskebalansen återställas.
• Vid hypervolemi kan hastigheten hos den nettoultrafiltrering som ordinerats för CRRT-enheten ökas och/eller tillförselhastigheten hos vätskor som inte är ersättningsvätskor och/eller dialysat sänkas.
• Vid hypovolemi kan hastigheten hos den nettoultrafiltrering som ordinerats för CRRT-enheten sänkas och/eller tillförselhastigheten hos vätskor som inte är ersättningsvätskebalans och/eller dialysat ökas.
Varningar:
Phoxilium ska inte användas till patienter med hyperkalemi. Kaliumkoncentrationen i blodet måste övervakas före och under hemofiltration och/eller hemodialys.
Eftersom Phoxilium är en lösning innehållandes kalium kan hyperkalemi uppstå tillfälligt efter att behandlingen har påbörjats. Sänk infusionstakten till dess att önskad kaliumkoncentration uppnås. Om tillståndet hyperkalemi inte försvinner ska administreringen avbrytas direkt.
Om hyperkalemi utvecklas när Phoxilium används som dialysat kan administrering av kaliumfritt dialysat vara nödvändigt för att kalium ska avlägsnas snabbare.
Eftersom Phoxilium är en lösning innehållandes fosfat kan hyperfosfatemi uppstå tillfälligt efter att behandlingen har påbörjats. Sänk infusionstakten till dess att önskad fosfatkoncentration uppnås. Om tillståndet hyperfosfatemi inte försvinner ska administreringen avbrytas direkt.
Elektrolyt- och syra/bas-parametrar i blodet ska övervakas regelbundet i patienter som behandlas med Phoxilium. Phoxilium innehåller vätefosfat som är en svag syra som kan påverka patientens syra/bas-balans. Om metabol acidos utvecklas eller förvärras under behandling med Phoxilium kan man behöva sänka infusionstakten eller avbryta administreringen.
Eftersom Phoxilium inte innehåller glukos kan administrering leda till hypoglykemi. Blodglukosnivåer ska regelbundet övervakas hos patienter med diabetes (i synnerhet patienter som får insulin eller andra glukossänkande läkemedel) men även övervägas hos patienter som inte har diabetes, t.ex. med tanke på risken för dold hypoglykemi under behandlingen. Om hypoglykemi utvecklas ska användning av en vätska som innehåller glukos övervägas. Andra korrigerande åtgärder kan vara nödvändiga för att upprätthålla önskad glykemisk kontroll.
Dosering:
Vilken volym och hastighet av Phoxilium som administreras beror på koncentrationen av fosfat och andra elektrolyter i blodet, syra/bas-balansen, vätskebalansen och patientens övergripande kliniska tillstånd. Volymen av ersättningsvätska och/eller dialysat som administreras beror också på den önskade behandlingseffekten (dosen). Administration (dos, infusionshastighet och ackumulerad volym) av Phoxilium ska endast fastställas av en läkare med erfarenhet av intensivvård och CRRT (kontinuerlig njurersättningsterapi).
Doseringen bestäms och ordineras därför av ansvarig läkare.
Flödeshastighetsområde för ersättningslösning vid hemofiltration och hemodiafiltration:
Vuxna: 500–3 000 ml/h
Flödeshastighetsområde för dialysat vid kontinuerlig hemodialys och kontinuerlig hemodiafiltration:
Vuxna: 500–2 500 ml/h
Vanliga kombinerade totala flödeshastigheter för CRRT (dialysat och ersättningsvätskor) för vuxna är cirka 2 000 till 2 500 ml/h, vilket motsvarar en dygnsmängd vätska på cirka 48 till 60 l.
Pediatrisk population:
Hos barn från nyfödda till ungdomar upp till 18 år är flödeshastighetsområdet vid användning som ersättningsvätska i hemofiltration och hemodiafiltration och som dialysvätska (dialysat) i kontinuerlig hemodialys och kontinuerlig hemodiafiltration 1 000 till 4 000 ml/h/1,73 m2.
För ungdomar (12‑18 år) ska dosrekommendationen för vuxna användas när den beräknade pediatriska dosen överskrider den högsta dosen för vuxna.
Instruktioner för användning/hantering
Vätskan i den lilla kammaren A läggs till vätskan i den stora kammaren B efter att svetsfogen öppnats omedelbart före användning. Den blandade vätskan ska vara klar och färglös.
Använd aseptisk teknik under hela hanteringen och administreringen till patienten.
Använd endast om omslaget är oskadat, alla förseglingar är intakta, svetsfogen inte har öppnats och vätskan är klar. Kläm ordentligt på påsen för att kontrollera den avseende läckage. Kassera lösningen omedelbart om du upptäcker något läckage eftersom steriliteten då inte kan garanteras.
Den stora kammaren (B) är utrustad med en injektionsport för att kunna tillsätta andra nödvändiga läkemedel efter det att lösningen blandats. Det är användarens ansvar att bedöma om ett tillsatt läkemedel är kompatibelt med Phoxilium genom att kontrollera eventuell färgförändring och/eller eventuella fällningar, olösliga komplex eller kristaller. Innan ett läkemedel tillsätts, verifiera att det är lösligt och stabilt i detta läkemedel och att pH-intervallet i Phoxilium är passande (pH-värdet i blandad vätska är 7,0-8,5). Tillsatser kan vara inkompatibla. Bruksanvisningen för läkemedlet som ska tillsättas måste konsulteras.
Töm injektionsporten på all vätska. Vänd påsen uppochned och för in läkemedlet genom injektionsporten. Blanda ordentligt. Tillsättning och blandning av tillsatser måste alltid utföras innan påsen ansluts till den extrakorporeala kretsen. Lösningen måste administreras omedelbart.
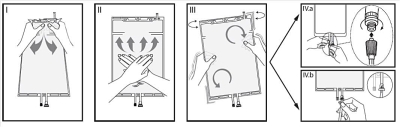
I Ta bort ytterförpackningen från påsen precis före användning och kasta bort annat förpackningsmaterial. Öppna förseglingen genom att hålla den lilla kammaren med båda händerna och trycka tills det blir en öppning i förslutningen mellan de två kamrarna. (Se figur I nedan.)
II Tryck med båda händerna på den stora kammaren tills svetsfogen (peel-seal-förslutningen) mellan de två kamrarna är helt öppen. (Se figur II nedan.)
III Se till att lösningen är helt blandad genom att försiktigt skaka påsen. Lösningen är nu klar att användas och kan hängas upp på utrustningen. (Se figur III nedan.)
IV Anslut slangen för dialys- eller ersättningsvätska till någon av de två accessportarna.
IV.a Om luerkopplingen används, ta bort skyddshatten genom att vrida och dra och anslut luerkopplingen (hane) på slangen för dialys- eller ersättningsvätskan till luerkopplingen (hona) på påsen genom att trycka och vrida. Se till att kopplingen sitter ordentligt och dra åt. Kopplingen är nu öppen. Kontrollera att vätskan flödar fritt. (Se figur IV.a nedan.)
När slangen för dialys- eller ersättningsvätska har kopplats bort från luerkopplingen stängs kopplingen och lösningsflödet upphör. Luerporten är nålfri och kan rengöras.
IV.b Om injektionsporten används, ta först bort skyddshatten. Injektionsporten kan rengöras. För sedan in spetsen genom gummimembranet. Kontrollera att vätskan flödar fritt. (Se figur IV.b nedan.)
Den färdigblandade lösningen ska användas omedelbart. Om den inte används omedelbart ska den användas inom 24 timmar, inklusive behandlingstid, efter det att lösning A blandats i lösning B.
Den färdigblandade lösningen är endast avsedd för engångsbruk. Kassera oanvänd lösning omedelbart efter användning.
Ej använt läkemedel och avfall ska kasseras enligt gällande anvisningar.